Неправильний вибір кабельних вводів в медичних установах і чистих приміщеннях спричиняє ризики забруднення, порушення нормативних вимог і несправності обладнання, що призводить до загрози безпеці пацієнтів, дорогих зупинок виробництва і порушень FDA, а неналежна герметизація, невідповідні матеріали і погане очищення призводять до розмноження бактерій, забруднення твердими частинками і порушення стерильності, які ставлять під загрозу критично важливі операції в охороні здоров'я. Багато керівників закладів стикаються з проблемою вибору залоз, які б відповідали суворим медичним стандартам, зберігаючи при цьому надійні електричні характеристики.
Вибір кабельних вводів для медичного обладнання та чистих приміщень вимагає розуміння правил FDA, Клас USP VI1 Вимоги до матеріалів, стандарти герметизації IP68+ і вимоги до класифікації чистих приміщень, з медичної нержавіючої сталі або спеціальної полімерної конструкції, що забезпечує біосумісність, хімічну стійкість і гладкі поверхні для ефективного очищення і стерилізації, зберігаючи при цьому електричну цілісність у критично важливих сферах охорони здоров'я. Успіх залежить від балансу між дотриманням регуляторних вимог та експлуатаційною надійністю.
Працюючи з інженерами великих медичних центрів у Бостоні, фармацевтичними виробниками у Швейцарії та чистими приміщеннями в Сінгапурі, я дізнався, що кабельні вводи медичного призначення необхідні для підтримання стерильного середовища та забезпечення безпеки пацієнтів. Дозвольте мені поділитися важливими знаннями для вибору оптимальних сальників для вашої медичної галузі та чистих приміщень.
Зміст
- Чим медичні кабельні вводи відрізняються від стандартних вводів?
- Як ви дотримуєтеся вимог FDA та правил щодо медичних виробів?
- Які матеріали потрібні для застосування в чистих приміщеннях?
- Як забезпечити належну сумісність очищення та стерилізації?
- Які ключові критерії вибору для різних медичних застосувань?
- Поширені запитання про медичні кабельні вводи
Чим медичні кабельні вводи відрізняються від стандартних вводів?
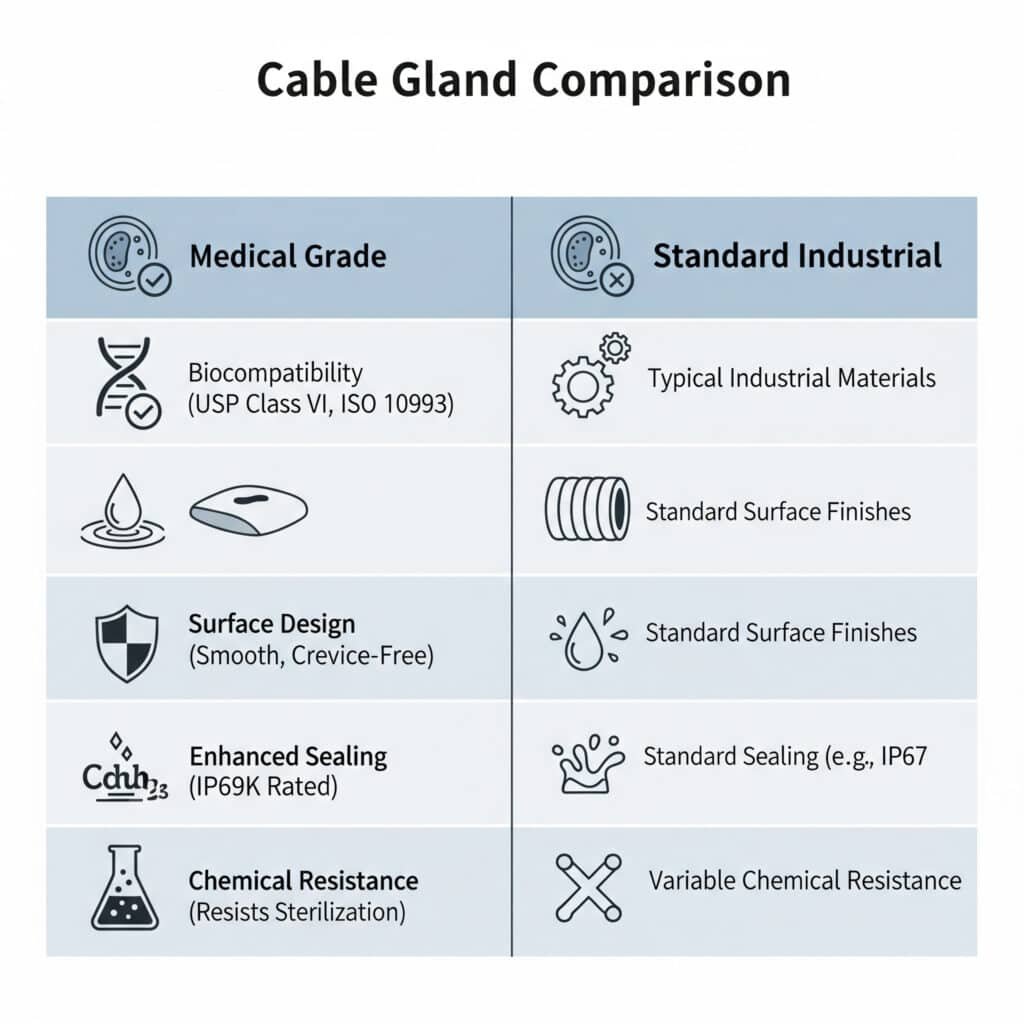
Медичні кабельні вводи відрізняються від стандартних вводів використанням біосумісних матеріалів, гладкою поверхнею, що легко чиститься, відповідністю нормам FDA, посиленим ущільненням для запобігання забрудненню, хімічною стійкістю до миючих засобів і процесів стерилізації, а також спеціалізованою конструкцією, яка усуває щілини, де можуть розмножуватися бактерії, зберігаючи при цьому електричні характеристики в критично важливих для охорони здоров'я середовищах.
Розуміння цих відмінностей має вирішальне значення, оскільки медичне застосування має унікальні вимоги до безпеки та регулювання, які стандартні промислові сальники не можуть адекватно задовольнити.
Вимоги до біосумісності
Відповідність USP класу VI: Медичні кабельні вводи повинні використовувати матеріали, які пройшли біологічні випробування класу VI Фармакопеї США на біосумісність і безпеку при застосуванні в медичних пристроях.
Стандарти ISO 10993: Матеріали повинні відповідати ISO 109932 стандарти біологічної оцінки медичних виробів, що гарантують відсутність цитотоксичного, сенсибілізуючого або подразнюючого впливу на тканини людини.
Схвалення FDA 21 CFR 177: Харчові матеріали, що відповідають вимогам FDA щодо прямого і непрямого контакту з харчовими продуктами, часто потрібні для застосування у фармацевтиці та медичному обладнанні.
Біосумісні полімери: Спеціалізовані матеріали, такі як медичний PEEK, PTFE або нейлон фармацевтичного класу, забезпечують біосумісність без шкоди для механічних властивостей.
Дизайн поверхні для зручності очищення
Гладка обробка поверхні: Медичні залози мають ультрагладку поверхню зі значенням Ra, як правило, нижче 0,8 мікрометра, що запобігає прилипанню бактерій і забезпечує ефективне очищення.
Дизайн без щілин: Усунення гострих кутів, глибоких ниток і складної геометрії, які можуть приховувати бактерії або чинити опір процесам очищення та стерилізації.
Закруглені краї: Усі зовнішні поверхні мають закруглені краї та плавні переходи, щоб полегшити очищення та запобігти пошкодженню рукавичок для чистих приміщень або стерильної упаковки.
Мінімальна площа поверхні: Обтічна конструкція мінімізує площу поверхні, що піддається забрудненню, зберігаючи при цьому необхідні механічні та електричні характеристики.
Покращена ефективність ущільнення
Клас захисту IP68+: Чудовий захист навколишнього середовища, що перевищує стандарт IP68, часто досягаючи рівня IP69K для очищення під високим тиском і при високих температурах.
Бар'єри забруднення: Кілька етапів герметизації запобігають потраплянню частинок, бактерій і миючих засобів, які можуть порушити стерильність середовища.
Опір тиску: Підвищений номінальний тиск, що дозволяє витримувати агресивні процедури очищення та стерилізації без пошкодження ущільнень.
Довгострокова надійність: Ущільнювальні матеріали зберігають цілісність завдяки багаторазовим циклам стерилізації та впливу агресивних миючих засобів.
Властивості хімічної стійкості
Сумісність з миючими засобами: Стійкість до лікарняних дезінфікуючих засобів, четвертинних амонієвих сполук, перекису водню та інших агресивних миючих засобів.
Стійкість до стерилізації: Матеріали витримують гамма-випромінювання, етиленоксид, автоклавування парою та інші методи стерилізації без деградації.
Фармацевтична хімія: Стійкість до розчинників, кислот, лугів і фармацевтичних сполук, які часто зустрічаються в медичному виробництві.
Стабільність температури: Збереження властивостей завдяки температурним циклам стерилізації та вимогам до контролю температури в чистих приміщеннях.
Девід, керівник виробництва на великому фармацевтичному заводі в Нью-Джерсі, зіткнувся з постійними проблемами забруднення на стерильних лініях розливу, де стандартні кабельні сальники приховували бактерії, незважаючи на суворі протоколи очищення. Існуючі латунні сальники мали складну різьбу та поверхню, яка не піддавалася належній стерилізації, що призводило до відбраковування партій та проблем з дотриманням вимог FDA. Ми вибрали кабельні вводи з медичної нержавіючої сталі з електрополірованою поверхнею та безщілинною конструкцією, які відповідали вимогам USP класу VI. Модернізація усунула джерела забруднення, досягла ефективності очищення 99,9% і допомогла підприємству пройти інспекції FDA, одночасно знизивши рівень браку на 85%. 😊
Як ви дотримуєтеся вимог FDA та правил щодо медичних виробів?
Дотримання вимог FDA та правил щодо медичних виробів вимагає використання матеріалів з відповідними сертифікатами, ведення детальної документації, дотримання наступних правил Належна виробнича практика (GMP)3забезпечення простежуваності та впровадження систем якості, що відповідають вимогам 21 CFR, частина 820, з медичними кабельними вводами, що вимагають використання матеріалів, схвалених FDA, тестування на біосумісність і виробничого контролю, які забезпечують стабільну якість і безпеку при застосуванні медичних виробів.
Відповідність нормативним вимогам не підлягає обговоренню в медичному застосуванні, оскільки порушення можуть призвести до шкоди пацієнтам, відкликання продукції та серйозних юридичних наслідків.
Вимоги до матеріалів FDA
21 CFR, частина 177: Матеріали, що контактують з фармацевтичними препаратами або медичними виробами, повинні відповідати вимогам FDA щодо харчових добавок для речовин, що непрямо контактують з харчовими продуктами.
Головний файл доступу (MAF): Постачальники повинні вести основні файли доступу FDA, що документують безпеку матеріалів, виробничі процеси та процедури контролю якості.
Майстер-файл лікарського засобу (DMF): Для фармацевтичних застосувань матеріали можуть потребувати реєстрації реєстраційного досьє на лікарський засіб з детальною інформацією про склад і виробництво.
Сертифікат відповідності: Постачальники повинні надати сертифікати, що підтверджують відповідність матеріалів усім чинним нормам і специфікаціям FDA.
Стандарти якості медичних виробів
Відповідність стандарту ISO 13485: Виробництво повинно відповідати вимогам стандарту ISO 13485 щодо систем управління якістю медичних виробів для розробки, виробництва та постмаркетингового нагляду.
21 CFR, частина 820 (QSR): Відповідність вимогам Положення про систему якості, що забезпечує належний контроль проектування, контроль документації та коригувальні/попереджувальні дії.
Управління ризиками: ISO 14971 Процеси управління ризиками для медичних виробів, включаючи аналіз, оцінку та заходи контролю ризиків.
Дизайнерський контроль: Процеси формального контролю дизайну, включаючи планування дизайну, вимоги до вхідних/вихідних даних, огляди, верифікацію та валідацію.

Документація та простежуваність
Сертифікати на матеріали: Повна простежуваність матеріалів з сертифікатами аналізу, результатами випробувань на біосумісність та документацією про відповідність нормативним вимогам.
Виробничі записи: Детальні виробничі записи, включаючи параметри процесу, тестування контролю якості та документацію партії для повного відстеження.
Контроль змін: Офіційні процедури контролю змін для будь-яких модифікацій матеріалів, процесів або специфікацій, що впливають на відповідність нормативним вимогам.
Кваліфікація постачальника: Комплексні програми кваліфікації постачальників, які гарантують, що всі матеріали та компоненти відповідають вимогам до медичних виробів.
Вимоги до валідації
Тестування на біосумісність: Випробування класу VI USP, включаючи системні ін'єкційні, внутрішньошкірні та імплантаційні випробування для перевірки біологічної безпеки.
Перевірка очищення: Задокументовані процедури очищення з валідаційними даними, що підтверджують ефективне видалення забруднень та зменшення біонавантаження.
Валідація стерилізації: Валідація процесів стерилізації, включаючи картографування доз, рівні забезпечення стерильності та дослідження сумісності матеріалів.
Тестування продуктивності: Електричні, механічні та екологічні випробування для перевірки відповідності характеристик вимогам до медичних виробів протягом усього життєвого циклу продукту.
Підтримка при подачі документів до регуляторних органів
510(k) Документація: Технічна документація, що підтверджує подачу заявок на реєстрацію FDA 510(k) для медичних виробів, що містять кабельні вводи.
Технічні файли: Вичерпні технічні файли для маркування CE відповідно до Регламенту щодо медичних виробів (MDR) на європейських ринках.
Угоди про якість: Офіційні угоди про якість з постачальниками, що визначають обов'язки, специфікації та вимоги до дотримання стандартів.
Аудиторська підтримка: Підтримка аудитів FDA, нотифікованого органу та замовника, включаючи перевірку документації та інспекції об'єктів.
Які матеріали потрібні для застосування в чистих приміщеннях?
Для застосування в чистих приміщеннях потрібні матеріали з низькими властивостями газовиділення, стійкістю до утворення частинок, хімічною сумісністю з миючими засобами, гладкою непористою поверхнею і відповідним рівнем провідності. Медична нержавіюча сталь 316L, PEEK, PTFE і спеціалізовані полімери, схвалені для використання в чистих приміщеннях, забезпечують оптимальні експлуатаційні характеристики при дотриманні наступних вимог. ISO 146444 Стандарти чистих приміщень та підтримка електричної цілісності в контрольованих середовищах.
Вибір матеріалу має вирішальне значення, оскільки чисті приміщення вимагають суворого контролю частинок і молекулярних забруднень, які можуть погіршити якість продукції або стерильні умови.
Вимоги до нержавіючої сталі
316L медичний клас: Аустенітна нержавіюча сталь з низьким вмістом вуглецю забезпечує чудову корозійну стійкість і біосумісність для медичного застосування.
Електрополіроване покриття: Електрополірування усуває дефекти поверхні, зменшує утворення частинок і створює гладку поверхню для ефективного очищення.
Лікування пасивацією: Хімічна пасивація підвищує корозійну стійкість і видаляє забруднення залізом, яке може спричинити зміну кольору або утворення частинок.
Шорсткість поверхні: Значення Ra нижче 0,8 мікрометра (32 мікродюймів) мінімізують адгезію бактерій і полегшують процеси очищення та стерилізації.
Високоефективні полімери
PEEK (поліефірефіркетон): Відмінна хімічна стійкість, низьке газовиділення та біосумісність роблять ПЕЕК ідеальним для застосування у фармацевтиці та медичному обладнанні.
ПТФЕ (політетрафторетилен): Чудова хімічна інертність і антипригарні властивості забезпечують відмінну стійкість до чистячих хімічних засобів і біологічних матеріалів.
Медичні нейлонові шкарпетки: Спеціально розроблені капрони з допуском USP класу VI мають хороші механічні властивості та біосумісність для медичного застосування.
POM, схвалений для використання в чистих приміщеннях: Поліоксиметилен з низьким рівнем утворення частинок і хорошою стабільністю розмірів для застосування в прецизійних чистих приміщеннях.
Сумісність з класифікацією чистих приміщень
Клас ISO 5 (клас 100): Надзвичайно гладкі поверхні з мінімальним утворенням частинок для напівпровідникового та фармацевтичного виробництва.
Клас ISO 6 (клас 1000): Помірний контроль твердих частинок для виробництва медичного обладнання та деяких фармацевтичних процесів.
Клас ISO 7 (клас 10000): Стандартні вимоги до чистоти приміщень для загальних операцій зі складання фармацевтичних та медичних виробів.
Клас ISO 8 (клас 100000): Основні вимоги до чистоти приміщень для пакування та деяких процесів виробництва медичних виробів.
Контроль газовиділення та забруднення
Матеріали з низьким рівнем газовиділення: Матеріали з мінімальними викидами летких органічних сполук (ЛОС), які можуть забруднити чутливі процеси або продукти.
Молекулярне забруднення: Контроль молекулярних забруднювачів, включаючи силікони, пластифікатори та інші органічні сполуки, які можуть вплинути на якість продукції.
Іонне забруднення: Матеріали з низьким вмістом іонів для запобігання забрудненню електронних компонентів і фармацевтичних продуктів.
Речовини, що витягуються: Мінімальна кількість екстрагованих речовин, які можуть потрапити у фармацевтичні продукти або миючі розчини під час використання.
Матриця хімічної сумісності
| Миючий засіб | 316L SS | ПІК | ПТФЕ | Медичний нейлон |
|---|---|---|---|---|
| Ізопропіловий спирт | Чудово. | Чудово. | Чудово. | Добре. |
| Перекис водню | Чудово. | Чудово. | Чудово. | Справедливо |
| Четвертинний амоній | Чудово. | Чудово. | Чудово. | Добре. |
| Гіпохлорит натрію | Добре. | Чудово. | Чудово. | Бідолаха. |
| Оцтова кислота | Добре. | Чудово. | Чудово. | Бідолаха. |
Хассан, який керує виробництвом на сучасному фармацевтичному підприємстві у Швейцарії, потребував модернізації кабельних сальників у чистому приміщенні класу 5 за стандартом ISO для виробництва стерильних ін'єкційних препаратів. Існуючі сальники генерували частинки під час циклів очищення і не витримували агресивних протоколів стерилізації, необхідних для нових біологічних продуктів. Ми запропонували електрополіровані кабельні сальники з нержавіючої сталі 316L з підтвердженим низьким рівнем утворення частинок і повною хімічною сумісністю з їхніми процесами очищення та стерилізації. Модернізація дозволила досягти кількості частинок 90% нижче граничних значень класу 5 ISO, усунути випадки забруднення, пов'язані з очищенням, і підтримати успішну валідацію нової стерильної виробничої лінії.
Як забезпечити належну сумісність очищення та стерилізації?
Забезпечення належної сумісності з очищенням і стерилізацією вимагає вибору матеріалів, які витримують багаторазовий вплив хімічних засобів для очищення і методів стерилізації, проектування поверхонь для повного очищення, валідації процедур очищення і ведення детальної документації, причому медичні кабельні сальники вимагають гладких поверхонь без щілин, хімічно стійких матеріалів і валідованих протоколів очищення, які забезпечують необхідний рівень стерильності.
Сумісність з очищенням і стерилізацією має важливе значення, оскільки неналежна дезінфекція може призвести до забруднення продукту, ризиків для безпеки пацієнта і порушень нормативних вимог.
Сумісність з методами стерилізації
Автоклавування парою: Матеріали повинні витримувати температуру 121°C-134°C автоклавування парою5 циклів без деградації, зміни розмірів або пошкодження ущільнень.
Гамма-випромінювання: Стійкість до доз гамма-випромінювання 25-50 кГр, які зазвичай використовуються для стерилізації медичних виробів без деградації матеріалу.
Оксид етилену (EtO): Хімічна сумісність зі стерилізацією EtO, включаючи стійкість до стерилізатора та належні характеристики дегазації.
Плазма перекису водню: Сумісність із системами низькотемпературної плазмової стерилізації, включаючи стабільність матеріалу і повне проникнення стерилізатора.
Вимоги до валідації очищення
Процедури очищення: Задокументовані процедури очищення із зазначенням хімічних речовин, концентрацій, часу контакту та механічної дії, необхідних для ефективного знезараження.
Протоколи валідації: Офіційні валідаційні дослідження, що демонструють ефективність очищення з використанням найгірших сценаріїв забруднення та аналітичного тестування.
Критерії прийняття: Визначені критерії прийнятності чистоти, включаючи візуальний огляд, підрахунок часток, рівень біологічного навантаження та обмеження хімічних залишків.
Рутинний моніторинг: Програми постійного моніторингу для перевірки ефективності очищення та виявлення будь-якого погіршення продуктивності.
Міркування щодо дизайну поверхні
Особливості дренажу: Конструктивні особливості, які сприяють повному зливу миючих розчинів і запобігають утворенню калюж, в яких можуть накопичуватися забруднення.
Доступність: Всі поверхні повинні бути доступними для очищення за допомогою стандартних засобів для чищення та процедур, що використовуються в медичних установах.
Вимоги до розбирання: Подумайте, чи потрібно розбирати залози для очищення, чи достатньо їхнього цілого очищення для застосування.
Заміна прокладки: Процедури заміни та перевірки прокладок, коли ущільнювальні компоненти потребують періодичної заміни через вплив хімічних засобів для чищення.
Документація та комплаєнс
Інструкція з чищення: Детальні інструкції з очищення, включаючи покрокові процедури, специфікації хімічних речовин та заходи безпеки.
Дані про безпеку матеріалів: Повна інформація про безпеку матеріалів, включаючи хімічну сумісність, температурні обмеження та сумісність зі стерилізацією.
Звіти про перевірку: Звіти про валідацію очищення, що демонструють ефективність і встановлюють вимоги до регулярного моніторингу.
Навчальні матеріали: Навчальні матеріали для персоналу закладу щодо належного очищення, поводження та обслуговування медичних кабельних вводів.
Контроль якості Тестування
Тестування біонавантажень: Регулярне тестування на мікробне забруднення для перевірки ефективності очищення та виявлення потенційних проблемних зон.
Тестування на ендотоксин: Тестування на наявність бактеріальних ендотоксинів, які можуть викликати пірогенні реакції у фармацевтиці та медичному обладнанні.
Підрахунок частинок: Вимірювання кількості частинок для перевірки відповідності вимогам до чистоти приміщень продовжується після очищення та технічного обслуговування.
Аналіз хімічних залишків: Тестування на наявність залишків хімічних речовин, які можуть забруднити продукцію або вплинути на біосумісність.
Які ключові критерії вибору для різних медичних застосувань?
Основні критерії вибору залежать від сфери застосування, але включають вимоги до відповідності нормативним вимогам, рівні біосумісності, класифікацію чистих приміщень, методи стерилізації, хімічний вплив і вимоги до електричних характеристик, причому хірургічне обладнання вимагає найвищої біосумісності, фармацевтичне виробництво - хімічної стійкості, а діагностичне обладнання - електричної цілісності, в той час як для всіх сфер застосування потрібні відповідні нормативні сертифікати і сумісність з очищенням.
Різні медичні застосування мають унікальні вимоги, які необхідно ретельно враховувати при виборі кабельного вводу, щоб забезпечити оптимальну продуктивність і відповідність нормативним вимогам.
Хірургічне обладнання та обладнання для контакту з пацієнтом
Вимоги до прямого контакту: Біосумісність USP класу VI з додатковим тестуванням на цитотоксичність для матеріалів, що безпосередньо контактують з пацієнтом під час хірургічних процедур.
Частота стерилізації: Здатність витримувати часті цикли стерилізації без деградації, що зазвичай вимагає матеріалів, стійких до сотень циклів стерилізації.
Електробезпека: Підвищені вимоги до електробезпеки, включаючи низький струм витоку та надійну ізоляцію обладнання, підключеного до пацієнта.
Аварійна надійність: Критичні вимоги до надійності обладнання для життєзабезпечення та екстреної медичної допомоги, де відмова може безпосередньо вплинути на безпеку пацієнта.
Фармацевтичне виробництво
Відповідність GMP: Вимоги належної виробничої практики, включаючи простежуваність матеріалів, контроль змін і документацію з валідації.
Безпека контакту з продуктом: Матеріали, які не забруднюють фармацевтичну продукцію через вилуговування, утворення частинок або хімічну взаємодію.
Перевірка очищення: Широкі вимоги до валідації очищення з задокументованими процедурами та критеріями прийнятності для фармацевтичного виробництва.
Пакетна документація: Повна документація партії та простежуваність матеріалів, що використовуються у фармацевтичному виробничому обладнанні.
Діагностичне та лабораторне обладнання
Вимоги до точності: Стабільність розмірів і точність для аналітичних приладів, що вимагають стабільних механічних і електричних характеристик.
Хімічна стійкість: Стійкість до лабораторних хімікатів, реактивів і розчинників, які зазвичай використовуються в діагностиці.
Електромагнітні характеристики: Вимоги до електромагнітної сумісності для чутливих аналітичних приладів та діагностичного обладнання.
Стабільність калібрування: Механічна стабільність, яка не впливає на калібрування приладу або точність вимірювань з часом.
Виробництво медичних виробів
Перевірка процесу: Матеріали та компоненти, що відповідають вимогам валідації процесів виробництва медичних виробів.
Системи якості: Інтеграція з системами якості ISO 13485, включаючи кваліфікацію постачальників та процедури вхідного контролю.
Управління ризиками: Матеріали, які підтримують вимоги до управління ризиками медичних виробів, включаючи аналіз режимів відмов і стратегії їх зменшення.
Регуляторна підтримка: Підтримка постачальників у поданні документів до регуляторних органів, включаючи технічну документацію та регуляторну експертизу.
Матриця прийняття рішення про вибір
| Тип програми | Основні критерії | Вторинні критерії | Критичні стандарти |
|---|---|---|---|
| Хірургічне обладнання | Біосумісність | Стерилізація | USP клас VI, ISO 10993 |
| Фармацевтика | Хімічна стійкість | Відповідність вимогам GMP | FDA 21 CFR, cGMP |
| Діагностика | Точність | Електромагнітні характеристики | IEC 61326, ISO 15189 |
| Виробництво | Валідація процесу | Системи якості | ISO 13485, 21 CFR 820 |
Аналіз витрат і вигод
Початкова вартість проти життєвого циклу: Враховуйте загальну вартість володіння, включаючи витрати на технічне обслуговування, заміну та відповідність вимогам протягом усього терміну експлуатації обладнання.
Регуляторний ризик: Збалансуйте матеріальні витрати з ризиками дотримання нормативних вимог та потенційними витратами, пов'язаними з їх недотриманням.
Вимоги до виконання: Переконайтеся, що вибрані матеріали відповідають мінімальним експлуатаційним вимогам без надмірної деталізації, яка невиправдано збільшує витрати.
Можливості постачальників: Оцініть можливості постачальника щодо постійної підтримки, документації та допомоги у дотриманні нормативних вимог.
Висновок
Вибір кабельних вводів для медичного обладнання та чистих приміщень вимагає розуміння унікальних нормативних, матеріальних і експлуатаційних вимог, які відрізняють ці сфери застосування від стандартного промислового використання. Успіх залежить від дотримання балансу між біосумісністю, можливістю очищення, відповідністю нормативним вимогам та електричними характеристиками.
Запорукою надійної роботи медичних кабельних вводів є співпраця з постачальниками, які розуміються на нормативних вимогах до медичних виробів і можуть надати відповідні матеріали, документацію та постійну підтримку протягом усього життєвого циклу виробу. Компанія Bepto спеціалізується на виробництві кабельних вводів медичного призначення, які відповідають вимогам FDA і міжнародним стандартам медичних виробів, забезпечуючи гарантію якості та нормативну підтримку, необхідну для критично важливих застосувань в охороні здоров'я.
Поширені запитання про медичні кабельні вводи
З: Які сертифікати потрібні для медичних кабельних вводів?
A: Медичні кабельні вводи зазвичай вимагають сертифікації біосумісності USP класу VI, відповідності матеріалів FDA 21 CFR і систем якості виробництва ISO 13485. Конкретні вимоги залежать від вашої програми та регуляторної юрисдикції.
З: Чи можна використовувати звичайні кабельні вводи з нержавіючої сталі в медичних цілях?
A: Звичайна нержавіюча сталь може не відповідати медичним вимогам. Для медичних застосувань потрібна медична нержавіюча сталь 316L з електрополірованим покриттям, випробування на біосумісність і належна документація для дотримання нормативних вимог.
З: Як очистити та стерилізувати медичні кабельні вводи?
A: Дотримуйтесь затверджених виробником процедур очищення, використовуючи дозволені миючі засоби та методи стерилізації. Більшість медичних залоз підтримують автоклавування парою, гамма-випромінювання або хімічну стерилізацію за умови належної сумісності матеріалів.
З: У чому різниця між кабельними сальниками для чистих приміщень і медичного призначення?
A: Медичний клас включає вимоги до біосумісності та відповідності FDA, тоді як клас для чистих приміщень фокусується на контролі вмісту частинок і хімічній стійкості. Для деяких застосувань потрібні як медичні, так і специфікації для чистих приміщень.
З: Як часто слід замінювати медичні кабельні сальники?
A: Частота заміни залежить від циклів стерилізації, хімічного впливу та рекомендацій виробника. Зазвичай перевіряють після кожних 100-200 циклів стерилізації і замінюють на основі оцінки стану та вимог валідації.
-
Дізнайтеся про специфічні тести на біологічну реактивність, необхідні для сертифікації USP класу VI. ↩
-
Ознайомтеся з оглядом серії стандартів ISO 10993 для біологічної оцінки медичних виробів. ↩
-
Ознайомтеся з офіційними настановами та правилами FDA щодо поточної належної виробничої практики (cGMP). ↩
-
Ознайомтеся з детальним посібником зі стандартів ISO 14644 для класифікації чистоти повітря в чистих приміщеннях. ↩
-
Розуміти принципи стерилізації парою, зокрема роль часу, температури та тиску. ↩



