Felaktigt val av kabelförskruvningar i medicinska miljöer och renrumsmiljöer orsakar kontamineringsrisker, bristande efterlevnad av regelverk och utrustningsfel som leder till patientsäkerhetsrisker, kostsamma driftstopp och FDA-överträdelser, medan otillräcklig tätning, olämpliga material och dålig rengörbarhet leder till bakterietillväxt, partikelföroreningar och sterilitetsbrott som äventyrar kritisk vårdverksamhet. Många fastighetsförvaltare kämpar med att välja genomföringar som uppfyller stränga medicinska standarder och samtidigt bibehåller tillförlitlig elektrisk prestanda.
För att välja kabelförskruvningar för medicinsk utrustning och renrum måste man förstå FDA:s regler, USP klass VI1 materialkrav, IP68+ tätningsstandarder och behov av renrumsklassificering, med konstruktion i medicinskt rostfritt stål eller specialiserad polymer som ger biokompatibilitet, kemisk beständighet och släta ytor för effektiv rengöring och sterilisering samtidigt som den elektriska integriteten bibehålls i kritiska sjukvårdsapplikationer. För att lyckas måste man balansera regelefterlevnad med driftsäkerhet.
Efter att ha arbetat med sjukhusingenjörer på stora medicinska center i Boston, läkemedelstillverkare i Schweiz och renrumsanläggningar i Singapore har jag lärt mig att kabelförskruvningar av medicinsk kvalitet är avgörande för att upprätthålla sterila miljöer och garantera patientsäkerheten. Låt mig dela med mig av den kritiska kunskapen för att välja optimala kabelförskruvningar för dina medicinska och renrumsapplikationer.
Innehållsförteckning
- Vad skiljer medicinska kabelförskruvningar från standardförskruvningar?
- Hur uppfyller du FDA:s och de medicintekniska föreskrifterna?
- Vilka material krävs för renrumsapplikationer?
- Hur säkerställer du korrekt rengöring och steriliseringskompatibilitet?
- Vilka är de viktigaste urvalskriterierna för olika medicinska tillämpningar?
- Vanliga frågor om medicinska kabelgenomföringar
Vad skiljer medicinska kabelförskruvningar från standardförskruvningar?
Kabelförskruvningar för medicinskt bruk skiljer sig från standardförskruvningar genom att använda biokompatibla material, ha släta ytor som kan rengöras, uppfylla FDA:s krav, ge förbättrad tätning för att förhindra kontaminering och erbjuda kemisk beständighet mot rengöringsmedel och steriliseringsprocesser, med specialkonstruktioner som eliminerar sprickor där bakterier kan hysas samtidigt som den elektriska prestandan bibehålls i kritiska sjukvårdsmiljöer.
Att förstå dessa skillnader är avgörande eftersom medicinska tillämpningar har unika säkerhets- och myndighetskrav som vanliga industriella genomföringar inte kan uppfylla på ett tillfredsställande sätt.
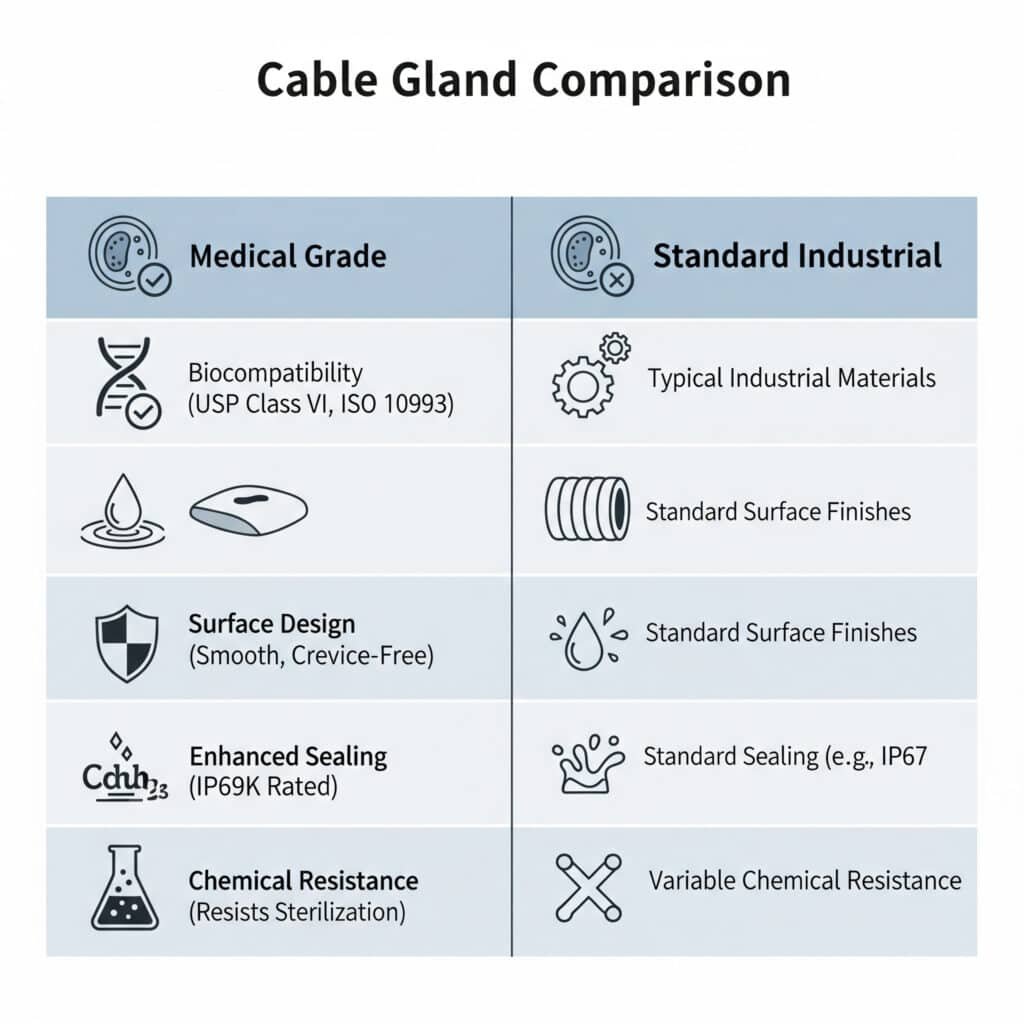
Krav på biokompatibilitet
USP klass VI Överensstämmelse: Kabelgenomföringar för medicinskt bruk måste använda material som klarar biologiska tester enligt United States Pharmacopeia Class VI för biokompatibilitet och säkerhet i medicintekniska tillämpningar.
ISO 10993-standarder: Materialen måste uppfylla ISO 109932 standarder för biologisk utvärdering av medicintekniska produkter som säkerställer att det inte finns några cytotoxiska, sensibiliserande eller irriterande effekter på mänsklig vävnad.
FDA 21 CFR 177 Godkännande: Livsmedelsgodkända material som uppfyller FDA:s regler för direkt och indirekt kontakt med livsmedel krävs ofta för farmaceutiska och medicintekniska tillämpningar.
Biokompatibla polymerer: Specialiserade material som PEEK av medicinsk kvalitet, PTFE eller nyloner av farmaceutisk kvalitet ger biokompatibilitet utan att kompromissa med de mekaniska egenskaperna.
Ytdesign för rengörbarhet
Slät ytfinish: Medicinska körtlar har extremt släta ytor med Ra-värden som normalt ligger under 0,8 mikrometer för att förhindra att bakterier fastnar och möjliggöra effektiv rengöring.
Sprickfri design: Eliminering av vassa hörn, djupa gängor och komplexa geometrier som kan hysa bakterier eller motstå rengörings- och steriliseringsprocesser.
Rundade kanter: Alla yttre ytor har rundade kanter och mjuka övergångar för att underlätta rengöring och förhindra skador på renrumshandskar eller sterila förpackningar.
Minimal ytarea: Strömlinjeformade konstruktioner minimerar den yta som utsätts för kontaminering samtidigt som nödvändiga mekaniska och elektriska prestanda bibehålls.
Förbättrad tätningsprestanda
IP68+-klassning: Överlägset miljöskydd utöver standard IP68, som ofta uppnår IP69K för rengöringsapplikationer med högt tryck och höga temperaturer.
Barriärer för kontaminering: Flera tätningssteg förhindrar inträngning av partiklar, bakterier och rengöringskemikalier som kan äventyra sterila miljöer.
Tryckbeständighet: Förbättrad tryckklassning för att klara aggressiva rengöringsprocedurer och steriliseringsprocesser utan att tätningen går sönder.
Långsiktig tillförlitlighet: Förseglingsmaterialen förblir intakta även efter upprepade steriliseringscykler och exponering för starka rengöringskemikalier.
Egenskaper för kemisk resistens
Kompatibilitet med rengöringsmedel: Motståndskraft mot desinfektionsmedel av sjukhuskvalitet, kvartära ammoniumföreningar, väteperoxid och andra aggressiva rengöringskemikalier.
Steriliseringsresistens: Materialen tål gammastrålning, etylenoxid, ångautoklavering och andra steriliseringsmetoder utan att försämras.
Farmaceutiska kemikalier: Motståndskraft mot lösningsmedel, syror, baser och farmaceutiska föreningar som är vanligt förekommande i medicinska tillverkningsmiljöer.
Temperaturstabilitet: Behåller sina egenskaper genom temperaturcykler vid sterilisering och krav på temperaturkontroll i renrum.
David, som är anläggningschef på en stor läkemedelsfabrik i New Jersey, hade återkommande problem med kontaminering i sina sterila fyllningslinjer där standardkabelförskruvningar hyste bakterier trots rigorösa rengöringsprotokoll. De befintliga mässingsförskruvningarna hade komplexa gängmönster och ytfinish som inte kunde steriliseras på ett tillfredsställande sätt, vilket ledde till att tillverkningssatser kasserades och till problem med FDA-efterlevnad. Vi specificerade rostfria kabelförskruvningar av medicinsk kvalitet med elektropolerade ytor och sprickfri design som uppfyllde USP Class VI-kraven. Uppgraderingen eliminerade kontamineringskällor, uppnådde en rengöringseffektivitet på 99,9% och hjälpte anläggningen att klara FDA-inspektioner samtidigt som antalet kasserade produkter minskade med 85%. 😊
Hur uppfyller du FDA:s och de medicintekniska föreskrifterna?
För att uppfylla FDA:s och de medicintekniska myndigheternas krav krävs att man använder material med korrekta certifieringar, upprätthåller detaljerad dokumentation och följer God tillverkningssed (GMP)3, säkerställa spårbarhet och implementera kvalitetssystem som överensstämmer med 21 CFR Part 820, med medicinska kabelgenomföringar som kräver FDA-godkända material, biokompatibilitetstestning och tillverkningskontroller som säkerställer konsekvent kvalitet och säkerhet i medicintekniska applikationer.
Regelefterlevnad är inte förhandlingsbart i medicinska applikationer eftersom fel kan leda till patientskador, produktåterkallelser och allvarliga juridiska konsekvenser.
FDA:s materialkrav
21 CFR del 177: Material som kommer i kontakt med läkemedel eller medicintekniska produkter måste uppfylla FDA:s regler för livsmedelstillsatser för ämnen som indirekt kommer i kontakt med livsmedel.
Master Access File (MAF): Leverantörer måste upprätthålla FDA Master Access Files som dokumenterar materialsäkerhet, tillverkningsprocesser och kvalitetskontrollförfaranden.
Drug Master File (DMF): För farmaceutiska tillämpningar kan material kräva Drug Master File-registrering med detaljerad information om sammansättning och tillverkning.
Intyg om överensstämmelse: Leverantörer måste tillhandahålla certifikat som bekräftar att materialen uppfyller alla tillämpliga FDA-bestämmelser och specifikationer.
Kvalitetsstandarder för medicintekniska produkter
Överensstämmelse med ISO 13485: Tillverkningen måste följa ISO 13485 kvalitetsledningssystem för medicintekniska produkter för design, produktion och övervakning efter marknadsintroduktion.
21 CFR del 820 (QSR): Efterlevnad av kvalitetssystemets regler för att säkerställa korrekta designkontroller, dokumentkontroll och korrigerande/förhindrande åtgärder.
Riskhantering: ISO 14971 riskhanteringsprocesser för medicintekniska produkter, inklusive riskanalys, utvärdering och kontrollåtgärder.
Designkontroller: Formella processer för designkontroll, inklusive designplanering, input/output-krav, granskning, verifiering och validering.

Dokumentation och spårbarhet
Materialcertifikat: Fullständig materialspårbarhet med analyscertifikat, testresultat för biokompatibilitet och dokumentation av efterlevnad av regelverk.
Tillverkningsregister: Detaljerad tillverkningsjournal med processparametrar, kvalitetskontrolltester och batchdokumentation för full spårbarhet.
Förändringskontroll: Formella rutiner för ändringskontroll för alla ändringar av material, processer eller specifikationer som påverkar efterlevnaden av regelverket.
Kvalificering av leverantör: Omfattande kvalificeringsprogram för leverantörer som säkerställer att alla material och komponenter uppfyller kraven för medicintekniska produkter.
Krav för validering
Test av biokompatibilitet: USP Class VI-testning inklusive systemiska injektions-, intrakutana och implantationstester för att verifiera biologisk säkerhet.
Validering av rengöring: Dokumenterade rengöringsrutiner med valideringsdata som bevisar effektiv borttagning av föroreningar och minskning av bioburden.
Validering av sterilisering: Validering av steriliseringsprocesser, inklusive doskartläggning, sterilitetssäkringsnivåer och studier av materialkompatibilitet.
Prestandatestning: Elektrisk, mekanisk och miljömässig testning för att verifiera att prestandan uppfyller kraven för medicintekniska produkter under hela produktens livscykel.
Stöd vid inlämnande av registreringsansökan
510(k)-dokumentation: Teknisk dokumentation som stödjer FDA 510(k)-ansökningar för medicintekniska produkter som innehåller kabelförskruvningar.
Tekniska filer: Omfattande tekniska filer för CE-märkning enligt Medical Device Regulation (MDR) på europeiska marknader.
Kvalitetsöverenskommelser: Formella kvalitetsavtal med leverantörer som definierar ansvar, specifikationer och krav på efterlevnad.
Stöd för revision: Stöd till FDA, anmälda organ och kundrevisioner, inklusive granskning av dokumentation och anläggningsinspektioner.
Vilka material krävs för renrumsapplikationer?
För renrumsapplikationer krävs material med låg avgasning, motståndskraft mot partikelgenerering, kemisk kompatibilitet med rengöringsmedel, släta icke-porösa ytor och lämpliga ledningsförmågor. Medicinskt rostfritt stål 316L, PEEK, PTFE och specialiserade renrumsgodkända polymerer ger optimal prestanda samtidigt som de uppfyller ISO 146444 renrumsstandarder och upprätthållande av elektrisk integritet i kontrollerade miljöer.
Materialvalet är avgörande eftersom renrum kräver strikt kontroll av partikel- och molekylkontaminering som kan äventyra produktkvaliteten eller de sterila förhållandena.
Krav på rostfritt stål
316L Medicinsk kvalitet: Austenitiskt rostfritt stål med låg kolhalt som ger överlägsen korrosionsbeständighet och biokompatibilitet för medicinska tillämpningar.
Elektropolerad Finish: Elektropolering avlägsnar ojämnheter i ytan, minskar partikelbildningen och skapar släta ytor för effektiv rengöring.
Passiveringsbehandling: Kemisk passivering förbättrar korrosionsbeständigheten och avlägsnar järnföroreningar som kan orsaka missfärgning eller partikelbildning.
Ytjämnhet: Ra-värden under 0,8 mikrometer (32 mikrotum) minimerar vidhäftning av bakterier och underlättar rengörings- och steriliseringsprocesser.
Högpresterande polymerer
PEEK (polyeteretereterketon): Utmärkt kemisk beständighet, låg avgasning och biokompatibilitet gör PEEK idealisk för farmaceutiska och medicintekniska tillämpningar.
PTFE (polytetrafluoretylen): Överlägsen kemisk inerthet och non-stick-egenskaper ger utmärkt motståndskraft mot rengöringskemikalier och biologiska material.
Nyloner av medicinsk kvalitet: Speciellt formulerade nyloner med USP Class VI-godkännande erbjuder goda mekaniska egenskaper med biokompatibilitet för medicinska tillämpningar.
Renrumsgodkänd POM: Polyoximetylen med låg partikelgenerering och god dimensionsstabilitet för precisionsrenrumsapplikationer.
Kompatibilitet med renrumsklassificering
ISO klass 5 (klass 100): Ultrajämna ytor med minimal partikelgenerering för halvledar- och läkemedelstillverkning.
ISO klass 6 (klass 1000): Måttlig partikelkontroll för tillverkning av medicintekniska produkter och vissa farmaceutiska processer.
ISO klass 7 (klass 10000): Standardkrav på renrum för montering av allmänna farmaceutiska och medicintekniska produkter.
ISO klass 8 (klass 100000): Grundläggande renrumskrav för förpackningar och vissa tillverkningsprocesser för medicintekniska produkter.
Kontroll av avgasning och kontaminering
Material med låg avgasning: Material med minimala utsläpp av flyktiga organiska föreningar (VOC) som kan förorena känsliga processer eller produkter.
Molekylär kontaminering: Kontroll av molekylära föroreningar, inklusive silikoner, mjukgörare och andra organiska föreningar som kan påverka produktkvaliteten.
Jonisk kontaminering: Material med låg jonhalt för att förhindra kontaminering av elektroniska komponenter och farmaceutiska produkter.
Extraherbara ämnen: Minimalt med extraherbara ämnen som kan läcka ut i läkemedelsprodukter eller rengöringslösningar under användning.
Matris för kemisk kompatibilitet
| Rengöringsmedel | 316L SS | PEEK | PTFE | Medicinsk nylon |
|---|---|---|---|---|
| Isopropylalkohol | Utmärkt | Utmärkt | Utmärkt | Bra |
| Väteperoxid | Utmärkt | Utmärkt | Utmärkt | Rättvist |
| Kvartära ammonium | Utmärkt | Utmärkt | Utmärkt | Bra |
| Natriumhypoklorit | Bra | Utmärkt | Utmärkt | Dålig |
| Perättiksyra | Bra | Utmärkt | Utmärkt | Dålig |
Hassan, som leder verksamheten vid en toppmodern läkemedelsanläggning i Schweiz, behövde uppgradera kabelförskruvningarna i sitt ISO klass 5-renrum för tillverkning av sterila injicerbara läkemedel. De befintliga kabelförskruvningarna genererade partiklar under rengöringscyklerna och klarade inte de aggressiva steriliseringsprotokoll som krävdes för de nya biologiska produkterna. Vi levererade elektropolerade kabelförskruvningar i rostfritt stål 316L med validerad låg partikelgenerering och fullständig kemisk kompatibilitet med deras rengörings- och steriliseringsprocesser. Uppgraderingen resulterade i partikelantal 90% under gränsvärdena för ISO klass 5, eliminerade rengöringsrelaterade kontamineringar och bidrog till en framgångsrik validering av den nya sterila tillverkningslinjen.
Hur säkerställer du korrekt rengöring och steriliseringskompatibilitet?
För att säkerställa korrekt rengörings- och steriliseringskompatibilitet måste man välja material som tål upprepad exponering för rengöringskemikalier och steriliseringsmetoder, utforma ytor för fullständig rengörbarhet, validera rengöringsprocedurer och upprätthålla detaljerad dokumentation, där medicinska kabelförskruvningar kräver släta, sprickfria ytor, kemikalieresistenta material och validerade rengöringsprotokoll som uppnår erforderliga sterilitetsnivåer.
Kompatibilitet mellan rengöring och sterilisering är avgörande eftersom otillräcklig dekontaminering kan leda till produktkontaminering, patientsäkerhetsrisker och överträdelser av gällande bestämmelser.
Steriliseringsmetod Kompatibilitet
Ångautoklavering: Materialen måste tåla 121°C-134°C autoklavering med ånga5 cykler utan försämring, dimensionsförändringar eller att tätningen går sönder.
Gammastrålning: Motståndskraft mot gammastrålningsdoser på 25-50 kGy som vanligen används för sterilisering av medicintekniska produkter utan att materialet försämras.
Etylenoxid (EtO): Kemisk kompatibilitet med EtO-sterilisering, inklusive resistens mot steriliseringsmedlet och korrekta avgasningsegenskaper.
Väteperoxidplasma: Kompatibilitet med lågtemperaturplasmasteriliseringssystem, inklusive materialstabilitet och fullständig penetration av steriliseringsmedel.
Krav för validering av rengöring
Rengöringsprocedurer: Dokumenterade rengöringsrutiner som anger kemikalier, koncentrationer, kontakttider och mekaniska åtgärder som krävs för effektiv dekontaminering.
Valideringsprotokoll: Formella valideringsstudier som visar rengöringseffektiviteten med hjälp av värsta tänkbara föroreningsscenarier och analytiska tester.
Kriterier för godkännande: Definierade acceptanskriterier för renhet, inklusive visuell inspektion, partikelantal, bioburden-nivåer och gränsvärden för kemiska rester.
Rutinmässig övervakning: Löpande övervakningsprogram för att verifiera fortsatt rengöringseffektivitet och identifiera eventuell försämring av prestanda.
Överväganden om ytdesign
Dräneringsfunktioner: Utforma funktioner som främjar fullständig dränering av rengöringslösningar och förhindrar ansamlingar som kan hysa föroreningar.
Tillgänglighet: Alla ytor måste vara åtkomliga för rengöring med vanliga rengöringsredskap och -metoder som används på vårdinrättningar.
Krav på demontering: Överväg om körtlarna måste demonteras för rengöring eller om intakt rengöring är tillräckligt för applikationen.
Byte av packning: Procedurer för byte och validering av packningar när tätningskomponenter kräver periodiskt byte på grund av exponering för rengöringskemikalier.
Dokumentation och efterlevnad
Rengöringsanvisningar: Detaljerade rengöringsinstruktioner med steg-för-steg-förfaranden, kemiska specifikationer och säkerhetsåtgärder.
Säkerhetsdata för material: Fullständig information om materialsäkerhet, inklusive kemisk kompatibilitet, temperaturgränser och steriliseringskompatibilitet.
Valideringsrapporter: Rengöringsvalideringsrapporter som visar effektiviteten och fastställer krav på rutinmässig övervakning.
Utbildningsmaterial: Utbildningsmaterial för vårdpersonal om korrekt rengöring, hantering och underhåll av medicinska kabelförskruvningar.
Testning av kvalitetskontroll
Testning av biobörda: Regelbundna tester för mikrobiell kontaminering för att verifiera rengöringseffektiviteten och identifiera potentiella problemområden.
Testning av endotoxin: Testning för bakteriella endotoxiner som kan orsaka pyrogena reaktioner i farmaceutiska och medicintekniska applikationer.
Partikelräkning: Test av partikelantal för att verifiera att renrumskraven uppfylls efter rengörings- och underhållsaktiviteter.
Analys av kemiska restsubstanser: Testning av rester av rengöringskemikalier som kan förorena produkter eller påverka biokompatibiliteten.
Vilka är de viktigaste urvalskriterierna för olika medicinska tillämpningar?
De viktigaste urvalskriterierna varierar beroende på applikation, men omfattar krav på regelefterlevnad, biokompatibilitetsnivåer, renrumsklassificeringar, steriliseringsmetoder, kemisk exponering och behov av elektrisk prestanda, där kirurgisk utrustning kräver högsta biokompatibilitet, läkemedelstillverkning kräver kemisk resistens och diagnostisk utrustning fokuserar på elektrisk integritet, medan alla applikationer kräver lämpliga regulatoriska certifieringar och rengöringskompatibilitet.
Olika medicinska tillämpningar har unika krav som måste beaktas noga vid valet av kabelförskruvning för att säkerställa optimal prestanda och efterlevnad av regelverk.
Kirurgisk utrustning och utrustning för patientkontakt
Krav på direktkontakt: USP Class VI biokompatibilitet med ytterligare cytotoxicitetstest för material i direkt patientkontakt under kirurgiska ingrepp.
Steriliseringsfrekvens: Förmåga att motstå frekventa steriliseringscykler utan försämring, vilket normalt kräver material som är stabila i hundratals steriliseringscykler.
Elektrisk säkerhet: Förbättrade krav på elsäkerhet, inklusive låg läckström och tillförlitlig isolering för patientansluten utrustning.
Tillförlitlighet i nödsituationer: Kritiska tillförlitlighetskrav för livsuppehållande och akutmedicinsk utrustning där fel direkt kan påverka patientsäkerheten.
Läkemedelstillverkning
GMP-överensstämmelse: Krav på god tillverkningssed, inklusive spårbarhet för material, ändringskontroll och valideringsdokumentation.
Säkerhet vid produktkontakt: Material som inte kontaminerar läkemedelsprodukter genom urlakning, partikelgenerering eller kemisk interaktion.
Validering av rengöring: Omfattande valideringskrav för rengöring med dokumenterade procedurer och acceptanskriterier för läkemedelstillverkning.
Batchdokumentation: Fullständig batchdokumentation och spårbarhet för material som används i utrustning för läkemedelstillverkning.
Diagnostik- och laboratorieutrustning
Krav på precision: Dimensionsstabilitet och precision för analysinstrument som kräver konsekvent mekanisk och elektrisk prestanda.
Kemisk beständighet: Beständighet mot laboratoriekemikalier, reagenser och rengöringsmedel som vanligen används i diagnostiska tillämpningar.
EMC Prestanda: Krav på elektromagnetisk kompatibilitet för känsliga analysinstrument och diagnostisk utrustning.
Stabilitet i kalibreringen: Mekanisk stabilitet som inte påverkar instrumentkalibrering eller mätnoggrannhet över tid.
Tillverkning av medicintekniska produkter
Validering av processer: Material och komponenter som stöder processvalideringskrav för tillverkning av medicintekniska produkter.
Kvalitetssystem: Integration med ISO 13485 kvalitetssystem inklusive leverantörskvalificering och rutiner för inkommande inspektion.
Riskhantering: Material som stöder kraven på riskhantering för medicintekniska produkter, inklusive analys av felsituationer och strategier för att minska riskerna.
Stöd i regleringsfrågor: Leverantörsstöd för regulatoriska ansökningar, inklusive teknisk dokumentation och regulatorisk expertis.
Beslutsmatris för urval
| Tillämpningstyp | Primära kriterier | Sekundära kriterier | Kritiska standarder |
|---|---|---|---|
| Kirurgisk utrustning | Biokompatibilitet | Sterilisering | USP klass VI, ISO 10993 |
| Läkemedel | Kemisk beständighet | GMP-överensstämmelse | FDA 21 CFR, cGMP |
| Diagnostik | Precision | EMC-prestanda | IEC 61326, ISO 15189 |
| Tillverkning | Validering av processer | Kvalitetssystem | ISO 13485, 21 CFR 820 |
Kostnads- och nyttoanalys
Initialkostnad kontra livscykel: Beakta den totala ägandekostnaden, inklusive kostnader för underhåll, utbyte och efterlevnad under utrustningens livslängd.
Regleringsrisk: Balansera materialkostnader mot risker för bristande regelefterlevnad och potentiella kostnader för bristande regelefterlevnad.
Krav på prestanda: Säkerställ att valda material uppfyller minimikraven på prestanda utan att överspecificeras vilket ökar kostnaderna i onödan.
Leverantörens kapacitet: Utvärdera leverantörernas kapacitet för löpande support, dokumentation och hjälp med efterlevnad av regelverk.
Slutsats
För att välja kabelförskruvningar för medicinsk utrustning och renrum måste man förstå de unika krav på regelverk, material och prestanda som skiljer dessa tillämpningar från vanliga industriella tillämpningar. För att lyckas måste man hitta en balans mellan biokompatibilitet, rengörbarhet, regelefterlevnad och elektrisk prestanda.
Nyckeln till tillförlitliga medicinska kabelförskruvningar ligger i att arbeta med leverantörer som förstår reglerna för medicintekniska produkter och kan tillhandahålla lämpliga material, dokumentation och löpande support under hela produktlivscykeln. På Bepto är vi specialiserade på kabelförskruvningar av medicinsk kvalitet som uppfyller FDA-krav och internationella standarder för medicintekniska produkter, vilket ger den kvalitetssäkring och det regulatoriska stöd som behövs för kritiska sjukvårdsapplikationer.
Vanliga frågor om medicinska kabelgenomföringar
F: Vilka certifieringar behöver jag för medicinska kabelförskruvningar?
A: Kabelgenomföringar för medicinskt bruk kräver vanligtvis USP Class VI-certifiering för biokompatibilitet, FDA 21 CFR-efterlevnad för material och ISO 13485-kvalitetssystem för tillverkning. Specifika krav beror på din applikation och myndigheternas jurisdiktion.
F: Kan vanliga kabelförskruvningar i rostfritt stål användas i medicinska tillämpningar?
A: Vanligt rostfritt stål kanske inte uppfyller de medicinska kraven. Medicinska tillämpningar kräver 316L medicinskt rostfritt stål med elektropolerad yta, biokompatibilitetstestning och korrekt dokumentation för att uppfylla kraven i lagstiftningen.
F: Hur rengör och steriliserar jag medicinska kabelförskruvningar?
A: Följ tillverkarens validerade rengöringsprocedurer med godkända rengöringsmedel och steriliseringsmetoder. De flesta medicinska körtlar klarar ångautoklavering, gammastrålning eller kemisk sterilisering med rätt materialkompatibilitet.
F: Vad är skillnaden mellan kabelförskruvningar för renrum och för medicinskt bruk?
A: Medicinsk kvalitet omfattar krav på biokompatibilitet och FDA-överensstämmelse medan renrumskvalitet fokuserar på partikelkontroll och kemisk beständighet. Vissa applikationer kräver både medicinska specifikationer och renrumsspecifikationer.
Q: Hur ofta bör medicinska kabelgenomföringar bytas ut?
A: Utbytesfrekvensen beror på steriliseringscykler, kemisk exponering och tillverkarens rekommendationer. Inspektera vanligen efter 100-200 steriliseringscykler och byt ut dem baserat på tillståndsbedömning och valideringskrav.
-
Läs mer om de specifika biologiska reaktivitetstester som krävs för USP Class VI-certifiering. ↩
-
Få en översikt över ISO 10993-serien med standarder för biologisk utvärdering av medicintekniska produkter. ↩
-
Granska FDA:s officiella riktlinjer och föreskrifter för Current Good Manufacturing Practices (cGMP). ↩
-
Utforska en detaljerad guide till ISO 14644-standarderna för klassificering av luftrenhet i renrum. ↩
-
Förstå principerna för ångsterilisering, inklusive betydelsen av tid, temperatur och tryck. ↩



