Napake pri sterilizaciji medicinskih pripomočkov proizvajalce letno stanejo milijone, pri čemer je 15-20% napak posledica neustreznega zračenja, ki preprečuje ustrezno penetracijo sterilizacijskega sredstva. Standardni ventilacijski čepi odpovedo pod avtoklav1 pri temperaturah 121-134 °C ali se razgradijo, če so izpostavljeni sterilizacija z etilenoksidom (ETO)2 kemikalij, kar ogroža zagotavljanje sterilnosti in skladnost s predpisi.
Sterilizacijski ventilacijski čepi omogočajo učinkovito sterilizacijo, saj omogočajo prodor pare ali plina ETO, hkrati pa ohranjajo sterilne ovire po sterilizaciji. Odprtine z membrano iz PTFE vzdržijo temperature avtoklava do 150 °C in so odporne na kemično razgradnjo ETO, kar zagotavlja zanesljivo vzdrževanje sterilnosti medicinskih pripomočkov, farmacevtske opreme in laboratorijskih instrumentov, za katere so potrebni potrjeni postopki sterilizacije.
Lani sem sodeloval z Dr. Sarah Mitchell, direktorico za kakovost pri vodilnem proizvajalcu medicinskih pripomočkov v Bostonu, ki se je soočal z napakami pri validaciji sterilizacije na embalaži pripomočkov za vsaditev. Njihovi standardni najlonski ventilacijski čepi so se med cikli avtoklava topili in preprečevali pravilno prodiranje pare. Po prehodu na naše sterilizacijske zamaške iz farmacevtskega PTFE s potrjeno temperaturno odpornostjo so dosegli učinkovitost sterilizacije 100% v 1 000 validacijskih ciklih - zagotovili so skladnost s predpisi FDA in varnost pacientov! 🏥
Kazalo vsebine
- Kaj so sterilizirani zračniki in zakaj so ključnega pomena?
- Kako različne metode sterilizacije vplivajo na materiale z zračnimi čepi?
- Kateri materiali so najboljši za sterilizacijo v avtoklavu?
- Kateri materiali so najboljši za postopke sterilizacije ETO?
- Kako izbrati in potrditi sterilizabilne prezračevalne čepke?
- Pogosta vprašanja o sterilizabilnih zamaških za prezračevanje
Kaj so sterilizirani zračniki in zakaj so ključnega pomena?
Razumevanje vloge sterilizabilnih ventilacijskih čepov v proizvodnji medicinskih pripomočkov in farmacevtskih izdelkov je bistvenega pomena za zagotavljanje sterilnosti in skladnosti z zakonodajo.
Sterilizacijski ventilacijski čepi so specializirani ventilacijski čepi, ki dihajo in so zasnovani tako, da prenesejo postopke sterilizacije, hkrati pa omogočajo prodiranje sterilnih sredstev in ohranjajo sterilne pregrade. Omogočajo izpodrivanje zraka med sterilizacijo, preprečujejo nastanek vakuuma med hlajenjem in ohranjajo sterilne pogoje po sterilizaciji. Kritične aplikacije vključujejo embalažo za medicinske pripomočke, farmacevtske posode, laboratorijsko opremo in opremo za sterilno obdelavo.
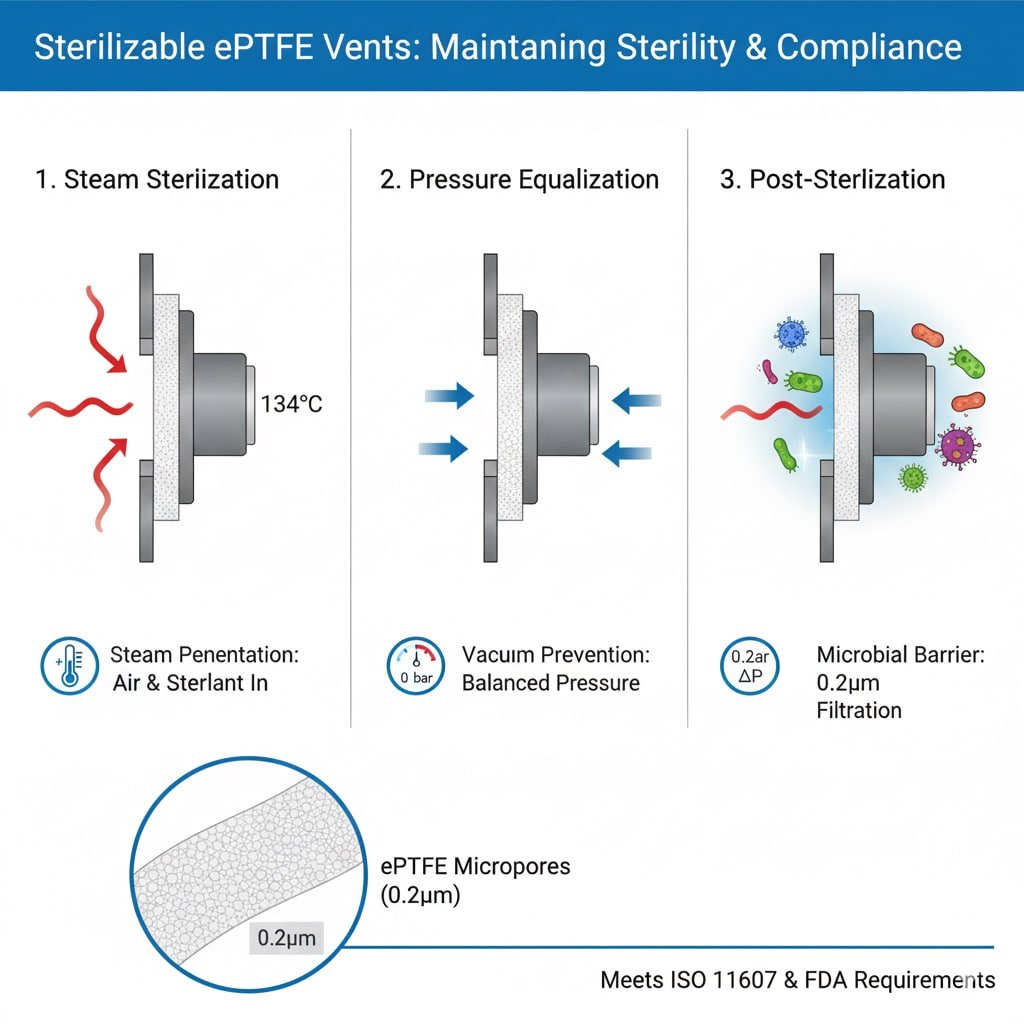
Zahteve za postopek sterilizacije
Penetracija pare: Pri sterilizaciji v avtoklavu mora para prodreti v embalažo in priti v stik z vsemi površinami, zato so potrebni zračniki, ki omogočajo pretok plina in hkrati ohranjajo mikrobne ovire.
Prostornina zraka: Učinkovita sterilizacija zahteva popolno odstranitev zraka in zamenjavo s sterilnim sredstvom, kar prezračevalniki omogočajo z nadzorovano izmenjavo plinov.
Izenačevanje tlaka: Sterilizacijski cikli ustvarjajo tlačne razlike, ki jih morajo prezračevalne odprtine prilagoditi, ne da bi pri tem ogrozili sterilne pregrade ali celovitost embalaže.
Kritični parametri delovanja
Temperaturna odpornost: Odprtine za sterilizacijo morajo pri temperaturah sterilizacije od 121 °C do 150 °C ohraniti strukturno celovitost in učinkovitost filtriranja.
Kemijska združljivost: Materiali morajo biti odporni na razgradnjo zaradi kemikalij za sterilizacijo, vključno s paro, etilenoksidom, vodikovim peroksidom in ozonom.
Učinkovitost mikrobioloških pregrad: Po sterilizaciji morajo zračniki zagotavljati zanesljivo mikrobna pregrada3 z velikostjo por običajno 0,2-0,22 mikrona za zadrževanje bakterij.
Upoštevanje skladnosti s predpisi
Zahteve FDA za validacijo: Za uporabo medicinskih pripomočkov so potrebni potrjeni postopki sterilizacije z dokumentiranim delovanjem prezračevalnika v vseh sterilizacijskih ciklih.
Skladnost s standardi ISO: Odprtine za sterilizacijo morajo ustrezati ISO 116074 standarde pakiranja in zahteve za parno sterilizacijo po standardu ISO 17665 za medicinske aplikacije.
Testiranje biokompatibilnosti: Pri aplikacijah za stik z medicinskimi pripomočki se lahko zahteva testiranje biokompatibilnosti razreda VI USP za zagotavljanje varnosti bolnikov.
Kategorije aplikacij
Pakiranje medicinskih pripomočkov: Sterilna embalaža za vsadke, kirurške instrumente in medicinske pripomočke za enkratno uporabo, ki zahtevajo ohranjanje sterilnosti do uporabe.
Farmacevtska proizvodnja: Sterilna obdelovalna oprema, bioreaktorji in farmacevtske posode, ki zahtevajo validirane postopke sterilizacije.
Laboratorijska oprema: Laboratorijske posode za avtoklaviranje, posode za kulture in analitična oprema, ki zahteva sterilne pogoje za točne rezultate.
Kako različne metode sterilizacije vplivajo na materiale z zračnimi čepi?
Različne metode sterilizacije predstavljajo edinstvene izzive za materiale, iz katerih so narejeni ventilacijski čepi, za optimalno delovanje pa so potrebne posebne lastnosti materialov in oblikovni vidiki.
Pri parni sterilizaciji so materiali izpostavljeni visokim temperaturam (121-134 °C) in nasičeni pari, kar lahko povzroči toplotno degradacijo, spremembe dimenzij in poškodbe membrane. Pri sterilizaciji ETO so materiali izpostavljeni reaktivnim kemikalijam pri nižjih temperaturah (37-63 °C), vendar daljšem času izpostavljenosti, kar lahko povzroči kemično razgradnjo in izpuščanje plinov. Vsaka metoda zahteva posebno izbiro materiala za zanesljivo delovanje.
Učinki sterilizacije s paro
Toplotni stres: Visoke temperature povzročajo toplotno raztezanje, morebitno taljenje termoplastičnih komponent in razgradnjo materialov, občutljivih na temperaturo.
Reakcije hidrolize5: Izpostavljenost pari lahko povzroči hidrolitsko razgradnjo nekaterih polimerov, zlasti poliestra in nekaterih poliamidov.
Dimenzijska stabilnost: Ponavljajoče se toplotno cikliranje lahko povzroči dimenzijske spremembe, ki vplivajo na učinkovitost tesnjenja in filtriranja.
Izzivi pri sterilizaciji ETO
Kemijska reaktivnost: Etilen oksid reagira z materiali, ki vsebujejo atome aktivnega vodika, kar lahko spremeni lastnosti materialov in povzroči nastanek strupenih ostankov.
Zahteve glede izpuščanja: Za izdelke, sterilizirane z ETO, je treba pred varno uporabo podaljšati obdobje zračenja, da se odstranijo absorbirani ETO in reakcijski produkti.
Značilnosti penetracije: ETO za učinkovito penetracijo zahteva posebne pogoje vlažnosti in temperature, kar vpliva na zahteve glede zasnove prezračevalnika.
Učinki plazme vodikovega peroksida
Oksidativna razgradnja: Plazma H2O2 ustvarja zelo reaktivne vrste, ki lahko z oksidacijskimi reakcijami razgradijo organske snovi.
Združljivost materialov: Številni elastomeri in nekatere plastične mase so zaradi hitre razgradnje nezdružljivi s plazemsko sterilizacijo s H2O2.
Prednosti pri nizkih temperaturah: Plazemska sterilizacija poteka pri nizkih temperaturah (45-55 °C), kar zmanjšuje toplotno obremenitev materialov, občutljivih na temperaturo.
Upoštevanje sevanja gama
Poškodbe zaradi sevanja: Visokoenergijsko sevanje gama lahko povzroči cepitev polimerne verige ali zamreženje, kar bistveno spremeni lastnosti materiala.
Akumulacija odmerka: Ponavljajoča se gama sterilizacija lahko povzroči kumulativne poškodbe, kar omejuje število sterilizacijskih ciklov, ki jih materiali lahko prenesejo.
Potrebe po antioksidantih: Formulacije, odporne na sevanje, pogosto potrebujejo antioksidante za preprečevanje oksidativne razgradnje med obsevanjem in po njem.
Nedavno sem Ahmedu Al-Rashidu, vodji operacij v farmacevtskem obratu v Dubaju, pomagal rešiti težave s sterilizacijo ETO s sistemi za odzračevanje bioreaktorjev. Njihovi standardni ventilacijski čepi so absorbirali ETO in zahtevali daljša 14-dnevna obdobja zračenja, kar je motilo proizvodne urnike. Z uvedbo naših z ETO združljivih zračilnih čepov iz PTFE z minimalnimi absorpcijskimi lastnostmi so skrajšali čas prezračevanja na 24 ur, pri čemer so ohranili popolno zagotavljanje sterilnosti - kar je bistveno izboljšalo učinkovitost proizvodnje! 🚀
Kateri materiali so najboljši za sterilizacijo v avtoklavu?
Za izbiro ustreznih materialov za sterilizacijo v avtoklavu je treba razumeti toplotno stabilnost, odpornost na hidrolizo in dolgoročno delovanje pri večkratni izpostavljenosti pari.
PTFE (politetrafluoretilen) zagotavlja vrhunsko delovanje v avtoklavu z neprekinjenim delovanjem pri temperaturah do 260 °C, odlično kemično inertnost in odpornost proti hidrolizi. PVDF (poliviniliden fluorid) zagotavlja dobro toplotno stabilnost do 150 °C in nižjo ceno. Izogibajte se najlonu, standardnemu polietilenu in večini elastomerov, ki se v pogojih avtoklava razgradijo, kar poslabša učinkovitost filtriranja in tesnjenja.
Prednosti PTFE membrane
Izjemna temperaturna odpornost: PTFE ohranja strukturno celovitost in učinkovitost filtracije pri temperaturah, ki so precej višje od običajnih pogojev v avtoklavu (121-134 °C).
Kemična inertnost: PTFE je odporen na razgradnjo zaradi pare, kemikalij za čiščenje in stranskih produktov sterilizacije, kar zagotavlja stalno dolgoročno delovanje.
Hidrofobne lastnosti: Hidrofobna narava PTFE preprečuje vpijanje vode in ohranja dimenzijsko stabilnost v vseh sterilizacijskih ciklih.
Primerjava učinkovitosti materialov
| Material | Najvišja temperatura (°C) | Odpornost na paro | Odpornost na hidrolizo | Stroškovni dejavnik |
|---|---|---|---|---|
| PTFE | 260 | Odlično | Odlično | Visoka |
| PVDF | 150 | Dobro | Dobro | Srednja |
| PP (polipropilen) | 135 | Fair | Fair | Nizka |
| Najlon | 80-100 | Slaba | Slaba | Nizka |
Izbira materiala ohišja
Iz nerjavečega jekla 316L: Zagotavlja odlično korozijsko odpornost, toplotno stabilnost in čistljivost za farmacevtske in medicinske aplikacije, ki zahtevajo potrjene postopke čiščenja.
PEEK (polieterski eteroketon): Ponuja izjemno toplotno stabilnost (neprekinjena uporaba do 250 °C) z odlično kemično odpornostjo za zahtevne aplikacije v avtoklavu.
Polipropilen: Cenovno učinkovita možnost za aplikacije za enkratno uporabo z ustrezno zmogljivostjo za standardne cikle avtoklava pri 121 °C.
Upoštevanje komponent za tesnjenje
O-obročki iz EPDM: Zagotavljajo dobro odpornost na paro in toplotno stabilnost pri temperaturah do 150 °C ter odlično tesnilno zmogljivost.
Silikonska tesnila: Ponujajo visoko temperaturno odpornost (do 200 °C), vendar imajo lahko težave z združljivostjo z nekaterimi kemikalijami za čiščenje.
O-obročki s PTFE ohišjem: Kombinacija kemične odpornosti PTFE in tesnilnih lastnosti elastomera za zahtevne aplikacije, ki zahtevajo obe lastnosti.
Optimizacija zasnove za uporabo avtoklava
Toplotna razteznost Namestitev: Zasnove zračnikov morajo upoštevati diferencialno toplotno raztezanje med materiali, da se prepreči okvara tesnila med temperaturnimi cikli.
Značilnosti odvodnjavanja: Ustrezna zasnova odvodnjavanja preprečuje kopičenje kondenzata, ki bi lahko ogrozilo učinkovitost filtriranja ali povzročilo nevarnost onesnaženja.
Podpora za potrjevanje: Značilnosti zasnove morajo olajšati validacijsko preskušanje, vključno z razpadom tlaka, mikrobnim izzivom in preverjanjem toplotne učinkovitosti.
Kateri materiali so najboljši za postopke sterilizacije ETO?
Sterilizacija ETO predstavlja edinstvene izzive za materiale, ki za učinkovito obdelavo zahtevajo kemijsko združljivost, minimalno absorpcijo in hitre lastnosti izpuščanja plinov.
PTFE in PVDF zagotavljata odlično združljivost z ETO z minimalno absorpcijo kemikalij in hitrim izpuščanjem plinov. Izogibajte se materialom z aktivnimi vodikovimi mesti, kot so najlon, PVC in naravni kavčuk, ki reagirajo z ETO in tvorijo strupene spojine. Ohišja iz nerjavnega jekla zagotavljajo optimalno kemijsko odpornost, silikonska tesnila pa dobro združljivost z ETO s sprejemljivimi lastnostmi izpuščanja za večino aplikacij.
Kemijska združljivost ETO
Reakcijski mehanizmi: ETO reagira z materiali, ki vsebujejo hidroksilne, amino, karboksilne in sulfhidrilne skupine, pri čemer nastanejo derivati etilen glikola in druge potencialno strupene spojine.
Značilnosti absorpcije: Materiali z visoko absorpcijo ETO potrebujejo daljša obdobja zračenja, kar znatno podaljša čas obdelave in stroške.
Kinetika izpuščanja: Materiali s hitrim izpuščanjem omogočajo krajše cikle prezračevanja, kar izboljša učinkovitost procesa in skrajša čas skladiščenja zalog.
Razvrstitev uspešnosti materiala ETO
Odlična združljivost z ETO:
- PTFE: Minimalna absorpcija, hitro izpuščanje, brez kemične reaktivnosti
- PVDF: Nizka absorpcija, dobro izpuščanje, odlična kemijska odpornost
- Iz nerjavečega jekla: Ne absorbira se, možnost takojšnje uporabe
Dobra združljivost z ETO:
- Polipropilen: Zmerna absorpcija, sprejemljivo izpuščanje plinov
- Silikon: Nizka reaktivnost, zmerne zahteve glede izpuščanja plinov
Slaba združljivost ETO:
- Najlon: Visoka reaktivnost, potrebno daljše zračenje
- PVC: kemična razgradnja, nastajanje strupenih spojin
- Naravni kavčuk: visoka absorpcija, možna razgradnja
Časovne zahteve za zračenje
| Material | Običajni čas zračenja | Stopnja absorpcije ETO | Stopnja izpuščanja |
|---|---|---|---|
| PTFE | 8-24 ur | Minimalno | Hitro |
| PVDF | 24-48 ur | Nizka | Dobro |
| Polipropilen | 48-72 ur | Zmerno | Zmerno |
| Najlon | 7-14 dni | Visoka | Počasi |
Optimizacija parametrov procesa
Nadzor temperature: Sterilizacija ETO običajno poteka pri 37-63 °C, zato so potrebni materiali, ki ohranjajo učinkovitost v tem temperaturnem območju.
Zahteve glede vlažnosti: Za učinkovitost ETO je potrebna relativna vlažnost 40-80%, zato so potrebni materiali, ki so v teh pogojih vlage dosledno učinkoviti.
Upravljanje koncentracije plina: Koncentracije ETO 450-1200 mg/L zahtevajo materiale, ki so odporni na kemične napade in hkrati omogočajo prodiranje sterilizacijskega sredstva.
Razmisleki o potrjevanju
Testiranje ostankov: Pri izdelkih, steriliziranih z ETO, je treba opraviti testiranje na ostanke ETO in reakcijske produkte, da se zagotovi skladnost z varnostnimi mejami.
Vzdrževanje biokompatibilnosti: Materiali morajo ohraniti biokompatibilnost po izpostavljenosti ETO in zračenju, kar zahteva potrjeno izbiro materiala.
Spremljanje procesov: Sterilizacija ETO zahteva neprekinjeno spremljanje temperature, vlažnosti, tlaka in koncentracije plina med celotnim ciklom.
Kako izbrati in potrditi sterilizabilne prezračevalne čepke?
Pravilna izbira in potrditev sterilizabilnih ventilacijskih čepov zagotavljata zanesljivo sterilizacijo, skladnost s predpisi in dolgoročno uspešnost delovanja.
Pri izbiri je treba uskladiti lastnosti materiala z metodo sterilizacije, opredeliti zahteve glede zmogljivosti in upoštevati regulativne standarde. Validacija vključuje testiranje toplotne učinkovitosti, študije mikrobnih izzivov, oceno kemijske združljivosti in oceno dolgoročne stabilnosti. Dokumentirajte vsa testiranja v skladu s standardi FDA in ISO za regulativno predložitev in skladnost sistema kakovosti.
Okvir meril za izbor
Združljivost metode sterilizacije: Prilagodite materiale za prezračevanje posebnim metodam sterilizacije (para, ETO, plazma H2O2, gama) na podlagi zahtev glede temperature, kemične odpornosti in odpornosti na sevanje.
Specifikacije delovanja: Na podlagi zahtev uporabe določite zahtevane hitrosti pretoka, tlačne vrednosti, učinkovitost filtriranja in lastnosti mikrobioloških pregrad.
Regulativne zahteve: Upoštevajte razvrstitev pripomočkov FDA, skladnost s standardi ISO in zahteve glede biokompatibilnosti za predvideno uporabo.
Parametri ocenjevanja vlog
Delovno okolje: Ocenite temperaturna območja, izpostavljenost kemikalijam, tlačne razmere in tveganja onesnaženja v celotnem življenjskem ciklu izdelka.
Pogostost sterilizacije: Upoštevajte enkratno uporabo v primerjavi z več sterilizacijskimi cikli in kumulativne učinke na zmogljivost in zanesljivost materiala.
Področje validacije: Določite zahteve za preskušanje na podlagi ocene tveganja, regulativne poti in zahtev sistema kakovosti.
Protokol validacijskega preskušanja
Testiranje toplotne učinkovitosti:
- Ciklično spreminjanje temperature pri pogojih sterilizacije
- Merjenje dimenzijske stabilnosti
- Preverjanje učinkovitosti filtriranja po termični izpostavljenosti
Testiranje mikrobnih izzivov:
- Bakterijski izziv z ustreznimi testnimi organizmi
- Preverjanje vzdrževanja sterilnosti
- Dolgoročna ocena celovitosti pregrade
Ocena kemijske združljivosti:
- Vrednotenje degradacije materiala
- Testiranje ekstraktivnih in izluženih snovi
- Preverjanje vzdrževanja biokompatibilnosti
Zahteve glede dokumentacije
Specifikacije materiala: Popolni podatkovni listi materialov, vključno s kemijsko sestavo, toplotnimi lastnostmi in regulativnimi certifikati.
Preskusni protokoli: Podrobni validacijski protokoli v skladu s smernicami FDA in standardi ISO za validacijo sterilizacije.
Podatki o uspešnosti: Izčrpni rezultati preskusov, ki dokazujejo delovanje v določenih pogojih delovanja in sterilizacijskih ciklih.
Integracija sistema kakovosti
Kvalifikacija dobavitelja: Vzpostavite sporazume o kakovosti z dobavitelji, vključno s sledljivostjo materiala, nadzorom sprememb in zahtevami glede dokumentacije kakovosti.
Prihodnji inšpekcijski pregled: Razvijte postopke za preverjanje kritičnih dimenzij, lastnosti materiala in značilnosti delovanja.
Validacija procesa: Vključite delovanje prezračevalnika v celotno validacijo postopka sterilizacije, vključno s testiranjem najslabšega možnega scenarija.
Razmisleki o upravljanju tveganj
Analiza načina odpovedi: Opredelite možne načine okvar, vključno z degradacijo materiala, okvaro tesnila in ogrožanjem filtracije z ustreznimi strategijami za ublažitev.
Nadzor sprememb: Vzpostavite postopke za upravljanje sprememb materiala, sprememb dobaviteljev in sprememb specifikacij z ustreznimi zahtevami za ponovno potrditev.
Neprekinjeno spremljanje: izvajajte programe stalnega spremljanja, da preverite neprekinjeno delovanje in odkrijete morebitne težave, preden vplivajo na kakovost izdelka.
Zaključek
Sterilizabilni ventilacijski čepi imajo ključno vlogo pri zagotavljanju učinkovite sterilizacije in ohranjanju sterilnih pregrad v medicinskih pripomočkih in farmacevtskih aplikacijah. Razumevanje edinstvenih izzivov različnih metod sterilizacije in izbira ustreznih materialov sta bistvena za zanesljivo delovanje in skladnost z zakonodajo.
Ventilacijski čepi na osnovi PTFE zagotavljajo vrhunsko zmogljivost pri različnih metodah sterilizacije, odlično temperaturno odpornost, kemijsko združljivost in dolgoročno zanesljivost. Pravilna izbira in potrditev zagotavljata optimalno učinkovitost sterilizacije, hkrati pa zmanjšujeta čas obdelave in stroške.
V podjetju Bepto naša celovita ponudba sterilizabilnih ventilacijskih čepov vključuje membrane PTFE farmacevtske kakovosti, potrjeno temperaturno učinkovitost in popolne pakete dokumentacije za regulativne prijave. Z več kot desetletjem izkušenj na področju specializiranih aplikacij za odzračevanje in proizvodnimi zmogljivostmi s certifikatom ISO zagotavljamo zanesljive in stroškovno učinkovite rešitve, ki jih potrebujete za kritične aplikacije sterilizacije. Zaupajte nam, da bodo vaši postopki sterilizacije potrjeni, vaši izdelki pa varni! 🔬
Pogosta vprašanja o sterilizabilnih zamaških za prezračevanje
V: Ali se lahko isti odzračevalni čep uporablja tako za sterilizacijo v avtoklavu kot za sterilizacijo ETO?
A: Da, membranski ventilacijski čepi iz PTFE lahko učinkovito opravijo sterilizacijo v avtoklavu in ETO. PTFE zagotavlja odlično temperaturno odpornost za cikle avtoklava in minimalno absorpcijo ETO za hitro zračenje, zato je idealen za ustanove, ki uporabljajo več metod sterilizacije.
V: Koliko sterilizacijskih ciklov lahko zdrži prezračevalni čep?
A: Visokokakovostni ventilacijski čepi iz PTFE običajno zdržijo več kot 100 ciklov avtoklava ali več kot 50 ciklov ETO, pri čemer ohranijo učinkovitost filtriranja. Dejanska življenjska doba ciklov je odvisna od parametrov sterilizacije, postopkov ravnanja in meril za sprejemljivost delovanja za vašo posebno uporabo.
V: Kakšna velikost por je potrebna za sterilno filtracijo v medicini?
A: V medicinskih aplikacijah se za zanesljivo zadrževanje bakterij običajno zahtevajo pore velikosti 0,2 ali 0,22 mikrona. Ta velikost por zagotavlja potrjeno zagotavljanje sterilnosti, hkrati pa omogoča ustrezen pretok plina za učinkovito sterilizacijo in izenačevanje tlaka.
V: Ali je za sterilizabilne prezračevalne čepke potrebno posebno validacijsko testiranje?
A: Da, za sterilizabilne ventilacijske čepke je treba opraviti validacijsko testiranje, vključno s študijami toplotne učinkovitosti, mikrobioloških izzivov in združljivosti materialov. Testiranje mora potekati v skladu s smernicami FDA in standardi ISO, dokumentacija pa mora podpirati validacijo vašega sterilizacijskega postopka in predložitev regulativnim organom.
V: Kako med sterilizacijo preprečite kontaminacijo z zračnim čepom?
A: Kontaminacijo preprečite s pravilno namestitvijo, zaščitnimi pokrovi med rokovanjem, potrjenimi parametri sterilizacije in ustreznim shranjevanjem po sterilizaciji. Med namestitvijo uporabljajte sterilno tehniko in poskrbite, da so prezračevalni čepi zasnovani za vašo specifično metodo sterilizacije in zahteve za uporabo.
-
Spoznajte znanstvena načela sterilizacije v avtoklavu in način uporabe nasičene pare pod pritiskom za učinkovito uničevanje mikroorganizmov. ↩
-
Spoznajte kemični postopek sterilizacije z etilenoksidom (ETO), nizkotemperaturno metodo, ki se uporablja za sterilizacijo medicinskih pripomočkov, občutljivih na toploto in vlago. ↩
-
Spoznajte metode, ki se uporabljajo za preskušanje in potrjevanje učinkovitosti mikrobne pregrade, ki preprečuje vdor mikroorganizmov in ohranja sterilnost. ↩
-
Preglejte ključne zahteve standarda ISO 11607, ki določa materiale in preskušanje sterilnih pregradnih sistemov za medicinske pripomočke. ↩
-
Razumevanje kemijske reakcije hidrolize in kako lahko povzroči razgradnjo nekaterih polimernih materialov, če so izpostavljeni vodi ali pari pri visokih temperaturah. ↩



