Neustrezna izbira kabelskih žlez v medicinskih okoljih in čistih prostorih povzroča tveganja onesnaženja, neskladnost s predpisi in okvare opreme, ki ogrožajo varnost bolnikov, povzročajo drage zaustavitve obratov in kršitve FDA, medtem ko neustrezno tesnjenje, neustrezni materiali in slaba čistost povzročajo rast bakterij, onesnaženje z delci in kršitve sterilnosti, ki ogrožajo kritične zdravstvene dejavnosti. Številni vodje objektov se spopadajo z izbiro žlez, ki izpolnjujejo stroge medicinske standarde in hkrati ohranjajo zanesljivo električno delovanje.
Pri izbiri kabelskih ovojev za medicinsko opremo in čiste prostore je treba poznati predpise FDA, USP razred VI1 zahteve glede materialov, standarde tesnjenja IP68+ in potrebe po razvrstitvi v čiste prostore, pri čemer konstrukcija iz medicinskega nerjavnega jekla ali specializiranih polimerov zagotavlja biokompatibilnost, kemično odpornost in gladke površine za učinkovito čiščenje in sterilizacijo, hkrati pa ohranja električno celovitost v kritičnih aplikacijah v zdravstvu. Uspeh je odvisen od usklajevanja skladnosti z zakonodajo in zanesljivosti delovanja.
Pri delu z bolnišničnimi inženirji v večjih medicinskih centrih v Bostonu, farmacevtskimi proizvajalci v Švici in čistimi prostori v Singapurju sem spoznal, da so medicinska kabelska žrela bistvenega pomena za ohranjanje sterilnega okolja in zagotavljanje varnosti pacientov. Naj z vami delim ključno znanje za izbiro optimalnih kabelskih ovojnic za vaše aplikacije v medicini in čistih prostorih.
Kazalo vsebine
- Po čem se medicinska kabelska vtičnika razlikujejo od standardnih vtičnikov?
- Kako izpolnjujete predpise FDA in medicinske pripomočke?
- Kateri materiali so potrebni za uporabo v čistih prostorih?
- Kako zagotoviti ustrezno združljivost čiščenja in sterilizacije?
- Katera so ključna merila za izbiro različnih medicinskih aplikacij?
- Pogosta vprašanja o medicinskih kabelskih žicah
Po čem se medicinska kabelska vtičnika razlikujejo od standardnih vtičnikov?
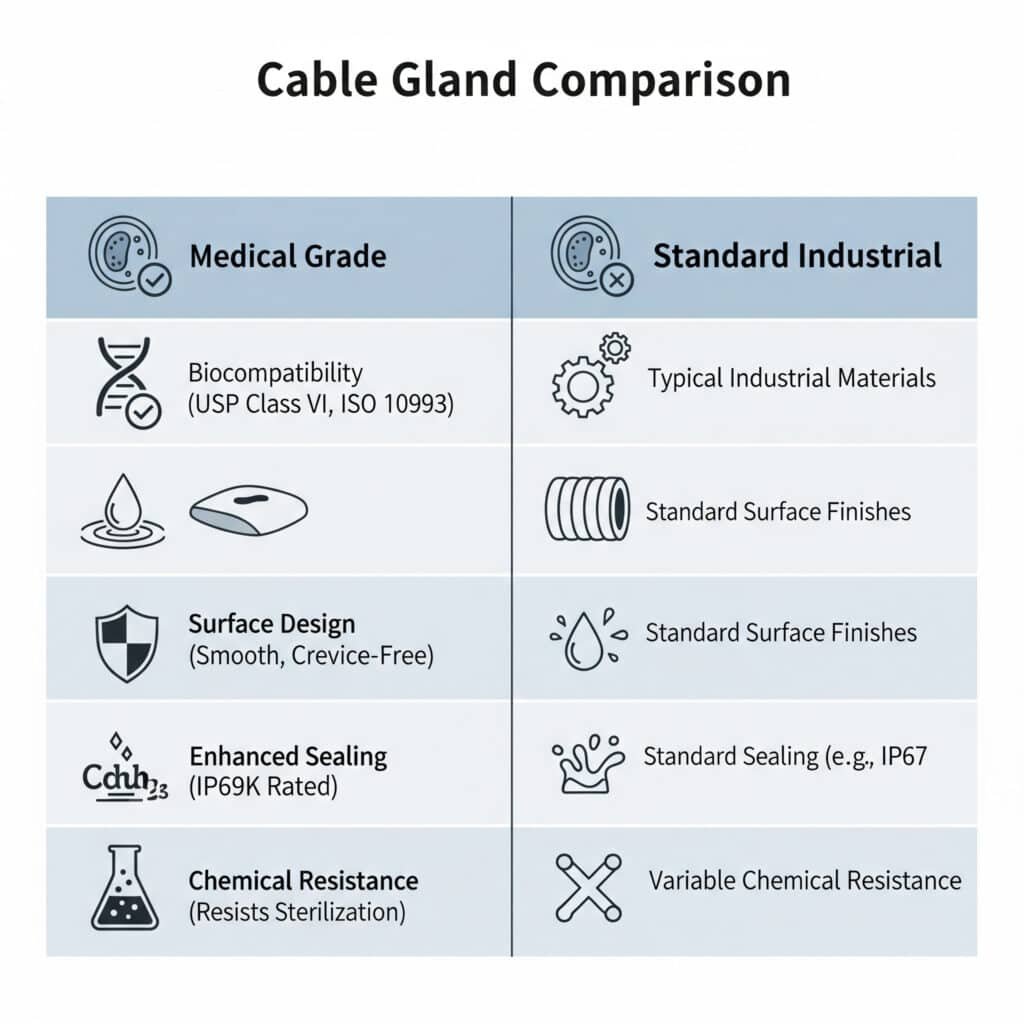
Medicinska kabelska vtičnika se od standardnih vtičnikov razlikujejo po uporabi biokompatibilnih materialov, gladkih čistljivih površinah, skladnosti s predpisi FDA, izboljšanem tesnjenju za preprečevanje kontaminacije in kemični odpornosti na čistilna sredstva in postopke sterilizacije, pri čemer posebne zasnove odpravljajo razpoke, v katerih se lahko zadržujejo bakterije, hkrati pa ohranjajo električno zmogljivost v kritičnih okoljih zdravstva.
Razumevanje teh razlik je ključnega pomena, saj imajo medicinske aplikacije edinstvene varnostne in regulativne zahteve, ki jih standardna industrijska žrela ne morejo ustrezno izpolniti.
Zahteve glede biokompatibilnosti
Skladnost z USP razreda VI: Za medicinske kabelske žleze morajo biti uporabljeni materiali, ki so uspešno prestali biološko testiranje razreda VI ameriške farmakopeje za biokompatibilnost in varnost pri uporabi v medicinskih pripomočkih.
Standardi ISO 10993: Materiali morajo ustrezati ISO 109932 biološke standarde za ocenjevanje medicinskih pripomočkov, ki zagotavljajo, da nimajo citotoksičnih, senzibilizirajočih ali dražečih učinkov na človeško tkivo.
Odobritev FDA 21 CFR 177: Za uporabo v farmacevtskih in medicinskih pripomočkih se pogosto zahtevajo materiali, ki ustrezajo predpisom FDA za neposreden in posreden stik z živili.
Biokompatibilni polimeri: Specializirani materiali, kot so medicinski PEEK, PTFE ali farmacevtski najlon, zagotavljajo biokompatibilnost brez poslabšanja mehanskih lastnosti.
Oblikovanje površin za čiščenje
Gladka površinska obdelava: Medicinske žleze imajo izjemno gladke površine z vrednostmi Ra, ki so običajno pod 0,8 mikrometra, kar preprečuje prijemanje bakterij in omogoča učinkovito čiščenje.
Zasnova brez razpok: Odprava ostrih vogalov, globokih navojev in zapletenih geometrijskih oblik, v katerih se lahko zadržujejo bakterije ali ki bi lahko kljubovale postopkom čiščenja in sterilizacije.
Zaobljeni robovi: Vse zunanje površine imajo zaobljene robove in gladke prehode, kar olajša čiščenje in preprečuje poškodbe rokavic za čiste prostore ali sterilne embalaže.
Minimalna površina: Racionalizirane zasnove zmanjšujejo površino, ki je izpostavljena onesnaženju, hkrati pa ohranjajo potrebno mehansko in električno zmogljivost.
Izboljšana učinkovitost tesnjenja
Ocene IP68+: Vrhunska okoljska zaščita, ki presega standard IP68 in pogosto dosega IP69K za visokotlačno in visokotemperaturno čiščenje.
Ovire za kontaminacijo: Več stopenj tesnjenja preprečuje vdor delcev, bakterij in kemikalij za čiščenje, ki bi lahko ogrozili sterilno okolje.
Odpornost na pritisk: Izboljšane vrednosti tlaka, ki vzdržijo agresivne postopke čiščenja in sterilizacije, ne da bi prišlo do okvare tesnila.
Dolgoročna zanesljivost: Materiali za tesnjenje ohranijo celovitost pri večkratnih sterilizacijskih ciklih in izpostavljenosti ostrim čistilnim kemikalijam.
Lastnosti kemične odpornosti
Združljivost s čistilnimi sredstvi: Odpornost na bolnišnična dezinfekcijska sredstva, kvarterne amonijeve spojine, vodikov peroksid in druge agresivne kemikalije za čiščenje.
Odpornost na sterilizacijo: Materiali so odporni na sevanje gama, etilen oksid, parno avtoklaviranje in druge metode sterilizacije brez degradacije.
Farmacevtske kemikalije: Odpornost na topila, kisline, baze in farmacevtske spojine, ki se pogosto pojavljajo v okolju medicinske proizvodnje.
Temperaturna stabilnost: Ohranjanje lastnosti v temperaturnih ciklih sterilizacije in zahtevah za nadzor temperature v čistih prostorih.
David, vodja prostorov v večji farmacevtski tovarni v New Jerseyju, se je soočal s ponavljajočimi se težavami s kontaminacijo na sterilnih polnilnih linijah, kjer so se kljub strogim protokolom čiščenja v standardnih kabelskih žlezah zadrževale bakterije. Obstoječa medeninasta žrela so imela zapletene vzorce navojev in površino, ki jih ni bilo mogoče ustrezno sterilizirati, kar je privedlo do zavrnitve serije in skrbi glede skladnosti z zahtevami FDA. Določili smo kabelska žrela iz nerjavečega jekla za medicinske namene z elektropoliranimi površinami in oblikami brez razpok, ki so izpolnjevale zahteve USP razreda VI. Nadgradnja je odpravila vire kontaminacije, dosegla učinkovitost čiščenja 99,9% in pripomogla k temu, da je obrat uspešno opravil inšpekcijske preglede FDA, hkrati pa je za 85% zmanjšala število zavrnjenih izdelkov 😊.
Kako izpolnjujete predpise FDA in medicinske pripomočke?
Za izpolnjevanje predpisov FDA in medicinskih pripomočkov je treba uporabljati materiale z ustreznimi certifikati, voditi podrobno dokumentacijo, upoštevati Dobra proizvodna praksa (GMP)3, zagotavljanje sledljivosti in izvajanje sistemov kakovosti, ki so skladni z 21 CFR del 820, pri čemer medicinske kabelske žleze zahtevajo materiale, ki jih je odobrila FDA, testiranje biokompatibilnosti in nadzor proizvodnje, ki zagotavljajo stalno kakovost in varnost pri uporabi medicinskih pripomočkov.
Skladnost s predpisi je v medicinskih aplikacijah nujna, saj lahko napake povzročijo poškodbe bolnikov, odpoklice izdelkov in hude pravne posledice.
Zahteve FDA za materiale
21 CFR del 177: Materiali, ki so v stiku s farmacevtskimi izdelki ali medicinskimi pripomočki, morajo izpolnjevati predpise FDA o aditivih za živila za snovi, ki so v posrednem stiku z živili.
Glavna datoteka za dostop (MAF): Dobavitelji morajo vzdrževati glavne datoteke FDA za dostop, ki dokumentirajo varnost materialov, proizvodne procese in postopke nadzora kakovosti.
glavna dokumentacija o zdravilih (DMF): Pri farmacevtskih aplikacijah se lahko za materiale zahteva registracija glavne dokumentacije o zdravilih s podrobnimi informacijami o sestavi in proizvodnji.
Potrdilo o skladnosti: Dobavitelji morajo predložiti potrdila, ki potrjujejo, da materiali izpolnjujejo vse veljavne predpise in specifikacije FDA.
Standardi kakovosti medicinskih pripomočkov
Skladnost s standardom ISO 13485: Proizvodnja mora upoštevati sisteme vodenja kakovosti medicinskih pripomočkov ISO 13485 za načrtovanje, proizvodnjo in nadzor po dajanju na trg.
21 CFR del 820 (QSR): Skladnost s predpisi o sistemu kakovosti, ki zagotavljajo ustrezen nadzor načrtovanja, nadzor dokumentov in korektivne/preventivne ukrepe.
Upravljanje tveganj: Postopki upravljanja tveganja za medicinske pripomočke po standardu ISO 14971, vključno z analizo tveganja, vrednotenjem in nadzornimi ukrepi.
Nadzor oblikovanja: Formalni postopki nadzora načrtovanja, vključno z načrtovanjem načrtovanja, vhodnimi/izhodnimi zahtevami, pregledi, preverjanjem in potrjevanjem.

Dokumentacija in sledljivost
Certifikati o materialu: Popolna sledljivost materialov s potrdili o analizi, rezultati testov biokompatibilnosti in dokumentacijo o skladnosti s predpisi.
Zapisi o proizvodnji: Podrobna proizvodna dokumentacija, vključno s procesnimi parametri, preskušanjem nadzora kakovosti in dokumentacijo serije za popolno sledljivost.
Nadzor sprememb: Formalni postopki nadzora sprememb za vse spremembe materialov, postopkov ali specifikacij, ki vplivajo na skladnost z zakonodajo.
Kvalifikacija dobavitelja: Celoviti programi kvalifikacije dobaviteljev, ki zagotavljajo, da vsi materiali in komponente izpolnjujejo zahteve za medicinske pripomočke.
Zahteve za potrjevanje
Testiranje biokompatibilnosti: Testiranje USP razreda VI, vključno s testi sistemskega vbrizgavanja, intrakutanega vbrizgavanja in implantacije za preverjanje biološke varnosti.
Potrjevanje čiščenja: Dokumentirani postopki čiščenja z validacijskimi podatki, ki dokazujejo učinkovito odstranjevanje kontaminantov in zmanjšanje biološke obremenitve.
Potrjevanje sterilizacije: Validacija postopkov sterilizacije, vključno s kartiranjem odmerkov, stopnjami zagotavljanja sterilnosti in študijami združljivosti materialov.
Preizkušanje zmogljivosti: Električno, mehansko in okoljsko preskušanje za preverjanje skladnosti delovanja z zahtevami za medicinske pripomočke v celotnem življenjskem ciklu izdelka.
Podpora pri predložitvi regulativnih zahtevkov
Dokumentacija 510(k): Tehnična dokumentacija, ki podpira predložitev dokumentacije FDA 510(k) za medicinske pripomočke, ki vsebujejo kabelske vložke.
Tehnične datoteke: Celovita tehnična dokumentacija za označevanje CE v skladu z Uredbo o medicinskih pripomočkih (MDR) na evropskih trgih.
Sporazumi o kakovosti: Formalni sporazumi o kakovosti z dobavitelji, ki opredeljujejo odgovornosti, specifikacije in zahteve glede skladnosti.
Revizijska podpora: Podpora pri revizijah FDA, priglašenih organov in strank, vključno s pregledom dokumentacije in pregledi objektov.
Kateri materiali so potrebni za uporabo v čistih prostorih?
Aplikacije za čiste prostore zahtevajo materiale z nizkimi izpušnimi lastnostmi, odpornostjo proti nastajanju delcev, kemično združljivostjo s čistilnimi sredstvi, gladkimi neporoznimi površinami in ustreznimi ravnmi prevodnosti, pri čemer nerjavno jeklo 316L, PEEK, PTFE in specializirani polimeri, odobreni za čiste prostore, zagotavljajo optimalno zmogljivost in hkrati izpolnjujejo ISO 146444 standardi za čiste prostore in ohranjanje električne celovitosti v nadzorovanih okoljih.
Izbira materiala je ključnega pomena, saj je za čiste prostore potreben strog nadzor nad onesnaženostjo z delci in molekulami, ki lahko ogrozijo kakovost izdelka ali sterilne pogoje.
Zahteve iz nerjavečega jekla
316L Medicinski razred: Austenitno nerjavno jeklo z nizko vsebnostjo ogljika, ki zagotavlja odlično odpornost proti koroziji in biokompatibilnost za uporabo v medicini.
Elektropolirani zaključek: Z elektropoliranjem odstranite površinske nepravilnosti, zmanjšate nastajanje delcev in ustvarite gladke površine za učinkovito čiščenje.
Obdelava s pasivacijo: Kemična pasivacija poveča korozijsko odpornost in odstrani onesnaženje z železom, ki bi lahko povzročilo razbarvanje ali nastajanje delcev.
Hrapavost površine: Vrednosti Ra pod 0,8 mikrometra (32 mikroinčev) zmanjšujejo oprijem bakterij ter olajšajo postopke čiščenja in sterilizacije.
Visoko zmogljivi polimeri
PEEK (polieterski eteroketon): Zaradi odlične kemične odpornosti, nizke stopnje izpuščanja in biokompatibilnosti je PEEK idealen za uporabo v farmacevtskih in medicinskih pripomočkih.
PTFE (politetrafluoretilen): Izjemna kemična inertnost in nelepljivost zagotavljata odlično odpornost na čistilne kemikalije in biološke materiale.
Medicinski najlon: Posebej oblikovani najloni z odobritvijo USP razreda VI zagotavljajo dobre mehanske lastnosti in biokompatibilnost za uporabo v medicini.
POM, odobren za čiste prostore: Polioksimetilen z majhnim nastajanjem delcev in dobro dimenzijsko stabilnostjo za uporabo v natančnih čistih prostorih.
Združljivost z razvrstitvijo čistih prostorov
ISO razred 5 (razred 100): Izjemno gladke površine z minimalnim nastajanjem delcev za polprevodnike in farmacevtsko proizvodnjo.
ISO razred 6 (razred 1000): Zmeren nadzor delcev za proizvodnjo medicinskih pripomočkov in nekatere farmacevtske postopke.
Razred ISO 7 (razred 10000): Standardne zahteve za čiste prostore za splošno montažo farmacevtskih izdelkov in medicinskih pripomočkov.
ISO razred 8 (razred 100000): Osnovne zahteve za čiste prostore za pakiranje in nekatere postopke izdelave medicinskih pripomočkov.
Nadzor izpustov in kontaminacije
Materiali z nizko vsebnostjo izpustov: Materiali z minimalnimi emisijami hlapnih organskih spojin (HOS), ki bi lahko onesnažile občutljive postopke ali izdelke.
Molekularna kontaminacija: Nadzor molekularnih onesnaževalcev, vključno s silikoni, mehčalci in drugimi organskimi spojinami, ki lahko vplivajo na kakovost izdelka.
Ionska kontaminacija: Materiali z nizko vsebnostjo ionov za preprečevanje kontaminacije elektronskih komponent in farmacevtskih izdelkov.
Snovi, ki jih je mogoče ekstrahirati: Najmanj snovi, ki jih je mogoče izločiti in ki bi se med uporabo lahko izlužile v farmacevtske izdelke ali čistilne raztopine.
Matrika kemijske združljivosti
| Sredstvo za čiščenje | 316L SS | PEEK | PTFE | Medicinski najlon |
|---|---|---|---|---|
| Izopropilni alkohol | Odlično | Odlično | Odlično | Dobro |
| Vodikov peroksid | Odlično | Odlično | Odlično | Fair |
| Četverni amonij | Odlično | Odlično | Odlično | Dobro |
| Natrijev hipoklorit | Dobro | Odlično | Odlično | Slaba |
| perocetna kislina | Dobro | Odlično | Odlično | Slaba |
Hassan, ki vodi dejavnosti v najsodobnejšem farmacevtskem obratu v Švici, je moral nadgraditi kabelske žile v čistem prostoru razreda ISO 5 za proizvodnjo sterilnih injekcij. Obstoječa dvojajčna vodila so med cikli čiščenja ustvarjala delce in niso prenesla agresivnih sterilizacijskih protokolov, ki so bili potrebni za njihove nove biološke izdelke. Zagotovili smo elektropolirana kabelska vodila iz nerjavnega jekla 316L s potrjenim nizkim nastajanjem delcev in popolno kemijsko združljivostjo s postopki čiščenja in sterilizacije. Z nadgradnjo smo dosegli število delcev 90% pod mejnimi vrednostmi ISO razreda 5, odpravili dogodke kontaminacije, povezane s čiščenjem, in podprli uspešno validacijo njihove nove sterilne proizvodne linije.
Kako zagotoviti ustrezno združljivost čiščenja in sterilizacije?
Za zagotavljanje ustrezne združljivosti čiščenja in sterilizacije je treba izbrati materiale, ki so odporni na večkratno izpostavljenost kemikalijam za čiščenje in metodam sterilizacije, oblikovati površine za popolno čiščenje, potrditi postopke čiščenja in voditi podrobno dokumentacijo, pri čemer medicinski kabelski vložki zahtevajo gladke površine brez gub, materiale, odporne na kemikalije, in potrjene protokole čiščenja, ki dosegajo zahtevane ravni zagotavljanja sterilnosti.
Združljivost čiščenja in sterilizacije je bistvenega pomena, saj lahko neustrezna dekontaminacija povzroči kontaminacijo izdelkov, tveganje za varnost pacientov in kršitve predpisov.
Združljivost metode sterilizacije
Avtoklaviranje s paro: Materiali morajo biti odporni na temperaturo 121°C-134°C parno avtoklaviranje5 ciklov brez degradacije, sprememb dimenzij ali okvare tesnila.
Sevanje gama: Odpornost na odmerke sevanja gama 25-50 kGy, ki se običajno uporabljajo za sterilizacijo medicinskih pripomočkov, brez degradacije materiala.
Etilen oksid (EtO): Kemijska združljivost s sterilizacijo z EtO, vključno z odpornostjo na sterilizacijsko sredstvo in ustreznimi lastnostmi odplinjevanja.
Plazma vodikovega peroksida: Združljivost s sistemi nizkotemperaturne plazemske sterilizacije, vključno s stabilnostjo materiala in popolno penetracijo sterilizacijskega sredstva.
Zahteve za validacijo čiščenja
Postopki čiščenja: Dokumentirani postopki čiščenja, ki določajo kemikalije, koncentracije, čas stika in mehanske ukrepe, potrebne za učinkovito dekontaminacijo.
Protokoli potrjevanja: Formalne validacijske študije, ki dokazujejo učinkovitost čiščenja z uporabo scenarijev najhujše kontaminacije in analitičnih testov.
Merila sprejemljivosti: Opredeljena merila sprejemljivosti za čistočo, vključno z vizualnim pregledom, številom delcev, ravnmi biološke obremenitve in mejnimi vrednostmi kemičnih ostankov.
Redno spremljanje: Programi stalnega spremljanja za preverjanje nadaljnje učinkovitosti čiščenja in ugotavljanje morebitnega poslabšanja učinkovitosti.
Razmisleki o oblikovanju površine
Značilnosti odvodnjavanja: Konstrukcijske značilnosti, ki omogočajo popolno odtekanje čistilnih raztopin in preprečujejo nabiranje v bazenih, v katerih bi se lahko zadrževala onesnaževala.
Dostopnost: Vse površine morajo biti dostopne za čiščenje s standardnimi čistilnimi orodji in postopki, ki se uporabljajo v zdravstvenih ustanovah.
Zahteve za razstavljanje: Upoštevajte, ali je treba žleze za čiščenje razstaviti ali pa za uporabo zadostuje nepoškodovano čiščenje.
Zamenjava tesnila: Postopki za zamenjavo in potrditev tesnil, kadar je treba tesnilne sestavne dele zaradi izpostavljenosti kemikalijam pri čiščenju redno zamenjati.
Dokumentacija in skladnost
Navodila za čiščenje: Podrobna navodila za čiščenje, vključno s postopki po korakih, kemičnimi specifikacijami in varnostnimi ukrepi.
Varnostni podatki o materialu: Popolne informacije o varnosti materiala, vključno s kemijsko združljivostjo, temperaturnimi omejitvami in združljivostjo pri sterilizaciji.
Poročila o potrjevanju: Poročila o validaciji čiščenja, ki dokazujejo učinkovitost in določajo zahteve za redno spremljanje.
Gradivo za usposabljanje: Gradivo za usposabljanje osebja v ustanovi o pravilnem čiščenju, ravnanju in vzdrževanju medicinskih kabelskih žlez.
Testiranje nadzora kakovosti
Testiranje biološke obremenitve: Redno testiranje mikrobne kontaminacije za preverjanje učinkovitosti čiščenja in prepoznavanje morebitnih problematičnih območij.
Testiranje endotoksinov: Testiranje bakterijskih endotoksinov, ki lahko povzročijo pirogene reakcije v farmacevtskih in medicinskih pripomočkih.
Štetje delcev: Testiranje števila delcev za preverjanje, ali so po čiščenju in vzdrževanju izpolnjene zahteve za čiste prostore.
Analiza kemičnih ostankov: Testiranje ostankov čistilnih kemikalij, ki bi lahko onesnažili izdelke ali vplivali na biokompatibilnost.
Katera so ključna merila za izbiro različnih medicinskih aplikacij?
Ključna merila za izbiro se razlikujejo glede na aplikacijo, vendar vključujejo zahteve glede skladnosti z zakonodajo, ravni biokompatibilnosti, klasifikacije čistih prostorov, metode sterilizacije, izpostavljenost kemikalijam in potrebe po električni zmogljivosti, pri čemer kirurška oprema zahteva najvišjo biokompatibilnost, farmacevtska proizvodnja kemično odpornost, diagnostična oprema pa se osredotoča na električno celovitost, medtem ko vse aplikacije zahtevajo ustrezne regulativne certifikate in združljivost s čiščenjem.
Različne medicinske aplikacije imajo edinstvene zahteve, ki jih je treba skrbno upoštevati pri izbiri kabelskih žlez, da zagotovimo optimalno delovanje in skladnost z zakonodajo.
Kirurška oprema in oprema za stik z bolniki
Zahteve za neposredni stik: Biokompatibilnost razreda VI USP z dodatnim testiranjem citotoksičnosti za materiale v neposrednem stiku z bolnikom med kirurškimi posegi.
Pogostost sterilizacije: sposobnost prenašanja pogostih sterilizacijskih ciklov brez degradacije, pri čemer se običajno zahtevajo materiali, ki so stabilni v več sto sterilizacijskih ciklih.
Električna varnost: Izboljšane zahteve glede električne varnosti, vključno z nizkim uhajalnim tokom in zanesljivo izolacijo za opremo, povezano z bolnikom.
Zanesljivost v nujnih primerih: Kritične zahteve glede zanesljivosti za opremo za vzdrževanje življenjskih funkcij in nujno medicinsko pomoč, pri kateri lahko odpoved neposredno vpliva na varnost pacientov.
Farmacevtska proizvodnja
Skladnost z GMP: zahteve dobre proizvodne prakse, vključno s sledljivostjo materiala, nadzorom sprememb in dokumentacijo o validaciji.
Varnost pri stiku z izdelkom: Materiali, ki ne onesnažujejo farmacevtskih izdelkov zaradi izpiranja, nastajanja delcev ali kemične interakcije.
Potrjevanje čiščenja: Obsežne zahteve za validacijo čiščenja z dokumentiranimi postopki in merili sprejemljivosti za farmacevtsko proizvodnjo.
Dokumentacija serije: Popolna dokumentacija serij in sledljivost materialov, ki se uporabljajo v farmacevtski proizvodni opremi.
Diagnostična in laboratorijska oprema
Zahteve glede natančnosti: Dimenzijska stabilnost in natančnost za analitične instrumente, ki zahtevajo dosledno mehansko in električno delovanje.
Kemijska odpornost: Odpornost na laboratorijske kemikalije, reagente in čistilna topila, ki se pogosto uporabljajo v diagnostičnih aplikacijah.
Uspešnost EMC: Zahteve za elektromagnetno združljivost občutljivih analitičnih instrumentov in diagnostične opreme.
Stabilnost kalibracije: Mehanska stabilnost, ki sčasoma ne vpliva na kalibracijo instrumenta ali natančnost meritev.
Proizvodnja medicinskih pripomočkov
Validacija procesa: Materiali in sestavni deli, ki podpirajo zahteve za potrjevanje postopkov v proizvodnji medicinskih pripomočkov.
Sistemi kakovosti: Integracija s sistemi kakovosti ISO 13485, vključno s postopki kvalifikacije dobaviteljev in vhodnega nadzora.
Upravljanje tveganj: Materiali, ki podpirajo zahteve za upravljanje tveganj medicinskih pripomočkov, vključno z analizo načina odpovedi in strategijami za ublažitev.
Regulativna podpora: Podpora dobavitelja za regulativne vloge, vključno s tehnično dokumentacijo in regulativnim strokovnim znanjem.
Matrika za odločanje o izbiri
| Vrsta uporabe | Osnovna merila | Sekundarna merila | Kritični standardi |
|---|---|---|---|
| Kirurška oprema | Biokompatibilnost | Sterilizacija | USP razred VI, ISO 10993 |
| Farmacevtski | Kemijska odpornost | Skladnost z GMP | FDA 21 CFR, cGMP |
| Diagnostika | Natančnost | Uspešnost EMC | IEC 61326, ISO 15189 |
| Proizvodnja | Potrjevanje procesa | Sistemi kakovosti | ISO 13485, 21 CFR 820 |
Analiza stroškov in koristi
Začetni stroški v primerjavi z življenjskim ciklom: Upoštevajte skupne stroške lastništva, vključno s stroški vzdrževanja, zamenjave in skladnosti v življenjski dobi opreme.
Regulativno tveganje: Uravnotežite materialne stroške s tveganji skladnosti z zakonodajo in morebitnimi stroški neskladnosti.
Zahteve za delovanje: Zagotovite, da izbrani materiali izpolnjujejo minimalne zahteve glede zmogljivosti brez pretiranih specifikacij, ki po nepotrebnem povečujejo stroške.
Zmogljivosti dobavitelja: Ocenite zmogljivosti dobaviteljev za stalno podporo, dokumentacijo in pomoč pri izpolnjevanju predpisov.
Zaključek
Pri izbiri kabelskih ovojev za medicinsko opremo in čiste prostore je treba razumeti posebne zakonske zahteve, zahteve glede materialov in zmogljivosti, ki te aplikacije razlikujejo od standardne industrijske uporabe. Uspeh je odvisen od uravnoteženja biokompatibilnosti, čistosti, skladnosti s predpisi in električne zmogljivosti.
Ključ do zanesljivega delovanja medicinskih kabelskih žlez je v sodelovanju z dobavitelji, ki razumejo predpise o medicinskih pripomočkih ter lahko zagotovijo ustrezne materiale, dokumentacijo in stalno podporo v celotnem življenjskem ciklu izdelka. V podjetju Bepto smo specializirani za medicinska kabelska žrela, ki izpolnjujejo zahteve FDA in mednarodne standarde za medicinske pripomočke, ter zagotavljamo zagotavljanje kakovosti in regulativno podporo, potrebno za kritične aplikacije v zdravstvu.
Pogosta vprašanja o medicinskih kabelskih žicah
V: Katere certifikate potrebujem za medicinske kabelske žile?
A: Medicinski kabelski vložki običajno zahtevajo certifikat biokompatibilnosti USP razreda VI, skladnost materialov s standardom FDA 21 CFR in proizvodne sisteme kakovosti ISO 13485. Posebne zahteve so odvisne od vaše uporabe in regulativne pristojnosti.
V: Ali se lahko običajna kabelska ovojnica iz nerjavnega jekla uporablja v medicinskih aplikacijah?
A: Običajno nerjavno jeklo morda ne izpolnjuje medicinskih zahtev. Za uporabo v medicini je potrebno nerjavno jeklo 316L medicinske kakovosti z elektropoliranim zaključkom, testiranjem biokompatibilnosti in ustrezno dokumentacijo za skladnost s predpisi.
V: Kako čistim in steriliziram medicinske kabelske žile?
A: Upoštevajte proizvajalčeve potrjene postopke čiščenja z uporabo odobrenih čistilnih sredstev in metod sterilizacije. Večina medicinskih žlez podpira avtoklaviranje s paro, sevanje gama ali kemično sterilizacijo ob ustrezni združljivosti materialov.
V: Kakšna je razlika med kabelskimi vtičnicami za čiste prostore in medicinskimi kabelskimi vtičnicami?
A: Medicinski razred vključuje zahteve glede biokompatibilnosti in skladnosti s predpisi FDA, medtem ko se razred za čiste prostore osredotoča na nadzor delcev in kemično odpornost. Pri nekaterih aplikacijah so potrebne tako medicinske specifikacije kot specifikacije za čiste prostore.
V: Kako pogosto je treba zamenjati medicinske kabelske žleze?
A: Pogostost zamenjave je odvisna od sterilizacijskih ciklov, izpostavljenosti kemikalijam in priporočil proizvajalca. Običajno jih preglejte po vsakih 100-200 sterilizacijskih ciklih in jih zamenjajte na podlagi ocene stanja in zahtev za validacijo.
-
Spoznajte posebne teste biološke reaktivnosti, ki se zahtevajo za certificiranje USP razreda VI. ↩
-
Oglejte si pregled serije standardov ISO 10993 za biološko vrednotenje medicinskih pripomočkov. ↩
-
Preglejte uradne smernice in predpise FDA za trenutno dobro proizvodno prakso (cGMP). ↩
-
Oglejte si podroben vodnik po standardih ISO 14644 za razvrščanje čistosti zraka v čistih prostorih. ↩
-
Razumeti načela parne sterilizacije, vključno z vlogo časa, temperature in tlaka. ↩



