Неправильный выбор кабельных вводов в медицинских и чистых помещениях приводит к рискам загрязнения, нарушению нормативных требований и сбоям в работе оборудования, что влечет за собой угрозу безопасности пациентов, дорогостоящие остановки предприятий и нарушения требований FDA, а недостаточная герметичность, неподходящие материалы и плохая очищаемость приводят к росту бактерий, загрязнению твердыми частицами и нарушению стерильности, что ставит под угрозу важнейшие операции в здравоохранении. Многие руководители предприятий сталкиваются с проблемой выбора сальников, которые отвечают строгим медицинским стандартам, сохраняя при этом надежные электрические характеристики.
Выбор кабельных вводов для медицинского оборудования и чистых помещений требует понимания правил FDA, USP Класс VI1 Требования к материалам, стандарты герметичности IP68+ и классификация чистых помещений. Конструкция из нержавеющей стали медицинского класса или специализированных полимеров обеспечивает биосовместимость, химическую стойкость и гладкие поверхности для эффективной очистки и стерилизации, сохраняя при этом целостность электрической сети в критически важных областях здравоохранения. Успех зависит от баланса между соблюдением нормативных требований и эксплуатационной надежностью.
Работая с инженерами больниц в крупных медицинских центрах Бостона, фармацевтическими производителями в Швейцарии и специалистами по чистоте помещений в Сингапуре, я понял, что кабельные вводы медицинского класса необходимы для поддержания стерильной среды и обеспечения безопасности пациентов. Позвольте мне поделиться важнейшими знаниями о том, как выбрать оптимальные сальники для применения в медицине и чистых помещениях.
Оглавление
- Чем медицинские кабельные вводы отличаются от стандартных?
- Как обеспечить соответствие требованиям FDA и правилам производства медицинских изделий?
- Какие материалы требуются для чистых помещений?
- Как обеспечить надлежащую совместимость при очистке и стерилизации?
- Каковы ключевые критерии выбора для различных областей применения в медицине?
- Вопросы и ответы о медицинских кабельных вводах
Чем медицинские кабельные вводы отличаются от стандартных?
Медицинские кабельные вводы отличаются от стандартных вводов использованием биосовместимых материалов, гладкой очищаемой поверхностью, соответствием нормам FDA, повышенной герметичностью для предотвращения загрязнения, химической стойкостью к чистящим средствам и процессам стерилизации, а также специальной конструкцией, исключающей образование щелей, в которых могут размножаться бактерии, и сохраняющей электрические характеристики в критических условиях здравоохранения.
Понимание этих различий крайне важно, поскольку медицинские приложения имеют уникальные требования к безопасности и нормативным требованиям, которые стандартные промышленные сальники не могут удовлетворить.
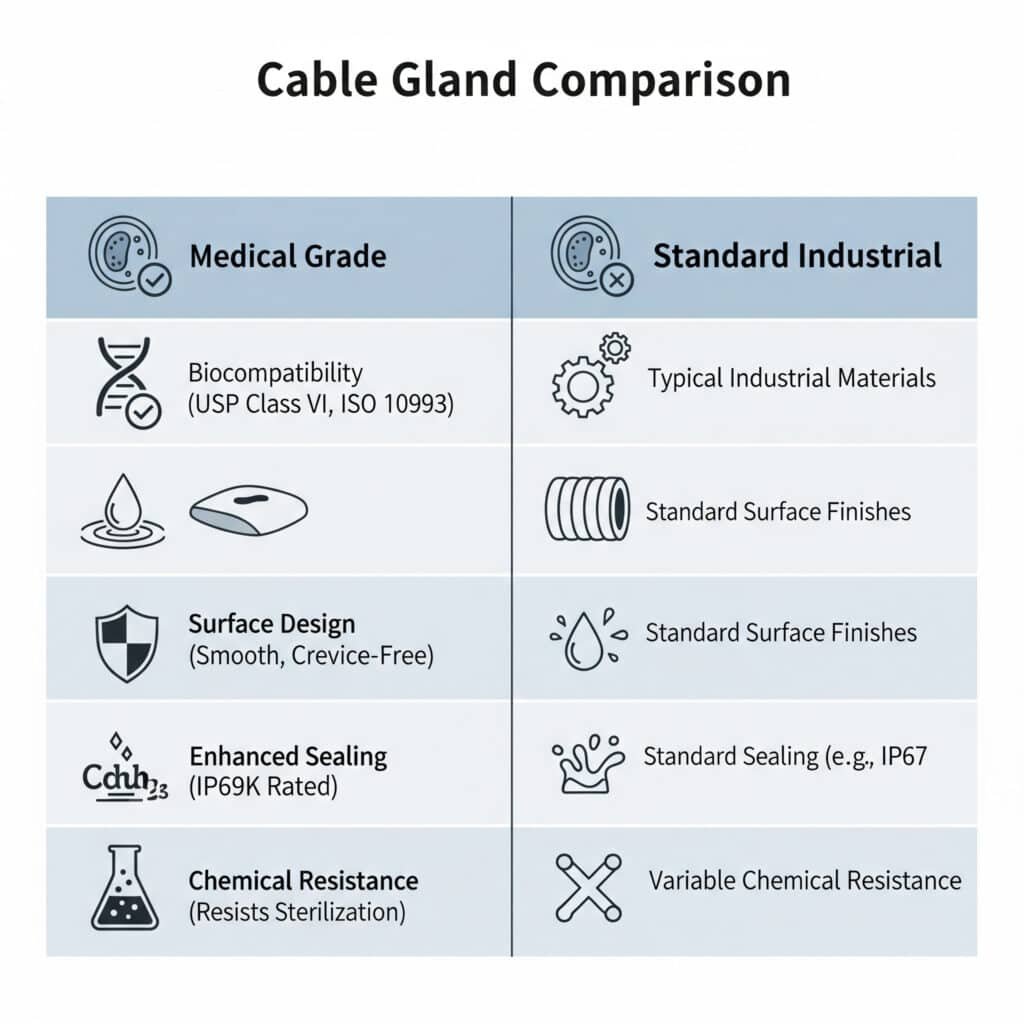
Требования к биосовместимости
Соответствие требованиям USP Class VI: Для изготовления медицинских кабельных вводов должны использоваться материалы, прошедшие биологические испытания United States Pharmacopeia Class VI на биосовместимость и безопасность при использовании в медицинских устройствах.
Стандарты ISO 10993: Материалы должны соответствовать ISO 109932 стандарты биологической оценки медицинских изделий, гарантирующие отсутствие цитотоксического, сенсибилизирующего или раздражающего воздействия на ткани человека.
Одобрение FDA 21 CFR 177: Для применения в фармацевтике и медицинском оборудовании часто требуются материалы пищевого класса, отвечающие требованиям FDA по прямому и непрямому контакту с пищевыми продуктами.
Биосовместимые полимеры: Специализированные материалы, такие как PEEK, PTFE или нейлон фармацевтического качества, обеспечивают биосовместимость без ущерба для механических свойств.
Дизайн поверхности для обеспечения чистоты
Гладкая поверхность: Медицинские сальники имеют ультрагладкую поверхность с показателем Ra, обычно не превышающим 0,8 микрометра, что предотвращает прилипание бактерий и обеспечивает эффективную очистку.
Дизайн без трещин: Устранение острых углов, глубоких резьб и сложных геометрических форм, которые могут стать причиной размножения бактерий или противостоять процессам очистки и стерилизации.
Скругленные края: Все внешние поверхности имеют закругленные края и плавные переходы для облегчения очистки и предотвращения повреждения перчаток для чистых помещений или стерильной упаковки.
Минимальная площадь поверхности: Обтекаемые конструкции минимизируют площадь поверхности, подверженной загрязнению, сохраняя при этом необходимые механические и электрические характеристики.
Улучшенные характеристики герметизации
Степень защиты IP68+: Превосходная защита от воздействия окружающей среды, превышающая стандартный IP68, часто достигающая IP69K для применения в системах очистки под высоким давлением и при высоких температурах.
Барьеры от загрязнений: Многоступенчатая герметизация предотвращает попадание частиц, бактерий и чистящих химикатов, которые могут нарушить стерильность среды.
Устойчивость к давлению: Повышенные показатели давления позволяют выдерживать агрессивные процедуры очистки и стерилизации без разрушения уплотнений.
Долгосрочная надежность: Уплотнительные материалы сохраняют целостность при многократных циклах стерилизации и воздействии агрессивных чистящих средств.
Свойства химической стойкости
Совместимость с чистящими средствами: Устойчивость к дезинфицирующим средствам больничного класса, четвертичным аммониевым соединениям, перекиси водорода и другим агрессивным чистящим средствам.
Устойчивость к стерилизации: Материалы выдерживают гамма-излучение, окись этилена, автоклавирование паром и другие методы стерилизации, не разрушаясь.
Фармацевтическая химия: Устойчивость к растворителям, кислотам, щелочам и фармацевтическим соединениям, обычно встречающимся в условиях медицинского производства.
Стабильность температуры: Сохранение свойств с помощью температурных циклов стерилизации и требований по контролю температуры в чистых помещениях.
Дэвид, менеджер по производству крупного фармацевтического завода в Нью-Джерси, столкнулся с проблемой постоянного загрязнения стерильных линий розлива, где стандартные кабельные вводы содержали бактерии, несмотря на строгие протоколы очистки. Существующие латунные сальники имели сложный рисунок резьбы и поверхностную отделку, которые не поддавались адекватной стерилизации, что приводило к браку партий и проблемам с соблюдением требований FDA. Мы предложили кабельные вводы из нержавеющей стали медицинского класса с электрополированной поверхностью и без щелей, отвечающие требованиям USP Class VI. Модернизация устранила источники загрязнения, обеспечила эффективность очистки 99,9% и помогла предприятию пройти инспекцию FDA, сократив количество брака продукции на 85%. 😊
Как обеспечить соответствие требованиям FDA и правилам производства медицинских изделий?
Соблюдение требований Управления по контролю за продуктами и лекарствами США (FDA) и нормативных требований к медицинским изделиям требует использования материалов, имеющих соответствующие сертификаты, ведения подробной документации, соблюдения Надлежащая производственная практика (GMP)3Обеспечение прослеживаемости и внедрение систем качества, соответствующих 21 CFR Part 820. Для медицинских кабельных вводов требуются материалы, одобренные FDA, испытания на биосовместимость и производственный контроль, которые обеспечивают постоянное качество и безопасность при использовании медицинских устройств.
Соответствие нормативным требованиям является обязательным условием для применения в медицине, поскольку сбои в работе могут привести к нанесению вреда пациентам, отзыву продукции и серьезным юридическим последствиям.
Требования FDA к материалам
21 CFR, часть 177: Материалы, контактирующие с фармацевтическими препаратами или медицинскими устройствами, должны соответствовать требованиям FDA по пищевым добавкам для веществ, непрямо контактирующих с пищевыми продуктами.
Главный файл доступа (MAF): Поставщики должны вести основные файлы доступа FDA, документирующие безопасность материалов, производственные процессы и процедуры контроля качества.
Главная картотека лекарств (DMF): Для применения в фармацевтике материалы могут потребовать регистрации Drug Master File с подробной информацией о составе и производстве.
Сертификат соответствия: Поставщики должны предоставить сертификаты, подтверждающие соответствие материалов всем применимым нормам и спецификациям FDA.
Стандарты качества медицинских изделий
Соответствие стандарту ISO 13485: Производство должно соответствовать системе управления качеством медицинских изделий ISO 13485 при разработке, производстве и постмаркетинговом контроле.
21 CFR, часть 820 (QSR): Соблюдение правил системы качества, обеспечивающих надлежащий контроль проектирования, контроль документации и корректирующие/предупреждающие действия.
Управление рисками: Процессы управления рисками ISO 14971 для медицинских изделий, включая анализ, оценку и меры контроля рисков.
Контроль над дизайном: Формальные процессы управления проектированием, включая планирование проектирования, входные/выходные требования, обзоры, верификацию и валидацию.

Документация и прослеживаемость
Сертификаты на материалы: Полная прослеживаемость материалов с сертификатами анализа, результатами испытаний на биосовместимость и документацией о соответствии нормативным требованиям.
Производственные записи: Подробные производственные записи, включая параметры процесса, испытания для контроля качества и документацию по партиям для полной прослеживаемости.
Контроль изменений: Официальные процедуры контроля изменений для любых модификаций материалов, процессов или спецификаций, влияющих на соответствие нормативным требованиям.
Квалификация поставщика: Комплексные программы квалификации поставщиков, обеспечивающие соответствие всех материалов и компонентов требованиям к медицинским изделиям.
Требования к валидации
Испытания на биосовместимость: Испытания USP класса VI, включая системные инъекции, внутрикожные и имплантационные испытания для проверки биологической безопасности.
Проверка чистоты: Документированные процедуры очистки с данными проверки, подтверждающими эффективное удаление загрязнений и снижение биологической нагрузки.
Проверка стерилизации: Валидация процессов стерилизации, включая картирование доз, определение уровней обеспечения стерильности и исследования совместимости материалов.
Тестирование производительности: Электрические, механические и экологические испытания для проверки соответствия характеристик требованиям к медицинским приборам на протяжении всего жизненного цикла изделия.
Поддержка подачи регуляторных документов
Документация 510(k): Техническая документация, поддерживающая заявки FDA 510(k) на медицинские устройства, включающие кабельные вводы.
Технические файлы: Исчерпывающие технические файлы для маркировки CE в соответствии с Положением о медицинских изделиях (MDR) на европейских рынках.
Соглашения о качестве: Официальные соглашения о качестве с поставщиками, определяющие ответственность, спецификации и требования к соблюдению.
Аудиторская поддержка: Поддержка при проведении аудитов FDA, нотифицированных органов и клиентов, включая анализ документации и инспекции производства.
Какие материалы требуются для чистых помещений?
Для применения в чистых помещениях требуются материалы с низким газовыделением, устойчивостью к образованию частиц, химической совместимостью с чистящими средствами, гладкими непористыми поверхностями и соответствующим уровнем проводимости. Медицинская нержавеющая сталь 316L, PEEK, PTFE и специализированные полимеры, одобренные для применения в чистых помещениях, обеспечивают оптимальные характеристики, удовлетворяя при этом требованиям. ISO 146444 Стандарты чистых помещений и поддержание целостности электрооборудования в контролируемых средах.
Выбор материала имеет решающее значение, поскольку чистые помещения требуют строгого контроля над загрязнением твердыми частицами и молекулами, которые могут поставить под угрозу качество продукции или стерильные условия.
Требования к нержавеющей стали
316L Medical Grade: Аустенитная нержавеющая сталь с низким содержанием углерода, обеспечивающая превосходную коррозионную стойкость и биосовместимость для применения в медицине.
Электрополированная отделка: Электрополировка удаляет дефекты поверхности, уменьшает образование частиц и создает гладкие поверхности для эффективной очистки.
Пассивирующая обработка: Химическая пассивация повышает коррозионную стойкость и удаляет загрязнения железом, которые могут вызвать обесцвечивание или образование частиц.
Шероховатость поверхности: Значения Ra ниже 0,8 микрометра (32 микродюйма) минимизируют прилипание бактерий и облегчают процессы очистки и стерилизации.
Высокоэффективные полимеры
PEEK (Polyetheretherketone): Отличная химическая стойкость, низкое газовыделение и биосовместимость делают PEEK идеальным для применения в фармацевтике и медицинских приборах.
PTFE (политетрафторэтилен): Превосходная химическая инертность и антипригарные свойства обеспечивают отличную устойчивость к чистящим химикатам и биологическим материалам.
Нейлон медицинского класса: Специально разработанный нейлон с допуском USP Class VI обеспечивает хорошие механические свойства и биосовместимость для применения в медицине.
Утвержденный для чистых помещений POM: Полиоксиметилен с низким образованием частиц и хорошей стабильностью размеров для прецизионных чистых помещений.
Совместимость с классификацией для чистых помещений
Класс ISO 5 (класс 100): Ультрагладкие поверхности с минимальным образованием частиц для полупроводникового и фармацевтического производства.
Класс ISO 6 (класс 1000): Умеренный контроль частиц для производства медицинского оборудования и некоторых фармацевтических процессов.
Класс ISO 7 (класс 10000): Стандартные требования к чистым помещениям для общих операций по сборке фармацевтических препаратов и медицинских изделий.
Класс ISO 8 (класс 100000): Основные требования к чистоте помещений для упаковки и некоторых процессов производства медицинских изделий.
Контроль за выделением газов и загрязнением
Материалы с низким уровнем выделения газов: Материалы с минимальными выбросами летучих органических соединений (ЛОС), которые могут загрязнить чувствительные процессы или продукты.
Молекулярное загрязнение: Контроль молекулярных загрязнений, включая силиконы, пластификаторы и другие органические соединения, которые могут повлиять на качество продукции.
Ионное загрязнение: Материалы с низким содержанием ионов для предотвращения загрязнения электронных компонентов и фармацевтической продукции.
Извлекаемые вещества: Минимальное количество экстрагируемых веществ, которые могут просочиться в фармацевтическую продукцию или моющие растворы во время использования.
Матрица химической совместимости
| Чистящее средство | 316L SS | PEEK | PTFE | Медицинский нейлон |
|---|---|---|---|---|
| Изопропиловый спирт | Превосходно | Превосходно | Превосходно | Хорошо |
| Перекись водорода | Превосходно | Превосходно | Превосходно | Ярмарка |
| Четвертичный аммоний | Превосходно | Превосходно | Превосходно | Хорошо |
| Гипохлорит натрия | Хорошо | Превосходно | Превосходно | Бедный |
| Надуксусная кислота | Хорошо | Превосходно | Превосходно | Бедный |
Хассану, управляющему операциями на современном фармацевтическом предприятии в Швейцарии, потребовалось обновить кабельные вводы в чистом помещении класса 5 ISO для производства стерильных инъекционных препаратов. Существующие сальники образовывали частицы во время циклов очистки и не выдерживали агрессивных протоколов стерилизации, необходимых для новых биологических продуктов. Мы поставили электрополированные кабельные вводы из нержавеющей стали 316L с подтвержденным низким уровнем образования частиц и полной химической совместимостью с процессами очистки и стерилизации. В результате модернизации количество частиц 90% оказалось ниже пределов класса 5 по ISO, были исключены случаи загрязнения, связанные с очисткой, и была успешно проведена валидация новой стерильной производственной линии.
Как обеспечить надлежащую совместимость при очистке и стерилизации?
Для обеспечения совместимости с чисткой и стерилизацией необходимо выбирать материалы, выдерживающие многократное воздействие чистящих химикатов и методов стерилизации, разрабатывать поверхности, обеспечивающие полную очистку, проверять процедуры очистки и вести подробную документацию. Для медицинских кабельных вводов требуются гладкие поверхности без щелей, химически стойкие материалы и проверенные протоколы очистки, обеспечивающие требуемый уровень стерильности.
Совместимость систем очистки и стерилизации очень важна, поскольку неадекватное обеззараживание может привести к загрязнению продукции, риску для безопасности пациентов и нарушению нормативных требований.
Совместимость с методами стерилизации
Паровое автоклавирование: Материалы должны выдерживать 121°C-134°C автоклавирование паром5 циклов без деградации, изменения размеров и разрушения уплотнений.
Гамма-излучение: Устойчивость к дозам гамма-излучения 25-50 кГр, обычно используемым для стерилизации медицинских приборов, без разрушения материала.
Оксид этилена (EtO): Химическая совместимость со стерилизацией EtO, включая устойчивость к стерилянту и надлежащие характеристики дегазации.
Плазма с перекисью водорода: Совместимость с системами низкотемпературной плазменной стерилизации, включая стабильность материала и полное проникновение стерилизанта.
Требования к валидации очистки
Процедуры очистки: Документированные процедуры очистки с указанием химических веществ, концентраций, времени контакта и механического воздействия, необходимого для эффективного обеззараживания.
Протоколы валидации: Официальные валидационные исследования, демонстрирующие эффективность очистки с использованием наихудших сценариев загрязнения и аналитических испытаний.
Критерии приемлемости: Определены критерии приемки по чистоте, включая визуальный осмотр, количество частиц, уровни биологической нагрузки и предельные уровни химических остатков.
Рутинный мониторинг: Программы постоянного мониторинга для проверки эффективности очистки и выявления любых ухудшений в работе.
Соображения по дизайну поверхности
Особенности дренажа: Конструкция способствует полному отводу моющих растворов и предотвращает скопление загрязняющих веществ.
Доступность: Все поверхности должны быть доступны для очистки стандартными средствами и процедурами, используемыми в медицинских учреждениях.
Требования к разборке: Подумайте, нужно ли разбирать сальники для чистки или достаточно чистить их в процессе эксплуатации.
Замена прокладки: Процедуры замены и проверки прокладок, когда уплотнительные компоненты требуют периодической замены из-за воздействия чистящих химических веществ.
Документация и соблюдение требований
Инструкции по очистке: Подробные инструкции по очистке, включая пошаговые процедуры, спецификации химикатов и меры предосторожности.
Данные по безопасности материала: Полная информация о безопасности материалов, включая химическую совместимость, температурные ограничения и совместимость со стерилизацией.
Отчеты о проверке: Отчеты о валидации очистки, демонстрирующие эффективность и устанавливающие требования к регулярному мониторингу.
Учебные материалы: Учебные материалы для персонала учреждений по надлежащим процедурам очистки, обращения и обслуживания медицинских кабельных вводов.
Тестирование для контроля качества
Испытание на бионагрузку: Регулярное тестирование на микробное загрязнение для проверки эффективности очистки и выявления потенциальных проблемных зон.
Испытание на эндотоксины: Тестирование на наличие бактериальных эндотоксинов, которые могут вызывать пирогенные реакции в фармацевтике и медицинском оборудовании.
Подсчет частиц: Проверка количества частиц для подтверждения соблюдения требований к чистоте помещения после уборки и технического обслуживания.
Анализ химических остатков: Тестирование на наличие остатков чистящих химических веществ, которые могут загрязнить продукцию или повлиять на биосовместимость.
Каковы ключевые критерии выбора для различных областей применения в медицине?
Ключевые критерии выбора зависят от области применения, но включают в себя требования нормативных документов, уровни биосовместимости, классификацию чистых помещений, методы стерилизации, химическое воздействие и электрические характеристики: хирургическое оборудование требует наивысшей биосовместимости, фармацевтическое производство - химической стойкости, а диагностическое оборудование - электрической целостности, при этом для всех областей применения требуются соответствующие нормативные сертификаты и совместимость с чистящими средствами.
Различные медицинские приложения имеют уникальные требования, которые необходимо тщательно учитывать при выборе кабельного ввода, чтобы обеспечить оптимальную производительность и соответствие нормативным требованиям.
Хирургическое оборудование и оборудование для контакта с пациентами
Требования к прямому контакту: Биосовместимость USP Class VI с дополнительными испытаниями на цитотоксичность для материалов, находящихся в непосредственном контакте с пациентом во время хирургических операций.
Частота стерилизации: Способность выдерживать частые циклы стерилизации без разрушения, обычно требуются материалы, стабильные в течение сотен циклов стерилизации.
Электробезопасность: Повышенные требования к электробезопасности, включая низкий ток утечки и надежную изоляцию для оборудования, подключенного к пациенту.
Аварийная надежность: Критические требования к надежности оборудования для жизнеобеспечения и экстренной медицинской помощи, отказ которого может непосредственно повлиять на безопасность пациентов.
Фармацевтическое производство
Соответствие требованиям GMP: Требования надлежащей производственной практики, включая прослеживаемость материалов, контроль изменений и валидационную документацию.
Безопасность контакта с продуктом: Материалы, которые не загрязняют фармацевтическую продукцию в результате вымывания, образования частиц или химического взаимодействия.
Проверка чистоты: Широкие требования к валидации очистки с документированными процедурами и критериями приемки для фармацевтического производства.
Пакетная документация: Полное документирование партий и прослеживаемость материалов, используемых в фармацевтическом производстве.
Диагностическое и лабораторное оборудование
Требования к точности: Стабильность размеров и точность для аналитических приборов, требующих стабильных механических и электрических характеристик.
Химическая стойкость: Устойчивость к лабораторным химикатам, реагентам и чистящим растворителям, обычно используемым в диагностике.
Производительность EMC: Требования к электромагнитной совместимости чувствительных аналитических приборов и диагностического оборудования.
Стабильность калибровки: Механическая стабильность, которая не влияет на калибровку прибора и точность измерений с течением времени.
Производство медицинского оборудования
Валидация процесса: Материалы и компоненты, поддерживающие требования к валидации процессов при производстве медицинских изделий.
Системы качества: Интеграция с системами качества ISO 13485, включая квалификацию поставщиков и процедуры входного контроля.
Управление рисками: Материалы, поддерживающие требования по управлению рисками медицинских изделий, включая анализ режимов отказов и стратегии по снижению рисков.
Нормативно-правовая поддержка: Поддержка поставщиков при подаче регуляторных документов, включая техническую документацию и экспертизу регуляторных документов.
Матрица принятия решений по выбору
| Тип приложения | Первичные критерии | Вторичные критерии | Критические стандарты |
|---|---|---|---|
| Хирургическое оборудование | Биосовместимость | Стерилизация | USP Class VI, ISO 10993 |
| Фармацевтика | Химическая стойкость | Соблюдение требований GMP | FDA 21 CFR, cGMP |
| Диагностика | Точность | Производительность ЭМС | IEC 61326, ISO 15189 |
| Производство | Валидация процесса | Системы качества | ISO 13485, 21 CFR 820 |
Анализ затрат и выгод
Первоначальная стоимость по сравнению с жизненным циклом: Учитывайте общую стоимость владения, включая расходы на обслуживание, замену и соблюдение нормативных требований в течение всего срока службы оборудования.
Регуляторный риск: Соотносите материальные затраты с рисками, связанными с соблюдением нормативных требований, и потенциальными издержками, связанными с их несоблюдением.
Требования к производительности: Убедитесь, что выбранные материалы соответствуют минимальным эксплуатационным требованиям без излишней спецификации, которая неоправданно увеличивает расходы.
Возможности поставщика: Оценить возможности поставщиков по обеспечению постоянной поддержки, документации и помощи в соблюдении нормативных требований.
Заключение
Выбор кабельных вводов для медицинского оборудования и чистых помещений требует понимания уникальных нормативных требований, требований к материалам и эксплуатационным характеристикам, которые отличают эти приложения от стандартных промышленных применений. Успех зависит от баланса между биосовместимостью, чистотой, соответствием нормативным требованиям и электрическими характеристиками.
Ключ к надежной работе кабельных вводов медицинского назначения лежит в сотрудничестве с поставщиками, которые понимают требования к медицинскому оборудованию и могут предоставить соответствующие материалы, документацию и постоянную поддержку на протяжении всего жизненного цикла продукта. Компания Bepto специализируется на производстве кабельных вводов медицинского назначения, которые отвечают требованиям FDA и международным стандартам на медицинское оборудование, обеспечивая гарантию качества и нормативную поддержку, необходимую для критически важных приложений в здравоохранении.
Вопросы и ответы о медицинских кабельных вводах
В: Какие сертификаты необходимы для медицинских кабельных вводов?
A: Медицинские кабельные вводы обычно требуют сертификации биосовместимости USP Class VI, соответствия материалов требованиям FDA 21 CFR и системы качества производства ISO 13485. Конкретные требования зависят от области применения и нормативной юрисдикции.
В: Можно ли использовать обычные кабельные вводы из нержавеющей стали в медицинских целях?
A: Обычная нержавеющая сталь может не соответствовать медицинским требованиям. Для применения в медицине необходима медицинская нержавеющая сталь 316L с электрополированной отделкой, испытаниями на биосовместимость и надлежащей документацией для соблюдения нормативных требований.
В: Как очищать и стерилизовать медицинские кабельные вводы?
A: Следуйте утвержденным производителем процедурам очистки с использованием одобренных чистящих средств и методов стерилизации. Большинство медицинских сальников поддерживают автоклавирование паром, гамма-излучение или химическую стерилизацию при условии надлежащей совместимости материалов.
В: В чем разница между кабельными вводами чистого и медицинского класса?
A: Медицинский класс включает требования к биосовместимости и соответствие требованиям FDA, в то время как класс для чистых помещений фокусируется на контроле частиц и химической стойкости. В некоторых случаях требуются спецификации как для медицинских, так и для чистых помещений.
В: Как часто следует заменять медицинские кабельные сальники?
A: Частота замены зависит от циклов стерилизации, химического воздействия и рекомендаций производителя. Обычно проверяют после каждых 100-200 циклов стерилизации и заменяют на основании оценки состояния и требований валидации.
-
Узнайте о специфических тестах на биологическую реактивность, необходимых для сертификации по классу VI USP. ↩
-
Ознакомьтесь с обзором серии стандартов ISO 10993 по биологической оценке медицинских изделий. ↩
-
Ознакомьтесь с официальными руководствами и правилами FDA по текущей надлежащей производственной практике (cGMP). ↩
-
Ознакомьтесь с подробным руководством по стандартам ISO 14644 для классификации чистоты воздуха в чистых помещениях. ↩
-
Понять принципы паровой стерилизации, включая роль времени, температуры и давления. ↩



