As falhas na esterilização de dispositivos médicos custam milhões aos fabricantes anualmente, sendo que 15-20% das falhas são atribuídas a uma ventilação inadequada que impede a penetração correta do esterilizante. Os tampões de ventilação padrão falham sob autoclave1 temperaturas de 121-134°C ou degradam-se quando expostos a esterilização por óxido de etileno (ETO)2 produtos químicos, comprometendo a garantia de esterilidade e a conformidade regulamentar.
Os tampões de ventilação esterilizáveis permitem uma esterilização eficaz, permitindo a penetração de vapor ou gás ETO, mantendo as barreiras estéreis após a esterilização. Os orifícios de ventilação com membrana de PTFE suportam temperaturas de autoclave até 150°C e resistem à degradação química do ETO, assegurando uma manutenção fiável da esterilidade para dispositivos médicos, equipamento farmacêutico e instrumentos de laboratório que requerem processos de esterilização validados.
No ano passado, trabalhei com a Dra. Sarah Mitchell, diretora de qualidade de um importante fabricante de dispositivos médicos em Boston, que estava a ter falhas na validação da esterilização das suas embalagens de dispositivos implantáveis. Os seus tampões de ventilação de nylon padrão estavam a derreter durante os ciclos de autoclave e a bloquear a penetração adequada do vapor. Depois de mudarem para os nossos tampões de ventilação esterilizáveis em PTFE de grau farmacêutico com resistência validada à temperatura, alcançaram uma eficácia de esterilização 100% em 1.000 ciclos de validação - garantindo a conformidade com a FDA e a segurança dos pacientes! 🏥
Índice
- O que são tampões de ventilação esterilizáveis e porque é que são essenciais?
- Como é que os diferentes métodos de esterilização afectam os materiais dos tampões de ventilação?
- Que materiais são melhores para a esterilização em autoclave?
- Que materiais funcionam melhor para os processos de esterilização por ETO?
- Como selecionar e validar os tampões de ventilação esterilizáveis?
- Perguntas frequentes sobre tampões de ventilação esterilizáveis
O que são tampões de ventilação esterilizáveis e porque é que são essenciais?
Compreender o papel dos tampões de ventilação esterilizáveis no fabrico de dispositivos médicos e produtos farmacêuticos é essencial para manter a garantia de esterilidade e a conformidade regulamentar.
Os tampões de ventilação esterilizáveis são aberturas respiráveis especializadas, concebidas para resistir aos processos de esterilização, permitindo a penetração do esterilizante e mantendo as barreiras estéreis. Permitem a deslocação do ar durante a esterilização, evitam a formação de vácuo durante o arrefecimento e mantêm as condições estéreis após a esterilização. As aplicações críticas incluem embalagens de dispositivos médicos, contentores farmacêuticos, equipamento de laboratório e equipamento de processamento estéril.
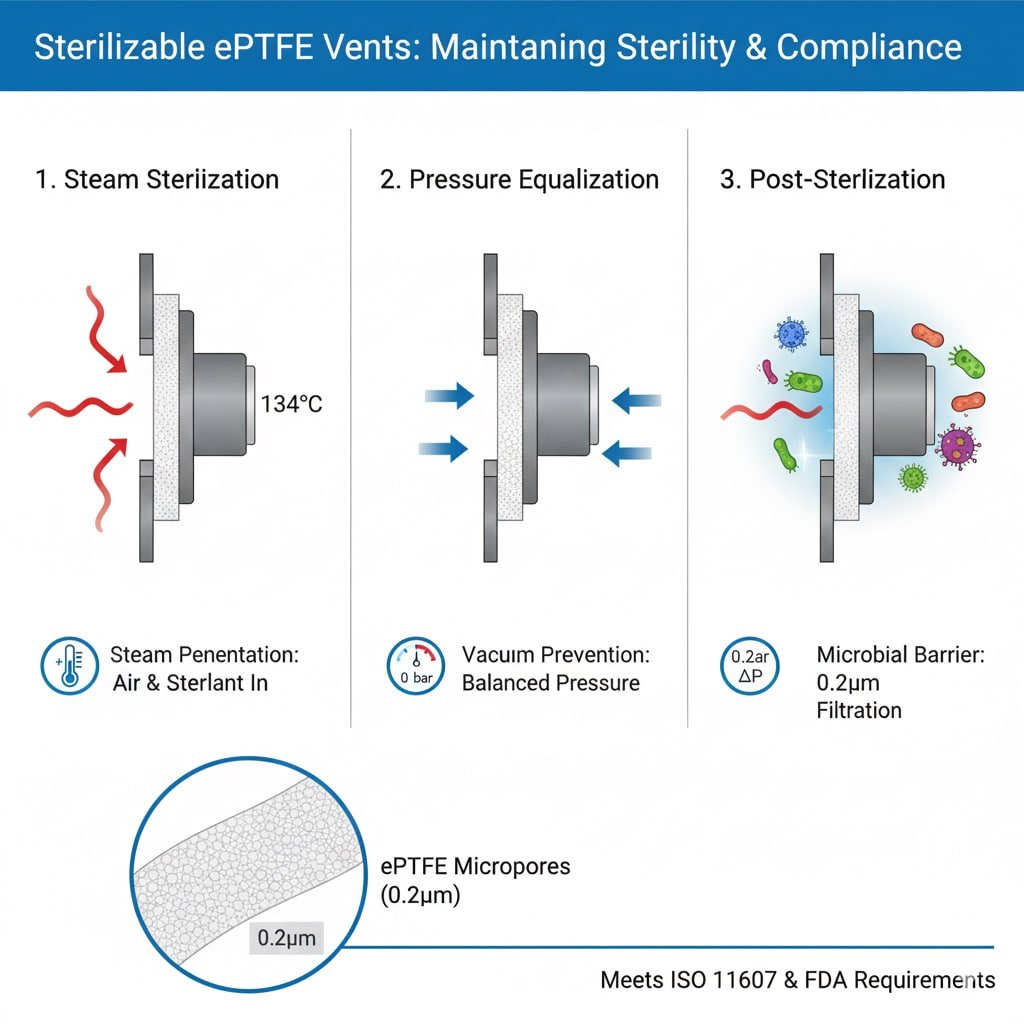
Requisitos do processo de esterilização
Penetração de vapor: A esterilização em autoclave requer que o vapor penetre na embalagem e entre em contacto com todas as superfícies, necessitando de aberturas que permitam o fluxo de gás, mantendo as barreiras microbianas.
Deslocamento de ar: Uma esterilização eficaz requer a remoção completa do ar e a sua substituição por esterilizante, o que os ventiladores facilitam através da troca controlada de gases.
Equalização da pressão: Os ciclos de esterilização criam diferenciais de pressão que os respiradouros devem acomodar sem comprometer as barreiras estéreis ou a integridade da embalagem.
Parâmetros críticos de desempenho
Resistência à temperatura: Os respiradouros esterilizáveis devem manter a integridade estrutural e o desempenho da filtragem a temperaturas de esterilização que variam entre 121°C e 150°C.
Compatibilidade química: Os materiais devem resistir à degradação dos produtos químicos de esterilização, incluindo vapor, óxido de etileno, peróxido de hidrogénio e ozono.
Eficiência da barreira microbiana: Após a esterilização, os respiradouros têm de proporcionar uma barreira microbiana3 com tamanhos de poros tipicamente de 0,2-0,22 microns para retenção de bactérias.
Considerações sobre a conformidade regulamentar
Requisitos de validação da FDA: As aplicações de dispositivos médicos requerem processos de esterilização validados com desempenho de ventilação documentado ao longo dos ciclos de esterilização.
Conformidade com as normas ISO: Os respiradouros esterilizáveis devem satisfazer ISO 116074 normas de embalagem e requisitos de esterilização a vapor ISO 17665 para aplicações médicas.
Testes de biocompatibilidade: As aplicações de contacto com dispositivos médicos podem exigir ensaios de biocompatibilidade USP Classe VI para garantir a segurança dos doentes.
Categorias de aplicação
Embalagem de dispositivos médicos: Embalagem esterilizada para implantes, instrumentos cirúrgicos e dispositivos médicos descartáveis que requerem manutenção da esterilidade até à sua utilização.
Fabrico de produtos farmacêuticos: Equipamento de processamento estéril, bioreactores e recipientes farmacêuticos que requerem processos de esterilização validados.
Equipamento de laboratório: Recipientes de laboratório autoclaváveis, recipientes de cultura e equipamento analítico que requerem condições estéreis para resultados exactos.
Como é que os diferentes métodos de esterilização afectam os materiais dos tampões de ventilação?
Os diferentes métodos de esterilização criam desafios únicos para os materiais dos tampões de ventilação, exigindo propriedades específicas do material e considerações de conceção para um desempenho ótimo.
A esterilização a vapor submete os materiais a temperaturas elevadas (121-134°C) e a condições de vapor saturado que podem causar degradação térmica, alterações dimensionais e danos nas membranas. A esterilização por ETO expõe os materiais a químicos reactivos a temperaturas mais baixas (37-63°C), mas com tempos de exposição mais longos que podem causar degradação química e libertação de gases. Cada método requer uma seleção específica de materiais para um desempenho fiável.
Efeitos da esterilização a vapor
Stress térmico: As temperaturas elevadas provocam a expansão térmica, a fusão potencial de componentes termoplásticos e a degradação de materiais sensíveis à temperatura.
Reacções de hidrólise5: A exposição ao vapor pode provocar a degradação hidrolítica de certos polímeros, nomeadamente os poliésteres e algumas poliamidas.
Estabilidade dimensional: Os ciclos térmicos repetidos podem causar alterações dimensionais que afectam o desempenho da vedação e a eficiência da filtragem.
Desafios da esterilização por ETO
Reatividade química: O óxido de etileno reage com materiais que contêm átomos de hidrogénio ativo, alterando potencialmente as propriedades do material e criando resíduos tóxicos.
Requisitos de emissão de gases: Os produtos esterilizados com ETO requerem períodos de arejamento prolongados para remover o ETO absorvido e os produtos de reação antes da utilização segura.
Caraterísticas de penetração: O ETO requer condições específicas de humidade e temperatura para uma penetração eficaz, o que afecta os requisitos de conceção da ventilação.
Efeitos do plasma de peróxido de hidrogénio
Degradação oxidativa: O plasma de H2O2 cria espécies altamente reactivas que podem degradar materiais orgânicos através de reacções de oxidação.
Compatibilidade de materiais: Muitos elastómeros e alguns plásticos são incompatíveis com a esterilização por plasma H2O2 devido à sua rápida degradação.
Benefícios a baixas temperaturas: A esterilização por plasma funciona a baixas temperaturas (45-55°C), reduzindo o stress térmico em materiais sensíveis à temperatura.
Considerações sobre a radiação gama
Danos por radiação: A radiação gama de alta energia pode provocar a cisão ou reticulação da cadeia polimérica, alterando significativamente as propriedades do material.
Acumulação de dose: A esterilização gama repetida pode causar danos cumulativos, limitando o número de ciclos de esterilização que os materiais podem suportar.
Necessidades em termos de antioxidantes: As formulações resistentes à radiação requerem frequentemente antioxidantes para evitar a degradação oxidativa durante e após a irradiação.
Recentemente, ajudei Ahmed Al-Rashid, diretor de operações de uma unidade farmacêutica no Dubai, a resolver problemas de validação da esterilização por ETO com os seus sistemas de ventilação de bioreactores. Os seus tampões de ventilação padrão estavam a absorver ETO e a exigir períodos de arejamento prolongados de 14 dias que perturbavam os programas de produção. Ao implementar os nossos tampões de ventilação de PTFE compatíveis com ETO com caraterísticas de absorção mínimas, reduziram o tempo de arejamento para 24 horas, mantendo a garantia de esterilidade total - melhorando drasticamente a eficiência da produção! 🚀
Que materiais são melhores para a esterilização em autoclave?
A seleção de materiais adequados para a esterilização em autoclave requer o conhecimento da estabilidade térmica, da resistência à hidrólise e do desempenho a longo prazo sob exposição repetida ao vapor.
O PTFE (politetrafluoroetileno) oferece um desempenho superior em autoclave com temperaturas de serviço contínuo até 260°C, excelente inércia química e resistência à hidrólise. O PVDF (fluoreto de polivinilideno) proporciona uma boa estabilidade térmica até 150°C com um custo inferior. Evite o nylon, o polietileno normal e a maioria dos elastómeros que se degradam em condições de autoclave, comprometendo o desempenho da filtragem e da vedação.
Vantagens da membrana PTFE
Resistência excecional à temperatura: O PTFE mantém a integridade estrutural e o desempenho de filtragem a temperaturas muito superiores às condições típicas de autoclave (121-134°C).
Inércia química: O PTFE resiste à degradação do vapor, dos produtos químicos de limpeza e dos subprodutos da esterilização, garantindo um desempenho consistente a longo prazo.
Propriedades hidrofóbicas: A natureza hidrofóbica do PTFE impede a absorção de água e mantém a estabilidade dimensional ao longo dos ciclos de esterilização.
Comparação do desempenho do material
| Material | Temperatura máxima (°C) | Resistência ao vapor | Resistência à hidrólise | Fator de custo |
|---|---|---|---|---|
| PTFE | 260 | Excelente | Excelente | Elevado |
| PVDF | 150 | Bom | Bom | Médio |
| PP (Polipropileno) | 135 | Justo | Justo | Baixa |
| Nylon | 80-100 | Pobres | Pobres | Baixa |
Seleção do material da caixa
Aço inoxidável 316L: Oferece uma excelente resistência à corrosão, estabilidade térmica e capacidade de limpeza para aplicações farmacêuticas e médicas que requerem procedimentos de limpeza validados.
PEEK (Poliéter-éter-cetona): Oferece uma estabilidade térmica excecional (utilização contínua até 250°C) com uma excelente resistência química para aplicações exigentes em autoclaves.
Polipropileno: Opção económica para aplicações de utilização única com desempenho adequado para ciclos normais de autoclave a 121°C.
Considerações sobre os componentes de vedação
O-Rings EPDM: Proporcionam uma boa resistência ao vapor e estabilidade térmica para temperaturas até 150°C com um excelente desempenho de vedação.
Vedantes de silicone: Oferecem uma resistência superior à temperatura (até 200°C), mas podem ter problemas de compatibilidade com determinados produtos químicos de limpeza.
O-Rings encapsulados em PTFE: Combinam a resistência química do PTFE com as propriedades de vedação do elastómero para aplicações exigentes que requerem ambas as caraterísticas de desempenho.
Otimização do design para utilização em autoclave
Alojamento de expansão térmica: Os projectos dos respiradouros devem ter em conta a expansão térmica diferencial entre os materiais para evitar falhas de vedação durante o ciclo de temperatura.
Caraterísticas de drenagem: A conceção adequada da drenagem evita a acumulação de condensado que pode comprometer o desempenho da filtragem ou criar riscos de contaminação.
Apoio à validação: As caraterísticas do projeto devem facilitar os ensaios de validação, incluindo a deterioração da pressão, o desafio microbiano e a verificação do desempenho térmico.
Que materiais funcionam melhor para os processos de esterilização por ETO?
A esterilização por ETO apresenta desafios únicos em termos de materiais, exigindo compatibilidade química, absorção mínima e caraterísticas de libertação rápida de gases para um processamento eficiente.
O PTFE e o PVDF oferecem uma excelente compatibilidade com o ETO, com uma absorção química mínima e libertação rápida de gases. Evite materiais com locais de hidrogénio ativo, como nylon, PVC e borracha natural, que reagem com o ETO formando compostos tóxicos. Os invólucros em aço inoxidável oferecem uma óptima resistência química, enquanto os vedantes em silicone oferecem uma boa compatibilidade com ETO com caraterísticas de libertação de gases aceitáveis para a maioria das aplicações.
Compatibilidade química com ETO
Mecanismos de reação: O ETO reage com materiais que contêm grupos hidroxilo, amino, carboxilo e sulfidrilo, formando derivados de etilenoglicol e outros compostos potencialmente tóxicos.
Caraterísticas de absorção: Os materiais com elevada absorção de ETO requerem períodos de arejamento prolongados, aumentando significativamente o tempo de processamento e os custos.
Cinética de emissão de gases: Os materiais de desgaseificação rápida permitem ciclos de arejamento mais curtos, melhorando a eficiência do processo e reduzindo os tempos de retenção do inventário.
Classificações de desempenho ETO de materiais
Excelente compatibilidade com ETO:
- PTFE: Absorção mínima, libertação rápida de gases, sem reatividade química
- PVDF: Baixa absorção, boa libertação de gases, excelente resistência química
- Aço inoxidável: Sem absorção, capacidade de utilização imediata
Boa compatibilidade com ETO:
- Polipropileno: Absorção moderada, libertação de gases aceitável
- Silicone: Baixa reatividade, requisitos moderados de libertação de gases
Fraca compatibilidade com ETO:
- Nylon: Reatividade elevada, é necessário um arejamento prolongado
- PVC: Degradação química, formação de compostos tóxicos
- Borracha natural: elevada absorção, potencial de degradação
Requisitos de tempo de arejamento
| Material | Tempo típico de arejamento | Nível de absorção de ETO | Taxa de desgaseificação |
|---|---|---|---|
| PTFE | 8-24 horas | Mínimo | Rápido |
| PVDF | 24-48 horas | Baixa | Bom |
| Polipropileno | 48-72 horas | Moderado | Moderado |
| Nylon | 7-14 dias | Elevado | Lento |
Otimização dos parâmetros do processo
Controlo da temperatura: A esterilização por ETO funciona normalmente a 37-63°C, exigindo materiais que mantenham o desempenho ao longo desta gama de temperaturas.
Requisitos de humidade: A eficácia do ETO requer uma humidade relativa de 40-80%, necessitando de materiais que funcionem consistentemente sob estas condições de humidade.
Gestão da concentração de gás: As concentrações de ETO de 450-1200 mg/L requerem materiais que resistam ao ataque químico, permitindo simultaneamente a penetração do esterilizante.
Considerações sobre a validação
Ensaios de resíduos: Os produtos esterilizados com ETO requerem testes para resíduos de ETO e produtos de reação para garantir a conformidade com os limites de segurança.
Manutenção da biocompatibilidade: Os materiais têm de manter a biocompatibilidade após a exposição e o arejamento por ETO, o que exige uma seleção de materiais validada.
Monitorização de processos: A esterilização por ETO requer a monitorização contínua da temperatura, humidade, pressão e concentração de gás durante todo o ciclo.
Como selecionar e validar os tampões de ventilação esterilizáveis?
A seleção e validação adequadas dos tampões de ventilação esterilizáveis garantem um desempenho de esterilização fiável, conformidade regulamentar e sucesso operacional a longo prazo.
A seleção requer a correspondência das propriedades do material com o método de esterilização, a definição dos requisitos de desempenho e a consideração das normas regulamentares. A validação envolve testes de desempenho térmico, estudos de desafio microbiano, avaliação da compatibilidade química e avaliação da estabilidade a longo prazo. Documentar todos os testes de acordo com as normas FDA e ISO para submissão regulamentar e conformidade do sistema de qualidade.
Quadro dos critérios de seleção
Compatibilidade com o método de esterilização: Adequar os materiais de ventilação aos métodos de esterilização específicos (vapor, ETO, plasma H2O2, gama) com base nos requisitos de resistência à temperatura, química e radiação.
Especificações de desempenho: Definir os caudais necessários, as classificações de pressão, a eficiência da filtragem e as propriedades de barreira microbiana com base nos requisitos da aplicação.
Requisitos regulamentares: Considere a classificação de dispositivos da FDA, a conformidade com as normas ISO e os requisitos de biocompatibilidade para as aplicações de utilização pretendida.
Parâmetros de avaliação da aplicação
Ambiente de funcionamento: Avaliar as gamas de temperatura, a exposição a produtos químicos, as condições de pressão e os riscos de contaminação ao longo do ciclo de vida do produto.
Frequência de esterilização: Considere a possibilidade de uma única utilização versus vários ciclos de esterilização e os efeitos cumulativos no desempenho e fiabilidade do material.
Âmbito de validação: Determinar os requisitos de ensaio com base na avaliação dos riscos, no percurso regulamentar e nos requisitos do sistema de qualidade.
Protocolo de ensaio de validação
Teste de desempenho térmico:
- Ciclo de temperatura em condições de esterilização
- Medição da estabilidade dimensional
- Verificação da eficiência da filtragem após exposição térmica
Testes de provocação microbiana:
- Desafio bacteriano com organismos de teste adequados
- Verificação da manutenção da esterilidade
- Avaliação da integridade da barreira a longo prazo
Avaliação da compatibilidade química:
- Avaliação da degradação dos materiais
- Ensaios de extractáveis e lixiviáveis
- Verificação da manutenção da biocompatibilidade
Requisitos de documentação
Especificações do material: Fichas de dados completas dos materiais, incluindo a composição química, as propriedades térmicas e as certificações regulamentares.
Protocolos de teste: Protocolos de validação pormenorizados que seguem as orientações da FDA e as normas ISO para a validação da esterilização.
Dados de desempenho: Resultados de testes abrangentes que demonstram o desempenho em todas as condições de funcionamento e ciclos de esterilização especificados.
Integração do sistema de qualidade
Qualificação de fornecedores: Estabelecer acordos de qualidade com fornecedores, incluindo rastreabilidade de materiais, controlo de alterações e requisitos de documentação de qualidade.
Inspeção de entrada: Desenvolver procedimentos de inspeção para a verificação das dimensões críticas, das propriedades dos materiais e das caraterísticas de desempenho.
Validação de processos: Integrar o desempenho do ventilador na validação geral do processo de esterilização, incluindo o teste do pior cenário possível.
Considerações sobre a gestão de riscos
Análise do modo de falha: Identificar potenciais modos de falha, incluindo degradação do material, falha do vedante e comprometimento da filtragem com estratégias de mitigação adequadas.
Controlo de alterações: Estabelecer procedimentos para gerir alterações de materiais, alterações de fornecedores e modificações de especificações com requisitos de revalidação adequados.
Monitorização contínua: Implementar programas de monitorização contínua para verificar o desempenho contínuo e identificar potenciais problemas antes que estes afectem a qualidade do produto.
Conclusão
Os tampões de ventilação esterilizáveis desempenham um papel fundamental na garantia de uma esterilização eficaz, mantendo barreiras estéreis em aplicações de dispositivos médicos e farmacêuticos. Compreender os desafios únicos dos diferentes métodos de esterilização e selecionar os materiais adequados é essencial para um desempenho fiável e conformidade regulamentar.
Os tampões de ventilação à base de PTFE oferecem um desempenho superior em vários métodos de esterilização, proporcionando uma excelente resistência à temperatura, compatibilidade química e fiabilidade a longo prazo. A seleção e validação adequadas garantem uma eficácia de esterilização óptima, minimizando o tempo e os custos de processamento.
Na Bepto, a nossa gama abrangente de tampões de ventilação esterilizáveis inclui membranas de PTFE de qualidade farmacêutica, desempenho validado em termos de temperatura e pacotes completos de documentação para submissões regulamentares. Com mais de uma década de experiência em aplicações de ventilação especializadas e capacidades de fabrico com certificação ISO, fornecemos as soluções fiáveis e económicas de que necessita para aplicações de esterilização críticas. Confie em nós para manter os seus processos de esterilização validados e os seus produtos seguros! 🔬
Perguntas frequentes sobre tampões de ventilação esterilizáveis
P: O mesmo bujão de ventilação pode ser utilizado para esterilização em autoclave e ETO?
A: Sim, os tampões de ventilação com membrana de PTFE podem lidar eficazmente com a esterilização por autoclave e por ETO. O PTFE oferece uma excelente resistência à temperatura para ciclos de autoclave e uma absorção mínima de ETO para um arejamento rápido, o que o torna ideal para instalações que utilizam vários métodos de esterilização.
P: Quantos ciclos de esterilização pode suportar um tampão de ventilação?
A: Os tampões de ventilação de PTFE de alta qualidade suportam normalmente mais de 100 ciclos de autoclave ou mais de 50 ciclos de ETO, mantendo o desempenho da filtração. A duração efectiva do ciclo depende dos parâmetros de esterilização, dos procedimentos de manuseamento e dos critérios de aceitação do desempenho para a sua aplicação específica.
Q: Que tamanho de poro é necessário para a filtragem estéril em aplicações médicas?
A: As aplicações médicas requerem normalmente tamanhos de poros de 0,2 ou 0,22 mícron para uma retenção bacteriana fiável. Este tamanho de poro fornece uma garantia de esterilidade validada, permitindo simultaneamente um fluxo de gás adequado para uma esterilização e equalização de pressão eficazes.
Q: Os tampões de ventilação esterilizáveis requerem testes de validação especiais?
A: Sim, os tampões de ventilação esterilizáveis requerem testes de validação, incluindo desempenho térmico, desafio microbiano e estudos de compatibilidade de materiais. Os testes devem seguir as orientações da FDA e as normas ISO, com documentação de apoio à validação do seu processo de esterilização e às submissões regulamentares.
P: Como é que se evita a contaminação do tampão de ventilação durante a esterilização?
A: Evite a contaminação através de uma instalação adequada, coberturas de proteção durante o manuseamento, parâmetros de esterilização validados e armazenamento adequado após a esterilização. Utilize uma técnica estéril durante a instalação e certifique-se de que os tampões de ventilação são concebidos para o seu método de esterilização e requisitos de aplicação específicos.
-
Aprenda os princípios científicos da esterilização em autoclave e como o vapor saturado sob pressão é utilizado para matar eficazmente os microrganismos. ↩
-
Explore o processo químico de esterilização por óxido de etileno (ETO), um método de baixa temperatura utilizado para esterilizar dispositivos médicos sensíveis ao calor e à humidade. ↩
-
Descubra os métodos utilizados para testar e validar a eficácia de uma barreira microbiana, garantindo que impede a entrada de microrganismos e mantém a esterilidade. ↩
-
Reveja os principais requisitos da norma ISO 11607, que especifica os materiais e os testes para sistemas de barreira estéril para dispositivos médicos. ↩
-
Compreender a reação química de hidrólise e como esta pode causar a degradação de certos materiais poliméricos quando expostos a água ou vapor a altas temperaturas. ↩



