A seleção incorrecta de bucins em ambientes médicos e de salas limpas causa riscos de contaminação, falhas de conformidade regulamentar e avarias no equipamento que resultam em riscos para a segurança dos doentes, encerramentos dispendiosos das instalações e violações da FDA, enquanto a vedação inadequada, os materiais inapropriados e a fraca capacidade de limpeza conduzem ao crescimento bacteriano, à contaminação por partículas e a violações da esterilidade que comprometem as operações críticas dos cuidados de saúde. Muitos gestores de instalações debatem-se com a seleção de bucins que cumpram as rigorosas normas médicas, mantendo um desempenho elétrico fiável.
A seleção de bucins para equipamento médico e salas limpas requer a compreensão dos regulamentos da FDA, USP Classe VI1 Os produtos da série IP68+ são compatíveis com os requisitos de material, as normas de vedação IP68+ e as necessidades de classificação de salas limpas, com uma construção em aço inoxidável de qualidade médica ou polímero especializado que proporciona biocompatibilidade, resistência química e superfícies lisas para uma limpeza e esterilização eficazes, mantendo a integridade eléctrica em aplicações críticas de cuidados de saúde. O sucesso depende do equilíbrio entre a conformidade regulamentar e a fiabilidade operacional.
Tendo trabalhado com engenheiros hospitalares em grandes centros médicos em Boston, fabricantes farmacêuticos na Suíça e instalações de salas limpas em Singapura, aprendi que os bucins de qualidade médica são essenciais para manter ambientes estéreis e garantir a segurança dos doentes. Deixe-me partilhar os conhecimentos essenciais para selecionar os bucins ideais para as suas aplicações médicas e de salas limpas.
Índice
- O que é que torna os bucins médicos diferentes dos bucins normais?
- Como é que cumpre os regulamentos da FDA e dos dispositivos médicos?
- Que materiais são necessários para aplicações em salas limpas?
- Como é que se garante uma compatibilidade adequada de limpeza e esterilização?
- Quais são os principais critérios de seleção para diferentes aplicações médicas?
- Perguntas frequentes sobre prensa-cabos médicos
O que é que torna os bucins médicos diferentes dos bucins normais?
Os bucins para cabos médicos diferem dos bucins normais pela utilização de materiais biocompatíveis, apresentando superfícies lisas e laváveis, cumprindo os regulamentos da FDA, proporcionando uma vedação melhorada para prevenção de contaminação e oferecendo resistência química a agentes de limpeza e processos de esterilização, com designs especializados que eliminam fendas onde as bactérias se podem alojar, mantendo o desempenho elétrico em ambientes críticos de cuidados de saúde.
Compreender estas diferenças é crucial porque as aplicações médicas têm requisitos regulamentares e de segurança únicos que os bucins industriais normais não conseguem satisfazer adequadamente.
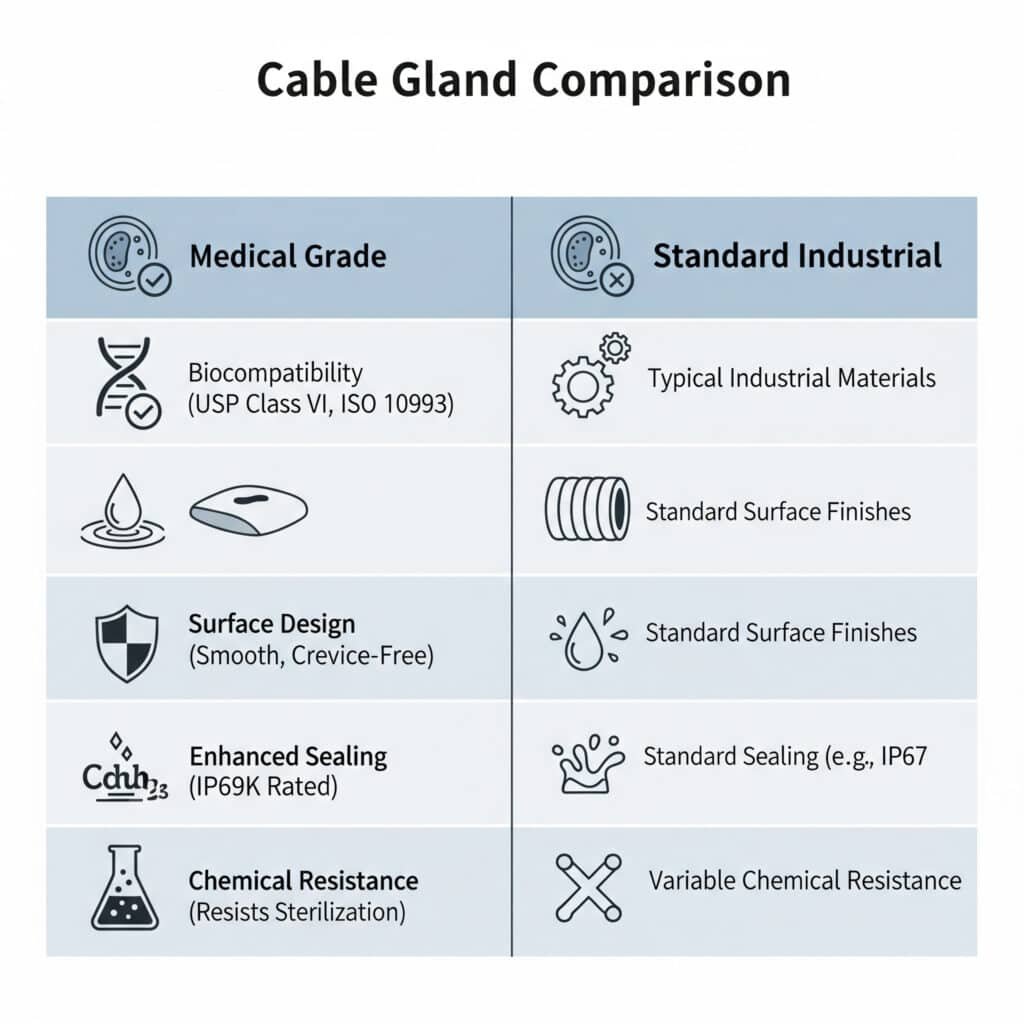
Requisitos de biocompatibilidade
Conformidade USP Classe VI: Os bucins para cabos médicos devem utilizar materiais que passem nos testes biológicos da Farmacopeia dos Estados Unidos da América de Classe VI para garantir a biocompatibilidade e a segurança em aplicações de dispositivos médicos.
Normas ISO 10993: Os materiais devem satisfazer ISO 109932 normas de avaliação biológica dos dispositivos médicos, garantindo a ausência de efeitos citotóxicos, sensibilizantes ou irritantes nos tecidos humanos.
Aprovação FDA 21 CFR 177: Os materiais de qualidade alimentar que cumprem os regulamentos da FDA para o contacto direto e indireto com os alimentos são frequentemente necessários para aplicações farmacêuticas e de dispositivos médicos.
Polímeros biocompatíveis: Materiais especializados como PEEK de grau médico, PTFE ou nylons de grau farmacêutico proporcionam biocompatibilidade sem comprometer as propriedades mecânicas.
Conceção da superfície para limpeza
Acabamento de superfície liso: As glândulas médicas apresentam superfícies ultra-lisas com valores Ra normalmente inferiores a 0,8 micrómetros para evitar a adesão de bactérias e permitir uma limpeza eficaz.
Conceção sem fendas: Eliminação de cantos afiados, roscas profundas e geometrias complexas que poderiam abrigar bactérias ou resistir a processos de limpeza e esterilização.
Arestas arredondadas: Todas as superfícies externas apresentam arestas arredondadas e transições suaves para facilitar a limpeza e evitar danos nas luvas de sala limpa ou nas embalagens esterilizadas.
Área de superfície mínima: Os designs simplificados minimizam a área de superfície exposta à contaminação, mantendo o desempenho mecânico e elétrico necessário.
Desempenho de vedação melhorado
Classificações IP68+: Proteção ambiental superior ao IP68 padrão, atingindo frequentemente o IP69K para aplicações de limpeza a alta pressão e alta temperatura.
Barreiras de contaminação: As várias fases de vedação impedem a entrada de partículas, bactérias e produtos químicos de limpeza que podem comprometer os ambientes estéreis.
Resistência à pressão: Classificações de pressão melhoradas para suportar procedimentos de limpeza agressivos e processos de esterilização sem falhas de vedação.
Fiabilidade a longo prazo: Os materiais de vedação mantêm a integridade através de ciclos de esterilização repetidos e da exposição a produtos químicos de limpeza agressivos.
Propriedades de resistência química
Compatibilidade com agentes de limpeza: Resistência a desinfectantes de qualidade hospitalar, compostos de amónio quaternário, peróxido de hidrogénio e outros produtos químicos de limpeza agressivos.
Resistência à esterilização: Os materiais resistem sem degradação à radiação gama, ao óxido de etileno, à autoclavagem a vapor e a outros métodos de esterilização.
Produtos químicos farmacêuticos: Resistência a solventes, ácidos, bases e compostos farmacêuticos normalmente encontrados em ambientes de fabrico médico.
Estabilidade de temperatura: Manter as propriedades através de ciclos de temperatura de esterilização e requisitos de controlo de temperatura de salas limpas.
David, gerente de instalações de uma grande fábrica farmacêutica em Nova Jersey, enfrentou problemas recorrentes de contaminação em suas linhas de enchimento estéreis, onde os prensa-cabos padrão estavam abrigando bactérias, apesar dos rigorosos protocolos de limpeza. Os prensa-cabos de latão existentes tinham padrões de rosca complexos e acabamentos de superfície que não podiam ser adequadamente esterilizados, levando a rejeições de lotes e preocupações com a conformidade com a FDA. Especificámos bucins de aço inoxidável de qualidade médica com superfícies electropolidas e designs sem fendas que cumpriam os requisitos da USP Classe VI. A atualização eliminou fontes de contaminação, alcançou uma eficácia de limpeza de 99,9% e ajudou a instalação a passar nas inspecções da FDA, reduzindo as taxas de rejeição de produtos em 85%. 😊
Como é que cumpre os regulamentos da FDA e dos dispositivos médicos?
O cumprimento dos regulamentos da FDA e dos dispositivos médicos exige a utilização de materiais com certificações adequadas, a manutenção de documentação detalhada, o cumprimento de Boas Práticas de Fabrico (BPF)3A FDA fornece uma gama completa de produtos, assegurando a rastreabilidade e implementando sistemas de qualidade que cumprem a 21 CFR Parte 820, com bucins de cabos médicos que requerem materiais aprovados pela FDA, testes de biocompatibilidade e controlos de fabrico que asseguram uma qualidade e segurança consistentes em aplicações de dispositivos médicos.
A conformidade regulamentar não é negociável em aplicações médicas, porque as falhas podem resultar em danos para os doentes, recolhas de produtos e consequências legais graves.
Requisitos de material da FDA
21 CFR Parte 177: Os materiais em contacto com produtos farmacêuticos ou dispositivos médicos devem cumprir os regulamentos de aditivos alimentares da FDA para substâncias em contacto indireto com os alimentos.
Ficheiro de acesso principal (MAF): Os fornecedores têm de manter ficheiros de acesso principal da FDA que documentem a segurança dos materiais, os processos de fabrico e os procedimentos de controlo de qualidade.
Ficheiro principal do medicamento (DMF): Para aplicações farmacêuticas, os materiais podem exigir o registo do Drug Master File com informações detalhadas sobre a composição e o fabrico.
Certificado de conformidade: Os fornecedores devem fornecer certificados que confirmem que os materiais cumprem todos os regulamentos e especificações aplicáveis da FDA.
Normas de qualidade para dispositivos médicos
Conformidade com a norma ISO 13485: O fabrico deve seguir os sistemas de gestão da qualidade dos dispositivos médicos ISO 13485 para a conceção, produção e vigilância pós-comercialização.
21 CFR Parte 820 (QSR): Conformidade com o Regulamento do Sistema de Qualidade, assegurando controlos de conceção adequados, controlo de documentos e acções corretivas/preventivas.
Gestão de riscos: Processos de gestão de riscos ISO 14971 para dispositivos médicos, incluindo análise de riscos, avaliação e medidas de controlo.
Controlos de conceção: Processos formais de controlo da conceção, incluindo planeamento da conceção, requisitos de entrada/saída, revisões, verificação e validação.

Documentação e rastreabilidade
Certificados de materiais: Rastreabilidade completa do material com certificados de análise, resultados de testes de biocompatibilidade e documentação de conformidade regulamentar.
Registos de fabrico: Registos de fabrico detalhados, incluindo parâmetros de processo, testes de controlo de qualidade e documentação de lotes para uma rastreabilidade total.
Controlo de alterações: Procedimentos formais de controlo de alterações para quaisquer modificações de materiais, processos ou especificações que afectem a conformidade regulamentar.
Qualificação de fornecedores: Programas abrangentes de qualificação de fornecedores que asseguram que todos os materiais e componentes cumprem os requisitos dos dispositivos médicos.
Requisitos de validação
Testes de biocompatibilidade: Testes USP Classe VI, incluindo testes de injeção sistémica, intracutâneos e de implantação para verificar a segurança biológica.
Validação da limpeza: Procedimentos de limpeza documentados com dados de validação que comprovam a remoção efectiva de contaminantes e a redução da carga biológica.
Validação da esterilização: Validação de processos de esterilização, incluindo mapeamento de doses, níveis de garantia de esterilidade e estudos de compatibilidade de materiais.
Teste de desempenho: Ensaios eléctricos, mecânicos e ambientais para verificar se o desempenho cumpre os requisitos dos dispositivos médicos ao longo do ciclo de vida do produto.
Apoio à apresentação de propostas regulamentares
Documentação 510(k): Documentação técnica de apoio às submissões da FDA 510(k) para dispositivos médicos que incorporam prensa-cabos.
Ficheiros técnicos: Ficheiros técnicos completos para a marcação CE ao abrigo do Regulamento de Dispositivos Médicos (MDR) nos mercados europeus.
Acordos de qualidade: Acordos formais de qualidade com fornecedores que definem responsabilidades, especificações e requisitos de conformidade.
Apoio à auditoria: Apoio a auditorias da FDA, de organismos notificados e de clientes, incluindo análise de documentação e inspecções de instalações.
Que materiais são necessários para aplicações em salas limpas?
As aplicações em salas limpas requerem materiais com propriedades de baixa libertação de gases, resistência à geração de partículas, compatibilidade química com agentes de limpeza, superfícies lisas e não porosas e níveis de condutividade adequados, com aço inoxidável 316L de qualidade médica, PEEK, PTFE e polímeros especializados aprovados para salas limpas que proporcionam um desempenho ótimo e cumprem ISO 146444 normas de salas limpas e manutenção da integridade eléctrica em ambientes controlados.
A seleção do material é crítica porque as salas limpas exigem um controlo rigoroso da contaminação molecular e de partículas que podem comprometer a qualidade do produto ou as condições de esterilização.
Requisitos de aço inoxidável
316L de grau médico: Aço inoxidável austenítico com baixo teor de carbono que proporciona uma resistência superior à corrosão e biocompatibilidade para aplicações médicas.
Acabamento electropolido: O electropolimento remove as imperfeições da superfície, reduz a produção de partículas e cria superfícies lisas para uma limpeza eficaz.
Tratamento de passivação: A passivação química aumenta a resistência à corrosão e remove a contaminação por ferro que poderia causar descoloração ou formação de partículas.
Rugosidade da superfície: Valores de Ra inferiores a 0,8 micrómetros (32 micropolegadas) minimizam a adesão bacteriana e facilitam os processos de limpeza e esterilização.
Polímeros de alto desempenho
PEEK (Poliéter-éter-cetona): A excelente resistência química, a baixa libertação de gases e a biocompatibilidade tornam o PEEK ideal para aplicações farmacêuticas e de dispositivos médicos.
PTFE (Politetrafluoroetileno): A inércia química superior e as propriedades antiaderentes proporcionam uma excelente resistência aos produtos químicos de limpeza e aos materiais biológicos.
Nylons de qualidade médica: Os nylons especialmente formulados com aprovação USP Classe VI oferecem boas propriedades mecânicas com biocompatibilidade para aplicações médicas.
POM aprovado para salas limpas: Polioximetileno com baixa produção de partículas e boa estabilidade dimensional para aplicações de precisão em salas limpas.
Compatibilidade com a classificação de salas limpas
ISO Classe 5 (Classe 100): Superfícies ultra-suaves com produção mínima de partículas para aplicações de fabrico de semicondutores e produtos farmacêuticos.
ISO Classe 6 (Classe 1000): Controlo moderado de partículas para o fabrico de dispositivos médicos e alguns processos farmacêuticos.
ISO Classe 7 (Classe 10000): Requisitos normalizados para salas limpas para operações gerais de montagem de produtos farmacêuticos e dispositivos médicos.
ISO Classe 8 (Classe 100000): Requisitos básicos de sala limpa para embalagens e alguns processos de fabrico de dispositivos médicos.
Controlo de desgaseificação e contaminação
Materiais de baixa emissão de gases: Materiais com emissões mínimas de compostos orgânicos voláteis (COV) que possam contaminar processos ou produtos sensíveis.
Contaminação molecular: Controlo de contaminantes moleculares, incluindo silicones, plastificantes e outros compostos orgânicos que possam afetar a qualidade do produto.
Contaminação iónica: Materiais com baixo teor iónico para evitar a contaminação de componentes electrónicos e produtos farmacêuticos.
Substâncias extraíveis: Mínimo de substâncias extraíveis que possam lixiviar para produtos farmacêuticos ou soluções de limpeza durante a utilização.
Matriz de compatibilidade química
| Agente de limpeza | AÇO INOXIDÁVEL 316L | PEEK | PTFE | Nylon médico |
|---|---|---|---|---|
| Álcool isopropílico | Excelente | Excelente | Excelente | Bom |
| Peróxido de hidrogénio | Excelente | Excelente | Excelente | Justo |
| Amónio quaternário | Excelente | Excelente | Excelente | Bom |
| Hipoclorito de sódio | Bom | Excelente | Excelente | Pobres |
| Ácido peracético | Bom | Excelente | Excelente | Pobres |
Hassan, que gere as operações de uma instalação farmacêutica de última geração na Suíça, precisava de atualizar os bucins na sua sala limpa ISO Classe 5 para o fabrico de injectáveis estéreis. Os bucins existentes estavam a gerar partículas durante os ciclos de limpeza e não conseguiam suportar os protocolos de esterilização agressivos necessários para os seus novos produtos biológicos. Fornecemos bucins em aço inoxidável 316L electropolido com baixa produção de partículas e compatibilidade química completa com os seus processos de limpeza e esterilização. A atualização alcançou contagens de partículas 90% abaixo dos limites da Classe 5 da ISO, eliminou eventos de contaminação relacionados à limpeza e apoiou a validação bem-sucedida de sua nova linha de fabricação estéril.
Como é que se garante uma compatibilidade adequada de limpeza e esterilização?
Assegurar a compatibilidade adequada de limpeza e esterilização requer a seleção de materiais que resistam à exposição repetida a produtos químicos de limpeza e métodos de esterilização, a conceção de superfícies para uma limpeza completa, a validação de procedimentos de limpeza e a manutenção de documentação detalhada, sendo que os bucins para cabos médicos requerem superfícies lisas e sem fendas, materiais resistentes a produtos químicos e protocolos de limpeza validados que atinjam os níveis de garantia de esterilidade necessários.
A compatibilidade da limpeza e da esterilização é essencial porque uma descontaminação inadequada pode levar à contaminação do produto, a riscos para a segurança dos doentes e a violações da regulamentação.
Compatibilidade do método de esterilização
Autoclavagem a vapor: Os materiais devem resistir a 121°C-134°C autoclavagem a vapor5 ciclos sem degradação, alterações dimensionais ou falhas de vedação.
Radiação gama: Resistência a doses de radiação gama de 25-50 kGy normalmente utilizadas para a esterilização de dispositivos médicos sem degradação do material.
Óxido de etileno (EtO): Compatibilidade química com a esterilização por EtO, incluindo resistência ao esterilizante e caraterísticas de desgaseificação adequadas.
Plasma de peróxido de hidrogénio: Compatibilidade com sistemas de esterilização por plasma a baixa temperatura, incluindo estabilidade do material e penetração completa do esterilizante.
Requisitos de validação da limpeza
Procedimentos de limpeza: Procedimentos de limpeza documentados que especificam os produtos químicos, as concentrações, os tempos de contacto e a ação mecânica necessários para uma descontaminação eficaz.
Protocolos de validação: Estudos formais de validação que demonstram a eficácia da limpeza utilizando os piores cenários de contaminação e testes analíticos.
Critérios de aceitação: Definição de critérios de aceitação de limpeza, incluindo inspeção visual, contagem de partículas, níveis de carga biológica e limites de resíduos químicos.
Monitorização de rotina: Programas de monitorização contínuos para verificar a eficácia da limpeza e identificar qualquer degradação do desempenho.
Considerações sobre o design da superfície
Caraterísticas de drenagem: Caraterísticas de conceção que promovam a drenagem completa das soluções de limpeza e evitem a formação de poças que possam abrigar contaminantes.
Acessibilidade: Todas as superfícies devem ser acessíveis para limpeza com os instrumentos e procedimentos de limpeza normais utilizados nas instalações médicas.
Requisitos de desmontagem: Considerar se os bucins têm de ser desmontados para limpeza ou se a limpeza intacta é suficiente para a aplicação.
Substituição da junta: Procedimentos para a substituição e validação de juntas quando os componentes de vedação requerem substituição periódica devido à exposição a produtos químicos de limpeza.
Documentação e conformidade
Instruções de limpeza: Instruções de limpeza pormenorizadas, incluindo procedimentos passo a passo, especificações químicas e precauções de segurança.
Dados de segurança do material: Informações completas sobre a segurança do material, incluindo compatibilidade química, limites de temperatura e compatibilidade de esterilização.
Relatórios de validação: Relatórios de validação de limpeza que demonstram a eficácia e estabelecem requisitos de monitorização de rotina.
Materiais de formação: Materiais de formação para o pessoal das instalações sobre os procedimentos corretos de limpeza, manuseamento e manutenção dos bucins de cabos médicos.
Testes de controlo de qualidade
Teste de carga biológica: Testes regulares de contaminação microbiana para verificar a eficácia da limpeza e identificar potenciais áreas problemáticas.
Teste de endotoxinas: Testes de endotoxinas bacterianas que podem causar reacções pirogénicas em aplicações farmacêuticas e de dispositivos médicos.
Contagem de partículas: Testes de contagem de partículas para verificar se os requisitos da sala limpa são mantidos após as actividades de limpeza e manutenção.
Análise de resíduos químicos: Testes de resíduos químicos de limpeza que possam contaminar os produtos ou afetar a biocompatibilidade.
Quais são os principais critérios de seleção para diferentes aplicações médicas?
Os principais critérios de seleção variam consoante a aplicação, mas incluem requisitos de conformidade regulamentar, níveis de biocompatibilidade, classificações de salas limpas, métodos de esterilização, exposição a produtos químicos e necessidades de desempenho elétrico, com o equipamento cirúrgico a exigir a mais elevada biocompatibilidade, o fabrico de produtos farmacêuticos a necessitar de resistência química e o equipamento de diagnóstico a centrar-se na integridade eléctrica, enquanto todas as aplicações exigem certificações regulamentares adequadas e compatibilidade de limpeza.
As diferentes aplicações médicas têm requisitos únicos que devem ser cuidadosamente considerados durante a seleção do bucim para garantir um desempenho ótimo e a conformidade regulamentar.
Equipamento cirúrgico e de contacto com o paciente
Requisitos de contacto direto: Biocompatibilidade USP Classe VI com testes adicionais de citotoxicidade para materiais em contacto direto com o doente durante procedimentos cirúrgicos.
Frequência de esterilização: Capacidade de suportar ciclos de esterilização frequentes sem degradação, exigindo normalmente materiais estáveis durante centenas de ciclos de esterilização.
Segurança eléctrica: Requisitos de segurança eléctrica melhorados, incluindo baixa corrente de fuga e isolamento fiável para equipamento ligado a doentes.
Fiabilidade de emergência: Requisitos críticos de fiabilidade para equipamento de suporte de vida e equipamento médico de emergência em que uma falha pode ter um impacto direto na segurança dos doentes.
Fabrico de produtos farmacêuticos
Conformidade com as BPF: Requisitos de boas práticas de fabrico, incluindo rastreabilidade dos materiais, controlo de alterações e documentação de validação.
Segurança no contacto com o produto: Materiais que não contaminam os produtos farmacêuticos através de lixiviação, formação de partículas ou interação química.
Validação da limpeza: Requisitos alargados de validação de limpeza com procedimentos documentados e critérios de aceitação para o fabrico de produtos farmacêuticos.
Documentação do lote: Documentação completa dos lotes e rastreabilidade dos materiais utilizados no equipamento de fabrico de produtos farmacêuticos.
Equipamento de diagnóstico e de laboratório
Requisitos de precisão: Estabilidade dimensional e precisão para instrumentos analíticos que exigem um desempenho mecânico e elétrico consistente.
Resistência química: Resistência a produtos químicos de laboratório, reagentes e solventes de limpeza normalmente utilizados em aplicações de diagnóstico.
Desempenho EMC: Requisitos de compatibilidade electromagnética para instrumentos analíticos sensíveis e equipamento de diagnóstico.
Estabilidade da calibração: Estabilidade mecânica que não afecta a calibração do instrumento ou a precisão da medição ao longo do tempo.
Fabrico de dispositivos médicos
Validação de processos: Materiais e componentes que suportam os requisitos de validação de processos para o fabrico de dispositivos médicos.
Sistemas de qualidade: Integração com sistemas de qualidade ISO 13485, incluindo qualificação de fornecedores e procedimentos de inspeção de entrada.
Gestão de riscos: Materiais que apoiam os requisitos de gestão do risco dos dispositivos médicos, incluindo a análise do modo de falha e estratégias de atenuação.
Apoio regulamentar: Apoio do fornecedor para submissões regulamentares, incluindo documentação técnica e conhecimentos regulamentares.
Matriz de decisão de seleção
| Tipo de aplicação | Critérios primários | Critérios secundários | Normas críticas |
|---|---|---|---|
| Equipamento cirúrgico | Biocompatibilidade | Esterilização | USP Classe VI, ISO 10993 |
| Farmacêutico | Resistência química | Conformidade com as BPF | FDA 21 CFR, cGMP |
| Diagnóstico | Precisão | Desempenho EMC | IEC 61326, ISO 15189 |
| Fabrico | Validação do processo | Sistemas de qualidade | ISO 13485, 21 CFR 820 |
Análise custo-benefício
Custo inicial vs. ciclo de vida: Considerar o custo total de propriedade, incluindo os custos de manutenção, substituição e conformidade ao longo da vida útil do equipamento.
Risco regulamentar: Equilibrar os custos materiais em relação aos riscos de conformidade regulamentar e aos potenciais custos de não conformidade.
Requisitos de desempenho: Assegurar que os materiais selecionados cumprem os requisitos mínimos de desempenho sem especificações excessivas que aumentem desnecessariamente os custos.
Capacidades do fornecedor: Avaliar as capacidades do fornecedor para apoio contínuo, documentação e assistência à conformidade regulamentar.
Conclusão
A seleção de bucins para equipamento médico e salas limpas requer a compreensão dos requisitos regulamentares, materiais e de desempenho únicos que distinguem estas aplicações das utilizações industriais normais. O sucesso depende do equilíbrio entre a biocompatibilidade, a capacidade de limpeza, a conformidade regulamentar e o desempenho elétrico.
A chave para um desempenho fiável dos bucins médicos reside no trabalho com fornecedores que compreendem os regulamentos relativos aos dispositivos médicos e que podem fornecer materiais adequados, documentação e apoio contínuo ao longo do ciclo de vida do produto. Na Bepto, somos especializados em prensa-cabos de grau médico que cumprem os requisitos da FDA e as normas internacionais para dispositivos médicos, fornecendo a garantia de qualidade e o apoio regulamentar necessários para aplicações críticas de cuidados de saúde.
Perguntas frequentes sobre prensa-cabos médicos
P: Que certificações são necessárias para os bucins de cabos médicos?
A: Os bucins médicos requerem normalmente certificação de biocompatibilidade USP Classe VI, conformidade com a norma FDA 21 CFR para materiais e sistemas de qualidade de fabrico ISO 13485. Os requisitos específicos dependem da sua aplicação e jurisdição regulamentar.
P: Os bucins de aço inoxidável normais podem ser utilizados em aplicações médicas?
A: O aço inoxidável normal pode não cumprir os requisitos médicos. As aplicações médicas necessitam de aço inoxidável 316L de qualidade médica com acabamento electropolido, testes de biocompatibilidade e documentação adequada para conformidade regulamentar.
P: Como é que limpo e esterilizo os bucins de cabos médicos?
A: Siga os procedimentos de limpeza validados pelo fabricante, utilizando agentes de limpeza e métodos de esterilização aprovados. A maioria das glândulas médicas suporta autoclavagem a vapor, radiação gama ou esterilização química com compatibilidade de material adequada.
P: Qual é a diferença entre os bucins para salas limpas e para uso médico?
A: O grau médico inclui requisitos de biocompatibilidade e conformidade com a FDA, enquanto o grau de sala limpa se centra no controlo de partículas e na resistência química. Algumas aplicações requerem especificações médicas e de sala limpa.
P: Com que frequência devem ser substituídos os bucins de cabos médicos?
A: A frequência de substituição depende dos ciclos de esterilização, da exposição química e das recomendações do fabricante. Normalmente, inspecionar após cada 100-200 ciclos de esterilização e substituir com base na avaliação do estado e nos requisitos de validação.
-
Saiba mais sobre os testes específicos de reatividade biológica necessários para a certificação USP Classe VI. ↩
-
Aceda a uma visão geral da série de normas ISO 10993 para a avaliação biológica de dispositivos médicos. ↩
-
Reveja as diretrizes e regulamentos oficiais da FDA para as Boas Práticas de Fabrico Actuais (cGMP). ↩
-
Explore um guia detalhado das normas ISO 14644 para classificar a limpeza do ar em salas limpas. ↩
-
Compreender os princípios da esterilização a vapor, incluindo o papel do tempo, da temperatura e da pressão. ↩



