Awarie sterylizacji urządzeń medycznych kosztują producentów miliony rocznie, a 15-20% awarii przypisuje się nieodpowiedniej wentylacji, która uniemożliwia prawidłową penetrację środka sterylizującego. Standardowe zatyczki wentylacyjne zawodzą pod autoklaw1 w temperaturach 121-134°C lub ulegają degradacji po wystawieniu na działanie sterylizacja tlenkiem etylenu (ETO)2 chemikaliów, zagrażając zapewnieniu sterylności i zgodności z przepisami.
Nadające się do sterylizacji korki odpowietrzające umożliwiają skuteczną sterylizację poprzez umożliwienie penetracji pary lub gazu ETO przy jednoczesnym zachowaniu sterylnych barier po sterylizacji. Otwory wentylacyjne z membraną PTFE wytrzymują temperatury autoklawu do 150°C i są odporne na degradację chemiczną ETO, zapewniając niezawodne utrzymanie sterylności urządzeń medycznych, sprzętu farmaceutycznego i instrumentów laboratoryjnych wymagających zatwierdzonych procesów sterylizacji.
W ubiegłym roku współpracowałem z dr Sarah Mitchell, dyrektorem ds. jakości w wiodącej firmie produkującej urządzenia medyczne w Bostonie, która doświadczała niepowodzeń w zakresie walidacji sterylizacji opakowań urządzeń do implantacji. Ich standardowe nylonowe korki wentylacyjne topiły się podczas cykli autoklawowania i blokowały prawidłową penetrację pary. Po przejściu na nasze sterylizowalne korki wentylacyjne PTFE klasy farmaceutycznej o potwierdzonej odporności na temperaturę, osiągnęli skuteczność sterylizacji 100% w 1000 cykli walidacji - zapewniając zgodność z FDA i bezpieczeństwo pacjentów! 🏥
Spis treści
- Czym są sterylizowalne korki odpowietrzające i dlaczego są tak ważne?
- Jak różne metody sterylizacji wpływają na materiały korków odpowietrzających?
- Które materiały są najlepsze do sterylizacji w autoklawie?
- Jakie materiały najlepiej sprawdzają się w procesach sterylizacji ETO?
- Jak wybrać i zweryfikować sterylizowalne korki odpowietrzające?
- Najczęściej zadawane pytania dotyczące sterylizowalnych zatyczek wentylacyjnych
Czym są sterylizowalne korki odpowietrzające i dlaczego są tak ważne?
Zrozumienie roli sterylizowalnych korków odpowietrzających w produkcji wyrobów medycznych i farmaceutycznych jest niezbędne do zapewnienia sterylności i zgodności z przepisami.
Sterylizowalne zatyczki wentylacyjne to specjalistyczne, oddychające otwory wentylacyjne zaprojektowane tak, aby wytrzymać procesy sterylizacji, jednocześnie umożliwiając penetrację środka sterylizującego i utrzymując sterylne bariery. Umożliwiają wypieranie powietrza podczas sterylizacji, zapobiegają tworzeniu się próżni podczas chłodzenia i utrzymują sterylne warunki po sterylizacji. Krytyczne zastosowania obejmują opakowania urządzeń medycznych, pojemniki farmaceutyczne, sprzęt laboratoryjny i sprzęt do sterylizacji.
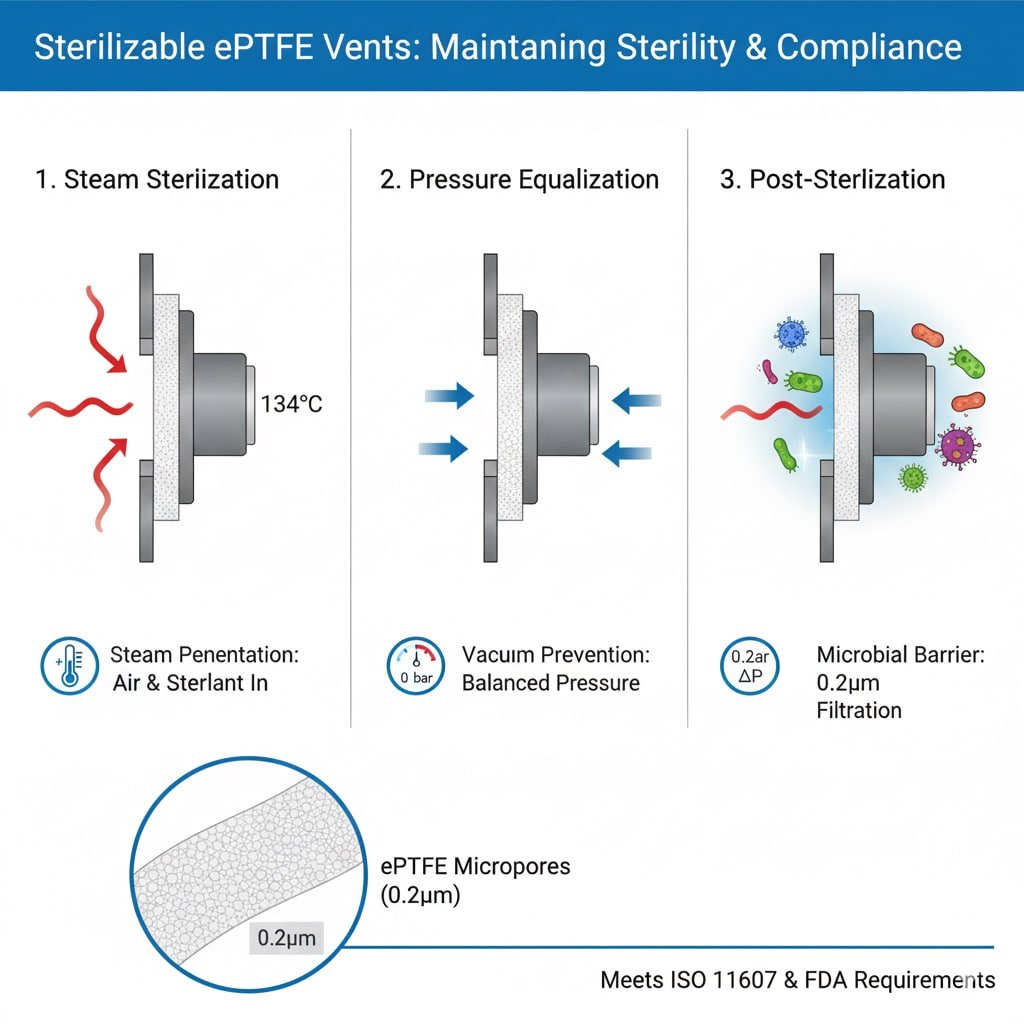
Wymagania dotyczące procesu sterylizacji
Penetracja pary: Sterylizacja w autoklawie wymaga przenikania pary przez opakowanie i kontaktu ze wszystkimi powierzchniami, co wymaga otworów wentylacyjnych umożliwiających przepływ gazu przy jednoczesnym zachowaniu barier mikrobiologicznych.
Wyporność powietrza: Skuteczna sterylizacja wymaga całkowitego usunięcia powietrza i zastąpienia go środkiem sterylizującym, co otwory wentylacyjne ułatwiają poprzez kontrolowaną wymianę gazową.
Wyrównanie ciśnienia: Cykle sterylizacji wytwarzają różnice ciśnień, które muszą być dostosowane do otworów wentylacyjnych bez naruszania barier sterylnych lub integralności opakowania.
Krytyczne parametry wydajności
Odporność na temperaturę: Nadające się do sterylizacji otwory wentylacyjne muszą zachowywać integralność strukturalną i wydajność filtracji w temperaturach sterylizacji od 121°C do 150°C.
Kompatybilność chemiczna: Materiały muszą być odporne na degradację pod wpływem chemikaliów do sterylizacji, w tym pary, tlenku etylenu, nadtlenku wodoru i ozonu.
Skuteczność bariery mikrobiologicznej: Po sterylizacji otwory wentylacyjne muszą zapewniać niezawodne bariera mikrobiologiczna3 z porami o wielkości zazwyczaj 0,2-0,22 mikrona do zatrzymywania bakterii.
Zgodność z przepisami
Wymagania walidacyjne FDA: Zastosowania urządzeń medycznych wymagają zatwierdzonych procesów sterylizacji z udokumentowaną wydajnością odpowietrzania przez cały cykl sterylizacji.
Zgodność z normami ISO: Sterylizowalne otwory wentylacyjne muszą spełniać ISO 116074 standardy pakowania i wymagania dotyczące sterylizacji parowej ISO 17665 dla zastosowań medycznych.
Testy biokompatybilności: Zastosowania kontaktowe urządzeń medycznych mogą wymagać testów biokompatybilności USP klasy VI w celu zapewnienia bezpieczeństwa pacjentów.
Kategorie aplikacji
Opakowania na urządzenia medyczne: Sterylne opakowania na implanty, narzędzia chirurgiczne i jednorazowe wyroby medyczne wymagające zachowania sterylności do momentu użycia.
Produkcja farmaceutyczna: Sprzęt do sterylnego przetwarzania, bioreaktory i pojemniki farmaceutyczne wymagające zatwierdzonych procesów sterylizacji.
Sprzęt laboratoryjny: Autoklawowalne pojemniki laboratoryjne, naczynia hodowlane i sprzęt analityczny wymagający sterylnych warunków dla uzyskania dokładnych wyników.
Jak różne metody sterylizacji wpływają na materiały korków odpowietrzających?
Różne metody sterylizacji stwarzają unikalne wyzwania dla materiałów korków odpowietrzających, wymagając określonych właściwości materiału i rozważań projektowych w celu uzyskania optymalnej wydajności.
Sterylizacja parowa poddaje materiały działaniu wysokiej temperatury (121-134°C) i nasyconej pary wodnej, co może powodować degradację termiczną, zmiany wymiarów i uszkodzenia membran. Sterylizacja ETO wystawia materiały na działanie reaktywnych chemikaliów w niższych temperaturach (37-63°C), ale przy dłuższym czasie ekspozycji, co może powodować degradację chemiczną i odgazowywanie. Każda metoda wymaga specjalnego doboru materiałów w celu zapewnienia niezawodnego działania.
Efekty sterylizacji parowej
Naprężenie termiczne: Wysokie temperatury powodują rozszerzalność cieplną, potencjalne topnienie elementów termoplastycznych i degradację materiałów wrażliwych na temperaturę.
Reakcje hydrolizy5: Ekspozycja na parę wodną może powodować hydrolityczną degradację niektórych polimerów, w szczególności poliestrów i niektórych poliamidów.
Stabilność wymiarowa: Powtarzające się cykle termiczne mogą powodować zmiany wymiarów, które wpływają na wydajność uszczelnienia i skuteczność filtracji.
Wyzwania związane ze sterylizacją ETO
Reaktywność chemiczna: Tlenek etylenu reaguje z materiałami zawierającymi aktywne atomy wodoru, potencjalnie zmieniając właściwości materiału i tworząc toksyczne pozostałości.
Wymagania dotyczące odgazowywania: Produkty sterylizowane ETO wymagają dłuższych okresów napowietrzania w celu usunięcia wchłoniętego ETO i produktów reakcji przed bezpiecznym użyciem.
Charakterystyka penetracji: ETO wymaga określonych warunków wilgotności i temperatury dla skutecznej penetracji, wpływając na wymagania projektowe wentylacji.
Działanie plazmy nadtlenku wodoru
Degradacja oksydacyjna: Plazma H2O2 tworzy wysoce reaktywne gatunki, które mogą rozkładać materiały organiczne poprzez reakcje utleniania.
Kompatybilność materiałowa: Wiele elastomerów i niektóre tworzywa sztuczne są niekompatybilne ze sterylizacją plazmową H2O2 z powodu szybkiej degradacji.
Korzyści w niskich temperaturach: Sterylizacja plazmowa działa w niskich temperaturach (45-55°C), zmniejszając obciążenie termiczne materiałów wrażliwych na temperaturę.
Uwagi dotyczące promieniowania gamma
Uszkodzenia spowodowane promieniowaniem: Wysokoenergetyczne promieniowanie gamma może powodować rozszczepienie łańcucha polimerowego lub sieciowanie, znacząco zmieniając właściwości materiału.
Kumulacja dawki: Wielokrotna sterylizacja promieniami gamma może powodować skumulowane uszkodzenia, ograniczając liczbę cykli sterylizacji, które mogą wytrzymać materiały.
Wymagania dotyczące przeciwutleniaczy: Preparaty odporne na promieniowanie często wymagają przeciwutleniaczy, aby zapobiec degradacji oksydacyjnej podczas i po napromieniowaniu.
Niedawno pomogłem Ahmedowi Al-Rashidowi, kierownikowi operacyjnemu w zakładzie farmaceutycznym w Dubaju, rozwiązać problemy związane z walidacją sterylizacji ETO w ich systemach odpowietrzania bioreaktorów. Ich standardowe korki odpowietrzające pochłaniały ETO i wymagały wydłużonych 14-dniowych okresów napowietrzania, które zakłócały harmonogramy produkcji. Dzięki wdrożeniu naszych kompatybilnych z ETO korków odpowietrzających z PTFE o minimalnych właściwościach absorpcyjnych, skrócono czas napowietrzania do 24 godzin przy jednoczesnym zachowaniu pełnej sterylności - znacznie poprawiając wydajność produkcji! 🚀
Które materiały są najlepsze do sterylizacji w autoklawie?
Wybór odpowiednich materiałów do sterylizacji w autoklawie wymaga zrozumienia stabilności termicznej, odporności na hydrolizę i długoterminowej wydajności przy wielokrotnej ekspozycji na parę.
PTFE (politetrafluoroetylen) oferuje doskonałą wydajność autoklawu z ciągłymi temperaturami pracy do 260°C, doskonałą obojętność chemiczną i odporność na hydrolizę. PVDF (polifluorek winylidenu) zapewnia dobrą stabilność termiczną do 150°C przy niższych kosztach. Unikaj nylonu, standardowego polietylenu i większości elastomerów, które ulegają degradacji w warunkach autoklawu, pogarszając wydajność filtracji i uszczelniania.
Zalety membran PTFE
Wyjątkowa odporność na temperaturę: PTFE zachowuje integralność strukturalną i wydajność filtracji w temperaturach znacznie przekraczających typowe warunki autoklawu (121-134°C).
Obojętność chemiczna: PTFE jest odporny na degradację przez parę, chemikalia czyszczące i produkty uboczne sterylizacji, zapewniając stałą, długoterminową wydajność.
Właściwości hydrofobowe: Hydrofobowa natura PTFE zapobiega wchłanianiu wody i utrzymuje stabilność wymiarową podczas cykli sterylizacji.
Porównanie wydajności materiałów
| Materiał | Maksymalna temperatura (°C) | Odporność na parę | Odporność na hydrolizę | Współczynnik kosztów |
|---|---|---|---|---|
| PTFE | 260 | Doskonały | Doskonały | Wysoki |
| PVDF | 150 | Dobry | Dobry | Średni |
| PP (polipropylen) | 135 | Uczciwy | Uczciwy | Niski |
| Nylon | 80-100 | Słaby | Słaby | Niski |
Wybór materiału obudowy
Stal nierdzewna 316L: Zapewnia doskonałą odporność na korozję, stabilność termiczną i łatwość czyszczenia w zastosowaniach farmaceutycznych i medycznych wymagających sprawdzonych procedur czyszczenia.
PEEK (polieteroeteroketon): Oferuje wyjątkową stabilność termiczną (praca ciągła do 250°C) i doskonałą odporność chemiczną do wymagających zastosowań w autoklawach.
Polipropylen: Ekonomiczna opcja do zastosowań jednorazowych z odpowiednią wydajnością dla standardowych cykli autoklawu w temperaturze 121°C.
Rozważania dotyczące elementów uszczelniających
O-ringi z EPDM: Zapewniają dobrą odporność na parę wodną i stabilność termiczną w temperaturach do 150°C oraz doskonałe właściwości uszczelniające.
Uszczelki silikonowe: Oferują doskonałą odporność na temperaturę (do 200°C), ale mogą mieć problemy z kompatybilnością z niektórymi chemikaliami czyszczącymi.
O-ringi w obudowie PTFE: Połączenie odporności chemicznej PTFE z właściwościami uszczelniającymi elastomeru dla wymagających zastosowań wymagających obu cech wydajności.
Optymalizacja konstrukcji pod kątem użytkowania w autoklawie
Rozszerzalność cieplna Zakwaterowanie: Konstrukcje odpowietrzników muszą uwzględniać różnicę rozszerzalności cieplnej między materiałami, aby zapobiec uszkodzeniu uszczelnienia podczas cyklicznych zmian temperatury.
Cechy drenażu: Odpowiednia konstrukcja drenażu zapobiega gromadzeniu się kondensatu, który mógłby pogorszyć wydajność filtracji lub stworzyć ryzyko zanieczyszczenia.
Wsparcie walidacji: Cechy konstrukcyjne powinny ułatwiać przeprowadzanie testów walidacyjnych, w tym testów zaniku ciśnienia, testów mikrobiologicznych i weryfikacji wydajności termicznej.
Jakie materiały najlepiej sprawdzają się w procesach sterylizacji ETO?
Sterylizacja ETO wiąże się z wyjątkowymi wyzwaniami materiałowymi wymagającymi kompatybilności chemicznej, minimalnej absorpcji i szybkiego odgazowywania w celu wydajnego przetwarzania.
PTFE i PVDF oferują doskonałą kompatybilność z ETO przy minimalnej absorpcji chemicznej i szybkim odgazowywaniu. Należy unikać materiałów z aktywnymi miejscami wodorowymi, takich jak nylon, PVC i kauczuk naturalny, które reagują z ETO, tworząc toksyczne związki. Obudowy ze stali nierdzewnej zapewniają optymalną odporność chemiczną, podczas gdy uszczelki silikonowe oferują dobrą kompatybilność z ETO przy akceptowalnej charakterystyce odgazowywania dla większości zastosowań.
Kompatybilność chemiczna ETO
Mechanizmy reakcji: ETO reaguje z materiałami zawierającymi grupy hydroksylowe, aminowe, karboksylowe i sulfhydrylowe, tworząc pochodne glikolu etylenowego i inne potencjalnie toksyczne związki.
Charakterystyka absorpcji: Materiały o wysokiej absorpcji ETO wymagają wydłużonych okresów napowietrzania, co znacznie wydłuża czas przetwarzania i zwiększa koszty.
Kinetyka odgazowywania: Szybko odgazowujące się materiały umożliwiają krótsze cykle napowietrzania, poprawiając wydajność procesu i skracając czas przechowywania zapasów.
Istotne rankingi wydajności ETO
Doskonała kompatybilność z ETO:
- PTFE: Minimalna absorpcja, szybkie odgazowywanie, brak reaktywności chemicznej
- PVDF: Niska absorpcja, dobre odgazowywanie, doskonała odporność chemiczna
- Stal nierdzewna: Brak absorpcji, możliwość natychmiastowego użycia
Dobra kompatybilność z ETO:
- Polipropylen: Umiarkowana absorpcja, dopuszczalne odgazowywanie
- Silikon: Niska reaktywność, umiarkowane wymagania dotyczące odgazowywania
Słaba kompatybilność z ETO:
- Nylon: Wysoka reaktywność, wymagane dłuższe napowietrzanie
- PVC: degradacja chemiczna, tworzenie toksycznych związków
- Kauczuk naturalny: wysoka absorpcja, potencjalna degradacja
Wymagania dotyczące czasu napowietrzania
| Materiał | Typowy czas napowietrzania | Poziom absorpcji ETO | Szybkość odgazowywania |
|---|---|---|---|
| PTFE | 8-24 godzin | Minimalny | Szybki |
| PVDF | 24-48 godzin | Niski | Dobry |
| Polipropylen | 48-72 godzin | Umiarkowany | Umiarkowany |
| Nylon | 7-14 dni | Wysoki | Powolny |
Optymalizacja parametrów procesu
Kontrola temperatury: Sterylizacja ETO zwykle działa w temperaturze 37-63°C, co wymaga materiałów, które zachowują wydajność w tym zakresie temperatur.
Wymagania dotyczące wilgotności: Skuteczność ETO wymaga wilgotności względnej 40-80%, co wymaga materiałów, które działają konsekwentnie w takich warunkach wilgotności.
Zarządzanie stężeniem gazu: Stężenia ETO wynoszące 450-1200 mg/l wymagają materiałów, które są odporne na atak chemiczny, a jednocześnie umożliwiają penetrację środka sterylizującego.
Rozważania dotyczące walidacji
Testowanie pozostałości: Produkty sterylizowane ETO wymagają testów na obecność pozostałości ETO i produktów reakcji w celu zapewnienia zgodności z limitami bezpieczeństwa.
Utrzymanie biokompatybilności: Materiały muszą zachować biokompatybilność po ekspozycji na ETO i napowietrzaniu, co wymaga zatwierdzonego wyboru materiału.
Monitorowanie procesów: Sterylizacja ETO wymaga ciągłego monitorowania temperatury, wilgotności, ciśnienia i stężenia gazu podczas całego cyklu.
Jak wybrać i zweryfikować sterylizowalne korki odpowietrzające?
Właściwy dobór i walidacja sterylizowalnych korków odpowietrzających zapewnia niezawodną wydajność sterylizacji, zgodność z przepisami i długoterminowy sukces operacyjny.
Wybór wymaga dopasowania właściwości materiału do metody sterylizacji, określenia wymagań dotyczących wydajności i uwzględnienia norm prawnych. Walidacja obejmuje testy termiczne, badania mikrobiologiczne, ocenę kompatybilności chemicznej i ocenę stabilności długoterminowej. Wszystkie testy należy udokumentować zgodnie z normami FDA i ISO w celu uzyskania zgodności z przepisami i systemem jakości.
Ramy kryteriów wyboru
Kompatybilność metody sterylizacji: Dopasowanie materiałów wentylacyjnych do określonych metod sterylizacji (para, ETO, plazma H2O2, promieniowanie gamma) w oparciu o wymagania dotyczące temperatury, odporności chemicznej i odporności na promieniowanie.
Specyfikacje wydajności: Zdefiniuj wymagane natężenia przepływu, wartości znamionowe ciśnienia, skuteczność filtracji i właściwości bariery mikrobiologicznej w oparciu o wymagania aplikacji.
Wymogi regulacyjne: Weź pod uwagę klasyfikację urządzeń FDA, zgodność z normami ISO i wymagania dotyczące biokompatybilności dla zamierzonych zastosowań.
Parametry oceny aplikacji
Środowisko operacyjne: Ocena zakresów temperatur, narażenia chemicznego, warunków ciśnieniowych i ryzyka zanieczyszczenia w całym cyklu życia produktu.
Częstotliwość sterylizacji: Rozważ jednorazowe lub wielokrotne cykle sterylizacji i łączny wpływ na wydajność i niezawodność materiału.
Zakres walidacji: Określenie wymagań testowych na podstawie oceny ryzyka, ścieżki regulacyjnej i wymagań systemu jakości.
Protokół testów walidacyjnych
Testowanie wydajności cieplnej:
- Cykliczne zmiany temperatury w warunkach sterylizacji
- Pomiar stabilności wymiarowej
- Weryfikacja skuteczności filtracji po ekspozycji termicznej
Testy na obecność drobnoustrojów:
- Prowokacja bakteryjna odpowiednimi organizmami testowymi
- Weryfikacja utrzymania sterylności
- Długoterminowa ocena integralności bariery
Ocena kompatybilności chemicznej:
- Ocena degradacji materiału
- Testowanie substancji ekstrahowalnych i wymywalnych
- Weryfikacja utrzymania biokompatybilności
Wymagania dotyczące dokumentacji
Specyfikacja materiałowa: Kompletne arkusze danych materiałowych, w tym skład chemiczny, właściwości termiczne i certyfikaty regulacyjne.
Protokoły testowe: Szczegółowe protokoły walidacji zgodne z wytycznymi FDA i normami ISO dotyczącymi walidacji sterylizacji.
Dane dotyczące wydajności: Kompleksowe wyniki testów wykazujące wydajność w określonych warunkach pracy i cyklach sterylizacji.
Integracja systemu jakości
Kwalifikacja dostawcy: Ustanowienie umów dotyczących jakości dostawców, w tym identyfikowalności materiałów, kontroli zmian i wymagań dotyczących dokumentacji jakościowej.
Inspekcja przychodząca: Opracowanie procedur kontroli krytycznych wymiarów, właściwości materiałów i weryfikacji charakterystyki działania.
Walidacja procesu: Włączenie wydajności odpowietrznika do ogólnej walidacji procesu sterylizacji, w tym testowanie najgorszego scenariusza.
Rozważania dotyczące zarządzania ryzykiem
Analiza trybów awarii: Zidentyfikować potencjalne tryby awarii, w tym degradację materiału, awarię uszczelnienia i pogorszenie filtracji wraz z odpowiednimi strategiami łagodzącymi.
Kontrola zmian: Ustanowienie procedur zarządzania zmianami materiałów, zmianami dostawców i modyfikacjami specyfikacji wraz z odpowiednimi wymogami dotyczącymi ponownej walidacji.
Ciągłe monitorowanie: Wdrożenie bieżących programów monitorowania w celu weryfikacji ciągłej wydajności i identyfikacji potencjalnych problemów, zanim wpłyną one na jakość produktu.
Wnioski
Sterylizowalne korki odpowietrzające odgrywają kluczową rolę w zapewnieniu skutecznej sterylizacji przy jednoczesnym zachowaniu sterylnych barier w urządzeniach medycznych i zastosowaniach farmaceutycznych. Zrozumienie unikalnych wyzwań związanych z różnymi metodami sterylizacji i wybór odpowiednich materiałów ma zasadnicze znaczenie dla niezawodnego działania i zgodności z przepisami.
Korki odpowietrzające na bazie PTFE oferują doskonałą wydajność w wielu metodach sterylizacji, zapewniając doskonałą odporność na temperaturę, kompatybilność chemiczną i długoterminową niezawodność. Właściwy dobór i walidacja zapewniają optymalną skuteczność sterylizacji przy jednoczesnej minimalizacji czasu i kosztów przetwarzania.
W Bepto nasza kompleksowa oferta sterylizowalnych korków odpowietrzających obejmuje membrany PTFE klasy farmaceutycznej, zweryfikowaną wydajność temperaturową i kompletne pakiety dokumentacji do składania wniosków regulacyjnych. Dzięki ponad dziesięcioletniemu doświadczeniu w specjalistycznych zastosowaniach wentylacyjnych i możliwościom produkcyjnym z certyfikatem ISO, zapewniamy niezawodne, opłacalne rozwiązania potrzebne do krytycznych zastosowań sterylizacyjnych. Zaufaj nam, aby zapewnić walidację procesów sterylizacji i bezpieczeństwo produktów! 🔬
Najczęściej zadawane pytania dotyczące sterylizowalnych zatyczek wentylacyjnych
P: Czy ten sam korek odpowietrzający może być używany zarówno do sterylizacji w autoklawie, jak i ETO?
A: Tak, korki odpowietrzające z membraną PTFE mogą skutecznie obsługiwać zarówno sterylizację w autoklawie, jak i ETO. PTFE oferuje doskonałą odporność na temperaturę w cyklach autoklawowych i minimalną absorpcję ETO w celu szybkiego napowietrzania, co czyni go idealnym rozwiązaniem dla obiektów stosujących wiele metod sterylizacji.
P: Ile cykli sterylizacji może wytrzymać korek odpowietrzający?
A: Wysokiej jakości korki odpowietrzające z PTFE zazwyczaj wytrzymują ponad 100 cykli sterylizacji w autoklawie lub ponad 50 cykli ETO przy zachowaniu wydajności filtracji. Rzeczywista żywotność zależy od parametrów sterylizacji, procedur obsługi i kryteriów akceptacji wydajności dla konkretnego zastosowania.
P: Jaki rozmiar porów jest wymagany do sterylnej filtracji w zastosowaniach medycznych?
A: Zastosowania medyczne zazwyczaj wymagają porów o wielkości 0,2 lub 0,22 mikrona w celu niezawodnego zatrzymywania bakterii. Ten rozmiar porów zapewnia potwierdzoną sterylność, umożliwiając jednocześnie odpowiedni przepływ gazu w celu skutecznej sterylizacji i wyrównania ciśnienia.
P: Czy sterylizowalne korki odpowietrzające wymagają specjalnych testów walidacyjnych?
A: Tak, sterylizowalne korki odpowietrzające wymagają testów walidacyjnych, w tym testów termicznych, testów mikrobiologicznych i badań kompatybilności materiałowej. Testy muszą być zgodne z wytycznymi FDA i normami ISO, z dokumentacją potwierdzającą walidację procesu sterylizacji i zgłoszenia do organów regulacyjnych.
P: Jak zapobiec zanieczyszczeniu korka odpowietrzającego podczas sterylizacji?
A: Zapobiegaj skażeniu poprzez prawidłową instalację, osłony ochronne podczas obsługi, zatwierdzone parametry sterylizacji i odpowiednie przechowywanie po sterylizacji. Podczas instalacji należy stosować sterylną technikę i upewnić się, że korki odpowietrzające są zaprojektowane dla konkretnej metody sterylizacji i wymagań aplikacji.
-
Poznaj naukowe zasady sterylizacji w autoklawie i dowiedz się, w jaki sposób nasycona para wodna pod ciśnieniem jest wykorzystywana do skutecznego zabijania mikroorganizmów. ↩
-
Zapoznaj się z procesem chemicznym sterylizacji tlenkiem etylenu (ETO), metodą niskotemperaturową stosowaną do sterylizacji wrażliwych na ciepło i wilgoć urządzeń medycznych. ↩
-
Odkryj metody stosowane do testowania i walidacji skuteczności bariery mikrobiologicznej, zapewniając, że zapobiega ona wnikaniu mikroorganizmów i utrzymuje sterylność. ↩
-
Zapoznaj się z kluczowymi wymaganiami normy ISO 11607, która określa materiały i testy dla sterylnych systemów barierowych dla urządzeń medycznych. ↩
-
Zrozumienie reakcji chemicznej hydrolizy i tego, w jaki sposób może ona powodować degradację niektórych materiałów polimerowych pod wpływem wody lub pary wodnej w wysokich temperaturach. ↩



