Niewłaściwy dobór dławików kablowych w środowiskach medycznych i pomieszczeniach czystych powoduje ryzyko zanieczyszczenia, naruszenia zgodności z przepisami i awarie sprzętu, które skutkują zagrożeniem bezpieczeństwa pacjentów, kosztownymi przestojami placówek i naruszeniami FDA, podczas gdy nieodpowiednie uszczelnienie, nieodpowiednie materiały i słaba łatwość czyszczenia prowadzą do rozwoju bakterii, zanieczyszczenia cząstkami stałymi i naruszenia sterylności, które zagrażają krytycznym operacjom opieki zdrowotnej. Wielu kierowników placówek zmaga się z wyborem dławnic spełniających rygorystyczne normy medyczne przy jednoczesnym zachowaniu niezawodnej wydajności elektrycznej.
Wybór dławików kablowych do sprzętu medycznego i pomieszczeń czystych wymaga zrozumienia przepisów FDA, USP Klasa VI1 Wymagania materiałowe, normy szczelności IP68+ i potrzeby klasyfikacji pomieszczeń czystych, ze stalą nierdzewną klasy medycznej lub specjalistyczną konstrukcją polimerową zapewniającą biokompatybilność, odporność chemiczną i gładkie powierzchnie do skutecznego czyszczenia i sterylizacji przy jednoczesnym zachowaniu integralności elektrycznej w krytycznych zastosowaniach opieki zdrowotnej. Sukces zależy od zrównoważenia zgodności z przepisami z niezawodnością operacyjną.
Współpracując z inżynierami szpitalnymi w głównych ośrodkach medycznych w Bostonie, producentami farmaceutycznymi w Szwajcarii i obiektami do pomieszczeń czystych w Singapurze, nauczyłem się, że dławiki kablowe klasy medycznej są niezbędne do utrzymania sterylnego środowiska i zapewnienia bezpieczeństwa pacjentów. Pozwolę sobie podzielić się kluczową wiedzą na temat wyboru optymalnych dławnic do zastosowań medycznych i w pomieszczeniach czystych.
Spis treści
- Czym medyczne dławnice kablowe różnią się od standardowych dławnic?
- Jak spełnić wymogi FDA i przepisy dotyczące urządzeń medycznych?
- Jakie materiały są wymagane do zastosowań w pomieszczeniach czystych?
- Jak zapewnić odpowiednie czyszczenie i sterylizację?
- Jakie są kluczowe kryteria wyboru dla różnych zastosowań medycznych?
- Najczęściej zadawane pytania dotyczące dławików kablowych
Czym medyczne dławnice kablowe różnią się od standardowych dławnic?
Medyczne dławiki kablowe różnią się od standardowych dławików zastosowaniem biokompatybilnych materiałów, gładkimi powierzchniami do czyszczenia, zgodnością z przepisami FDA, lepszym uszczelnieniem w celu zapobiegania zanieczyszczeniom oraz odpornością chemiczną na środki czyszczące i procesy sterylizacji, ze specjalnymi konstrukcjami, które eliminują szczeliny, w których mogą gromadzić się bakterie, przy jednoczesnym zachowaniu wydajności elektrycznej w krytycznych środowiskach opieki zdrowotnej.
Zrozumienie tych różnic ma kluczowe znaczenie, ponieważ zastosowania medyczne mają unikalne wymogi bezpieczeństwa i regulacyjne, których standardowe dławnice przemysłowe nie są w stanie odpowiednio spełnić.
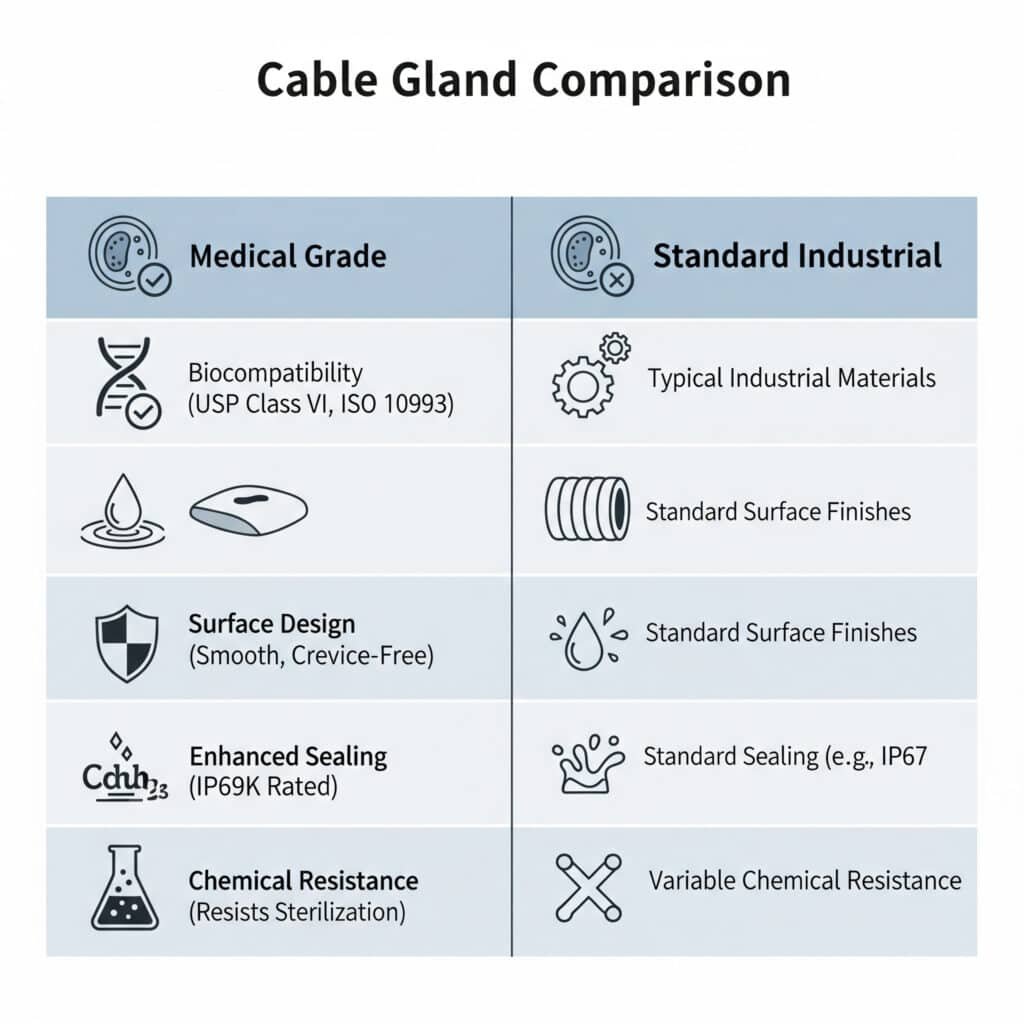
Wymagania dotyczące biokompatybilności
Zgodność z USP Klasa VI: Dławiki kabli medycznych muszą być wykonane z materiałów, które przeszły testy biologiczne klasy VI Farmakopei Stanów Zjednoczonych pod kątem biokompatybilności i bezpieczeństwa w zastosowaniach związanych z urządzeniami medycznymi.
Normy ISO 10993: Materiały muszą spełniać ISO 109932 standardy oceny biologicznej dla urządzeń medycznych, zapewniające brak cytotoksycznego, uczulającego lub drażniącego wpływu na tkanki ludzkie.
Zatwierdzenie FDA 21 CFR 177: Materiały przeznaczone do kontaktu z żywnością, spełniające wymogi FDA dotyczące bezpośredniego i pośredniego kontaktu z żywnością, są często wymagane w zastosowaniach farmaceutycznych i medycznych.
Biokompatybilne polimery: Specjalistyczne materiały, takie jak PEEK klasy medycznej, PTFE lub nylony klasy farmaceutycznej, zapewniają biokompatybilność bez pogarszania właściwości mechanicznych.
Konstrukcja powierzchni zapewniająca łatwość czyszczenia
Gładkie wykończenie powierzchni: Dławnice medyczne mają bardzo gładkie powierzchnie o wartości Ra zazwyczaj poniżej 0,8 mikrometra, co zapobiega przyleganiu bakterii i umożliwia skuteczne czyszczenie.
Konstrukcja bez szczelin: Eliminacja ostrych narożników, głębokich gwintów i złożonych geometrii, które mogą być siedliskiem bakterii lub być odporne na procesy czyszczenia i sterylizacji.
Zaokrąglone krawędzie: Wszystkie powierzchnie zewnętrzne mają zaokrąglone krawędzie i gładkie przejścia, aby ułatwić czyszczenie i zapobiec uszkodzeniu rękawic do pomieszczeń czystych lub sterylnych opakowań.
Minimalna powierzchnia: Usprawnione konstrukcje minimalizują powierzchnię narażoną na zanieczyszczenia, zachowując jednocześnie niezbędną wydajność mechaniczną i elektryczną.
Zwiększona wydajność uszczelniania
Stopień ochrony IP68+: Doskonała ochrona środowiska wykraczająca poza standardowe IP68, często osiągająca IP69K w zastosowaniach wymagających czyszczenia pod wysokim ciśnieniem i w wysokiej temperaturze.
Bariery zanieczyszczeń: Wiele etapów uszczelniania zapobiega przedostawaniu się cząstek, bakterii i chemikaliów czyszczących, które mogłyby zagrozić sterylnemu środowisku.
Odporność na ciśnienie: Zwiększone ciśnienie znamionowe pozwala wytrzymać agresywne procedury czyszczenia i sterylizacji bez uszkodzenia uszczelnienia.
Długoterminowa niezawodność: Materiały uszczelniające zachowują integralność podczas wielokrotnych cykli sterylizacji i ekspozycji na ostre chemikalia czyszczące.
Właściwości odporności chemicznej
Kompatybilność ze środkami czyszczącymi: Odporność na szpitalne środki dezynfekujące, czwartorzędowe związki amoniowe, nadtlenek wodoru i inne agresywne chemikalia czyszczące.
Odporność na sterylizację: Materiały są odporne na promieniowanie gamma, tlenek etylenu, autoklawowanie parowe i inne metody sterylizacji bez degradacji.
Chemikalia farmaceutyczne: Odporność na rozpuszczalniki, kwasy, zasady i związki farmaceutyczne powszechnie występujące w środowisku produkcji medycznej.
Stabilność temperaturowa: Zachowanie właściwości dzięki cyklom temperatur sterylizacji i wymogom kontroli temperatury w pomieszczeniach czystych.
David, kierownik zakładu w dużej fabryce farmaceutycznej w New Jersey, stanął w obliczu powtarzających się problemów z zanieczyszczeniem na sterylnych liniach napełniania, gdzie standardowe dławiki kablowe były siedliskiem bakterii pomimo rygorystycznych protokołów czyszczenia. Istniejące mosiężne dławnice miały złożone wzory gwintów i wykończenia powierzchni, których nie można było odpowiednio wysterylizować, co prowadziło do odrzucania partii i obaw o zgodność z FDA. Określiliśmy dławnice kablowe ze stali nierdzewnej klasy medycznej z elektropolerowanymi powierzchniami i konstrukcjami bez szczelin, które spełniały wymagania USP klasy VI. Modernizacja wyeliminowała źródła zanieczyszczeń, osiągnęła skuteczność czyszczenia na poziomie 99,9% i pomogła zakładowi przejść inspekcje FDA, jednocześnie zmniejszając współczynnik odrzucania produktów o 85%. 😊
Jak spełnić wymogi FDA i przepisy dotyczące urządzeń medycznych?
Spełnienie wymogów FDA i przepisów dotyczących urządzeń medycznych wymaga stosowania materiałów z odpowiednimi certyfikatami, prowadzenia szczegółowej dokumentacji, przestrzegania Dobre praktyki produkcyjne (GMP)3Zapewnienie identyfikowalności i wdrożenie systemów jakości zgodnych z 21 CFR część 820, z medycznymi dławikami kablowymi wymagającymi materiałów zatwierdzonych przez FDA, testów biokompatybilności i kontroli produkcji, które zapewniają stałą jakość i bezpieczeństwo w zastosowaniach urządzeń medycznych.
Zgodność z przepisami nie podlega negocjacjom w zastosowaniach medycznych, ponieważ awarie mogą skutkować szkodami dla pacjentów, wycofaniem produktu z rynku i poważnymi konsekwencjami prawnymi.
Wymagania materiałowe FDA
21 CFR część 177: Materiały mające kontakt z farmaceutykami lub urządzeniami medycznymi muszą spełniać przepisy FDA dotyczące dodatków do żywności dla substancji mających pośredni kontakt z żywnością.
Główny plik dostępu (MAF): Dostawcy muszą prowadzić FDA Master Access Files dokumentujące bezpieczeństwo materiałów, procesy produkcyjne i procedury kontroli jakości.
Główny plik leku (DMF): W przypadku zastosowań farmaceutycznych materiały mogą wymagać rejestracji w Drug Master File ze szczegółowymi informacjami o składzie i produkcji.
Certyfikat zgodności: Dostawcy muszą dostarczyć certyfikaty potwierdzające, że materiały spełniają wszystkie obowiązujące przepisy i specyfikacje FDA.
Standardy jakości wyrobów medycznych
Zgodność z normą ISO 13485: Produkcja musi być zgodna z systemem zarządzania jakością wyrobów medycznych ISO 13485 w zakresie projektowania, produkcji i nadzoru po wprowadzeniu do obrotu.
21 CFR część 820 (QSR): Zgodność z przepisami dotyczącymi systemu jakości zapewniająca odpowiednią kontrolę projektu, kontrolę dokumentów i działania naprawcze / zapobiegawcze.
Zarządzanie ryzykiem: ISO 14971 - procesy zarządzania ryzykiem dla wyrobów medycznych, w tym analiza, ocena i środki kontroli ryzyka.
Kontrola projektu: Formalne procesy kontroli projektu, w tym planowanie projektu, wymagania wejściowe/wyjściowe, przeglądy, weryfikacja i walidacja.

Dokumentacja i identyfikowalność
Certyfikaty materiałowe: Pełna identyfikowalność materiałów z certyfikatami analizy, wynikami testów biokompatybilności i dokumentacją zgodności z przepisami.
Ewidencja produkcji: Szczegółowa dokumentacja produkcyjna, w tym parametry procesu, testy kontroli jakości i dokumentacja partii dla pełnej identyfikowalności.
Kontrola zmian: Formalne procedury kontroli zmian dla wszelkich modyfikacji materiałów, procesów lub specyfikacji mających wpływ na zgodność z przepisami.
Kwalifikacja dostawcy: Kompleksowe programy kwalifikacji dostawców zapewniające, że wszystkie materiały i komponenty spełniają wymagania dotyczące urządzeń medycznych.
Wymagania dotyczące walidacji
Testy biokompatybilności: Testy USP klasy VI, w tym testy wstrzyknięć ogólnoustrojowych, śródskórnych i implantacji w celu weryfikacji bezpieczeństwa biologicznego.
Walidacja czyszczenia: Udokumentowane procedury czyszczenia z danymi walidacyjnymi potwierdzającymi skuteczne usuwanie zanieczyszczeń i redukcję obciążenia biologicznego.
Walidacja sterylizacji: Walidacja procesów sterylizacji, w tym mapowanie dawek, poziomy zapewnienia sterylności i badania kompatybilności materiałów.
Testowanie wydajności: Testy elektryczne, mechaniczne i środowiskowe w celu sprawdzenia, czy wydajność spełnia wymagania dotyczące urządzeń medycznych w całym cyklu życia produktu.
Wsparcie przy składaniu wniosków regulacyjnych
Dokumentacja 510(k): Dokumentacja techniczna wspierająca zgłoszenia FDA 510(k) dla urządzeń medycznych zawierających dławiki kablowe.
Pliki techniczne: Kompleksowa dokumentacja techniczna do oznakowania CE zgodnie z rozporządzeniem w sprawie wyrobów medycznych (MDR) na rynkach europejskich.
Umowy dotyczące jakości: Formalne umowy jakościowe z dostawcami określające obowiązki, specyfikacje i wymogi zgodności.
Wsparcie audytu: Wsparcie dla audytów FDA, jednostek notyfikowanych i klientów, w tym przegląd dokumentacji i inspekcje obiektów.
Jakie materiały są wymagane do zastosowań w pomieszczeniach czystych?
Zastosowania w pomieszczeniach czystych wymagają materiałów o niskich właściwościach odgazowywania, odporności na generowanie cząstek, kompatybilności chemicznej ze środkami czyszczącymi, gładkich nieporowatych powierzchniach i odpowiednich poziomach przewodności, z medyczną stalą nierdzewną 316L, PEEK, PTFE i specjalistycznymi polimerami zatwierdzonymi do pomieszczeń czystych, zapewniającymi optymalną wydajność przy jednoczesnym spełnieniu wymagań ISO 146444 standardy pomieszczeń czystych i utrzymanie integralności elektrycznej w kontrolowanych środowiskach.
Wybór materiału ma kluczowe znaczenie, ponieważ pomieszczenia czyste wymagają ścisłej kontroli zanieczyszczeń cząsteczkowych i molekularnych, które mogłyby zagrozić jakości produktu lub sterylnym warunkom.
Wymagania dotyczące stali nierdzewnej
316L Klasa medyczna: Austenityczna stal nierdzewna o niskiej zawartości węgla zapewnia doskonałą odporność na korozję i biokompatybilność w zastosowaniach medycznych.
Wykończenie elektropolerowane: Elektropolerowanie usuwa niedoskonałości powierzchni, zmniejsza wytwarzanie cząstek i tworzy gładkie powierzchnie dla skutecznego czyszczenia.
Obróbka pasywacyjna: Pasywacja chemiczna zwiększa odporność na korozję i usuwa zanieczyszczenia żelazem, które mogą powodować odbarwienia lub powstawanie cząstek.
Chropowatość powierzchni: Wartości Ra poniżej 0,8 mikrometra (32 mikrocale) minimalizują przywieranie bakterii i ułatwiają procesy czyszczenia i sterylizacji.
Polimery o wysokiej wydajności
PEEK (polieteroeteroketon): Doskonała odporność chemiczna, niski poziom odgazowywania i biokompatybilność sprawiają, że PEEK jest idealny do zastosowań farmaceutycznych i urządzeń medycznych.
PTFE (politetrafluoroetylen): Doskonała obojętność chemiczna i właściwości nieprzywierające zapewniają doskonałą odporność na chemikalia czyszczące i materiały biologiczne.
Nylony klasy medycznej: Specjalnie opracowane nylony z zatwierdzeniem USP Class VI oferują dobre właściwości mechaniczne i biokompatybilność do zastosowań medycznych.
POM zatwierdzony do pomieszczeń czystych: Polioksymetylen o niskiej generacji cząstek i dobrej stabilności wymiarowej do precyzyjnych zastosowań w pomieszczeniach czystych.
Zgodność z klasyfikacją pomieszczeń czystych
ISO klasa 5 (klasa 100): Niezwykle gładkie powierzchnie z minimalnym generowaniem cząstek do zastosowań w produkcji półprzewodników i farmaceutyków.
ISO klasy 6 (klasa 1000): Umiarkowana kontrola cząstek w produkcji urządzeń medycznych i niektórych procesach farmaceutycznych.
ISO klasy 7 (klasa 10000): Standardowe wymagania dotyczące pomieszczeń czystych dla ogólnych operacji montażu urządzeń farmaceutycznych i medycznych.
ISO klasa 8 (klasa 100000): Podstawowe wymagania dotyczące pomieszczeń czystych dla opakowań i niektórych procesów produkcji urządzeń medycznych.
Kontrola odgazowywania i zanieczyszczeń
Materiały o niskim poziomie odgazowywania: Materiały o minimalnej emisji lotnych związków organicznych (VOC), które mogłyby zanieczyścić wrażliwe procesy lub produkty.
Zanieczyszczenie molekularne: Kontrola zanieczyszczeń molekularnych, w tym silikonów, plastyfikatorów i innych związków organicznych, które mogą wpływać na jakość produktu.
Zanieczyszczenie jonowe: Materiały o niskiej zawartości jonów zapobiegające zanieczyszczeniu komponentów elektronicznych i produktów farmaceutycznych.
Substancje ekstrahowalne: Minimalna ilość substancji ekstrahowalnych, które mogłyby przedostać się do produktów farmaceutycznych lub roztworów czyszczących podczas użytkowania.
Matryca kompatybilności chemicznej
| Środek czyszczący | 316L SS | PEEK | PTFE | Nylon medyczny |
|---|---|---|---|---|
| Alkohol izopropylowy | Doskonały | Doskonały | Doskonały | Dobry |
| Nadtlenek wodoru | Doskonały | Doskonały | Doskonały | Uczciwy |
| Czwartorzędowy amon | Doskonały | Doskonały | Doskonały | Dobry |
| Podchloryn sodu | Dobry | Doskonały | Doskonały | Słaby |
| Kwas nadoctowy | Dobry | Doskonały | Doskonały | Słaby |
Hassan, który zarządza operacjami w najnowocześniejszym zakładzie farmaceutycznym w Szwajcarii, musiał zmodernizować dławiki kablowe w swoim pomieszczeniu czystym klasy ISO 5 do sterylnej produkcji zastrzyków. Istniejące dławnice generowały cząstki podczas cykli czyszczenia i nie były w stanie wytrzymać agresywnych protokołów sterylizacji wymaganych dla ich nowych produktów biologicznych. Dostarczyliśmy elektropolerowane dławnice kablowe ze stali nierdzewnej 316L o potwierdzonej niskiej generacji cząstek i pełnej zgodności chemicznej z procesami czyszczenia i sterylizacji. Modernizacja pozwoliła osiągnąć liczbę cząstek 90% poniżej limitów ISO klasy 5, wyeliminować zanieczyszczenia związane z czyszczeniem i wesprzeć pomyślną walidację nowej sterylnej linii produkcyjnej.
Jak zapewnić odpowiednie czyszczenie i sterylizację?
Zapewnienie odpowiedniej kompatybilności z czyszczeniem i sterylizacją wymaga wyboru materiałów, które są odporne na wielokrotne narażenie na działanie chemikaliów czyszczących i metod sterylizacji, projektowania powierzchni pod kątem pełnej możliwości czyszczenia, walidacji procedur czyszczenia i prowadzenia szczegółowej dokumentacji, przy czym medyczne dławiki kablowe wymagają gładkich powierzchni bez szczelin, materiałów odpornych na chemikalia i zatwierdzonych protokołów czyszczenia, które osiągają wymagane poziomy zapewnienia sterylności.
Zgodność czyszczenia i sterylizacji jest niezbędna, ponieważ nieodpowiednie odkażanie może prowadzić do zanieczyszczenia produktu, zagrożenia bezpieczeństwa pacjentów i naruszenia przepisów.
Kompatybilność metody sterylizacji
Autoklawowanie parowe: Materiały muszą być odporne na temperatury 121°C-134°C autoklawowanie parowe5 cykli bez degradacji, zmian wymiarów lub uszkodzenia uszczelnienia.
Promieniowanie gamma: Odporność na dawki promieniowania gamma 25-50 kGy powszechnie stosowane do sterylizacji urządzeń medycznych bez degradacji materiału.
Tlenek etylenu (EtO): Zgodność chemiczna ze sterylizacją EtO, w tym odporność na środek sterylizujący i odpowiednie właściwości odgazowywania.
Plazma nadtlenku wodoru: Kompatybilność z niskotemperaturowymi systemami sterylizacji plazmowej, w tym stabilność materiału i pełna penetracja środka sterylizującego.
Wymagania dotyczące walidacji czyszczenia
Procedury czyszczenia: Udokumentowane procedury czyszczenia określające środki chemiczne, stężenia, czas kontaktu i działania mechaniczne wymagane do skutecznego odkażania.
Protokoły walidacji: Formalne badania walidacyjne wykazujące skuteczność czyszczenia przy użyciu najgorszych scenariuszy zanieczyszczenia i testów analitycznych.
Kryteria akceptacji: Zdefiniowane kryteria akceptacji czystości, w tym kontrola wizualna, liczba cząstek, poziomy obciążenia biologicznego i limity pozostałości chemicznych.
Rutynowe monitorowanie: Bieżące programy monitorowania w celu weryfikacji ciągłej skuteczności czyszczenia i identyfikacji wszelkich spadków wydajności.
Rozważania dotyczące konstrukcji powierzchni
Cechy drenażu: Cechy konstrukcyjne, które ułatwiają całkowite odprowadzanie roztworów czyszczących i zapobiegają gromadzeniu się zanieczyszczeń.
Dostępność: Wszystkie powierzchnie muszą być dostępne do czyszczenia za pomocą standardowych narzędzi i procedur stosowanych w placówkach medycznych.
Wymagania dotyczące demontażu: Należy rozważyć, czy dławiki muszą być demontowane w celu czyszczenia, czy też czyszczenie w stanie nienaruszonym jest wystarczające dla danego zastosowania.
Wymiana uszczelki: Procedury wymiany i walidacji uszczelek, gdy elementy uszczelniające wymagają okresowej wymiany z powodu narażenia na działanie czyszczących środków chemicznych.
Dokumentacja i zgodność z przepisami
Instrukcje czyszczenia: Szczegółowe instrukcje czyszczenia, w tym procedury krok po kroku, specyfikacje chemiczne i środki ostrożności.
Dane dotyczące bezpieczeństwa materiałów: Pełne informacje na temat bezpieczeństwa materiałów, w tym kompatybilności chemicznej, limitów temperatury i kompatybilności ze sterylizacją.
Raporty walidacyjne: Raporty z walidacji czyszczenia wykazujące skuteczność i ustanawiające rutynowe wymagania dotyczące monitorowania.
Materiały szkoleniowe: Materiały szkoleniowe dla personelu placówki na temat prawidłowego czyszczenia, obsługi i procedur konserwacji dławików kablowych.
Testy kontroli jakości
Badanie obciążenia biologicznego: Regularne testy na obecność drobnoustrojów w celu weryfikacji skuteczności czyszczenia i identyfikacji potencjalnych obszarów problematycznych.
Testowanie endotoksyn: Testowanie endotoksyn bakteryjnych, które mogą powodować reakcje pirogenne w zastosowaniach farmaceutycznych i urządzeniach medycznych.
Zliczanie cząstek: Testowanie liczby cząstek w celu sprawdzenia, czy wymagania dotyczące pomieszczeń czystych są spełnione po czyszczeniu i konserwacji.
Analiza pozostałości chemicznych: Testowanie pod kątem pozostałości chemikaliów czyszczących, które mogłyby zanieczyścić produkty lub wpłynąć na biokompatybilność.
Jakie są kluczowe kryteria wyboru dla różnych zastosowań medycznych?
Kluczowe kryteria wyboru różnią się w zależności od zastosowania, ale obejmują wymogi zgodności z przepisami, poziomy biokompatybilności, klasyfikacje pomieszczeń czystych, metody sterylizacji, narażenie chemiczne i potrzeby w zakresie wydajności elektrycznej, przy czym sprzęt chirurgiczny wymaga najwyższej biokompatybilności, produkcja farmaceutyczna wymaga odporności chemicznej, a sprzęt diagnostyczny koncentruje się na integralności elektrycznej, podczas gdy wszystkie aplikacje wymagają odpowiednich certyfikatów regulacyjnych i zgodności z czyszczeniem.
Różne zastosowania medyczne mają unikalne wymagania, które należy dokładnie rozważyć podczas wyboru dławika kablowego, aby zapewnić optymalną wydajność i zgodność z przepisami.
Sprzęt chirurgiczny i do kontaktu z pacjentem
Wymagania dotyczące bezpośredniego kontaktu: Biokompatybilność klasy VI USP z dodatkowymi testami cytotoksyczności dla materiałów mających bezpośredni kontakt z pacjentem podczas zabiegów chirurgicznych.
Częstotliwość sterylizacji: Zdolność do wytrzymywania częstych cykli sterylizacji bez degradacji, zwykle wymagająca materiałów stabilnych przez setki cykli sterylizacji.
Bezpieczeństwo elektryczne: Zwiększone wymagania dotyczące bezpieczeństwa elektrycznego, w tym niski prąd upływowy i niezawodna izolacja dla urządzeń podłączonych do pacjenta.
Niezawodność w sytuacjach awaryjnych: Krytyczne wymagania dotyczące niezawodności sprzętu podtrzymującego życie i ratownictwa medycznego, którego awaria może mieć bezpośredni wpływ na bezpieczeństwo pacjentów.
Produkcja farmaceutyczna
Zgodność z GMP: Wymagania Dobrej Praktyki Wytwarzania, w tym identyfikowalność materiałów, kontrola zmian i dokumentacja walidacyjna.
Bezpieczeństwo kontaktu z produktem: Materiały, które nie zanieczyszczają produktów farmaceutycznych poprzez wymywanie, tworzenie cząstek lub interakcje chemiczne.
Walidacja czyszczenia: Rozbudowane wymagania dotyczące walidacji czyszczenia z udokumentowanymi procedurami i kryteriami akceptacji dla produkcji farmaceutycznej.
Dokumentacja wsadowa: Kompletna dokumentacja partii i identyfikowalność materiałów używanych w farmaceutycznym sprzęcie produkcyjnym.
Sprzęt diagnostyczny i laboratoryjny
Wymagania dotyczące precyzji: Stabilność wymiarowa i precyzja dla instrumentów analitycznych wymagających stałej wydajności mechanicznej i elektrycznej.
Odporność chemiczna: Odporność na chemikalia laboratoryjne, odczynniki i rozpuszczalniki czyszczące powszechnie stosowane w diagnostyce.
Wydajność EMC: Wymagania dotyczące kompatybilności elektromagnetycznej dla wrażliwych instrumentów analitycznych i sprzętu diagnostycznego.
Stabilność kalibracji: Stabilność mechaniczna, która nie wpłynie na kalibrację instrumentu lub dokładność pomiaru w czasie.
Produkcja urządzeń medycznych
Walidacja procesu: Materiały i komponenty wspierające wymagania walidacji procesów w produkcji urządzeń medycznych.
Systemy jakości: Integracja z systemami jakości ISO 13485, w tym kwalifikacja dostawców i procedury kontroli przychodzących.
Zarządzanie ryzykiem: Materiały wspierające wymagania dotyczące zarządzania ryzykiem związanym z urządzeniami medycznymi, w tym analizę trybu awaryjnego i strategie ograniczania ryzyka.
Wsparcie regulacyjne: Wsparcie dostawców przy składaniu wniosków regulacyjnych, w tym dokumentacja techniczna i ekspertyza regulacyjna.
Matryca decyzji wyboru
| Typ aplikacji | Kryteria podstawowe | Kryteria dodatkowe | Krytyczne standardy |
|---|---|---|---|
| Sprzęt chirurgiczny | Biokompatybilność | Sterylizacja | USP klasa VI, ISO 10993 |
| Farmaceutyczny | Odporność chemiczna | Zgodność z GMP | FDA 21 CFR, cGMP |
| Diagnostyka | Precyzja | Wydajność EMC | IEC 61326, ISO 15189 |
| Produkcja | Walidacja procesu | Systemy jakości | ISO 13485, 21 CFR 820 |
Analiza kosztów i korzyści
Koszt początkowy a cykl życia: Rozważ całkowity koszt posiadania, w tym koszty konserwacji, wymiany i zgodności w całym okresie eksploatacji sprzętu.
Ryzyko regulacyjne: Zrównoważyć koszty materialne z ryzykiem zgodności z przepisami i potencjalnymi kosztami braku zgodności.
Wymagania dotyczące wydajności: Upewnij się, że wybrane materiały spełniają minimalne wymagania dotyczące wydajności bez nadmiernej specyfikacji, która niepotrzebnie zwiększa koszty.
Możliwości dostawcy: Ocena możliwości dostawcy w zakresie bieżącego wsparcia, dokumentacji i pomocy w zakresie zgodności z przepisami.
Wnioski
Wybór dławików kablowych do sprzętu medycznego i pomieszczeń czystych wymaga zrozumienia unikalnych wymagań prawnych, materiałowych i wydajnościowych, które odróżniają te zastosowania od standardowych zastosowań przemysłowych. Sukces zależy od zrównoważenia biokompatybilności, możliwości czyszczenia, zgodności z przepisami i wydajności elektrycznej.
Kluczem do niezawodnego działania dławików kablowych do zastosowań medycznych jest współpraca z dostawcami, którzy rozumieją przepisy dotyczące urządzeń medycznych i mogą zapewnić odpowiednie materiały, dokumentację i bieżące wsparcie przez cały cykl życia produktu. W Bepto specjalizujemy się w dławnicach kablowych klasy medycznej, które spełniają wymagania FDA i międzynarodowe standardy urządzeń medycznych, zapewniając zapewnienie jakości i wsparcie regulacyjne potrzebne do krytycznych zastosowań w służbie zdrowia.
Najczęściej zadawane pytania dotyczące dławików kablowych
P: Jakich certyfikatów potrzebuję dla medycznych dławnic kablowych?
A: Medyczne dławnice kablowe zazwyczaj wymagają certyfikatu biokompatybilności USP klasy VI, zgodności materiałów z FDA 21 CFR i systemów jakości produkcji ISO 13485. Konkretne wymagania zależą od zastosowania i jurysdykcji prawnej.
P: Czy zwykłe dławiki kablowe ze stali nierdzewnej mogą być używane w zastosowaniach medycznych?
A: Zwykła stal nierdzewna może nie spełniać wymagań medycznych. Zastosowania medyczne wymagają stali nierdzewnej 316L klasy medycznej z elektropolerowanym wykończeniem, testami biokompatybilności i odpowiednią dokumentacją w celu zapewnienia zgodności z przepisami.
P: Jak czyścić i sterylizować dławiki kabli medycznych?
A: Należy postępować zgodnie z zatwierdzonymi przez producenta procedurami czyszczenia przy użyciu zatwierdzonych środków czyszczących i metod sterylizacji. Większość dławnic medycznych można sterylizować w autoklawie parowym, promieniowaniem gamma lub chemicznie przy zachowaniu odpowiedniej kompatybilności materiałowej.
P: Jaka jest różnica między dławnicami kablowymi do pomieszczeń czystych a dławnicami do zastosowań medycznych?
A: Klasa medyczna obejmuje wymagania dotyczące biokompatybilności i zgodności z FDA, podczas gdy klasa do pomieszczeń czystych koncentruje się na kontroli cząstek i odporności chemicznej. Niektóre zastosowania wymagają zarówno specyfikacji medycznej, jak i specyfikacji dla pomieszczeń czystych.
P: Jak często należy wymieniać dławiki kabli medycznych?
A: Częstotliwość wymiany zależy od cykli sterylizacji, ekspozycji chemicznej i zaleceń producenta. Zazwyczaj należy sprawdzać po każdych 100-200 cyklach sterylizacji i wymieniać w oparciu o ocenę stanu i wymagania walidacyjne.
-
Dowiedz się więcej o konkretnych testach reaktywności biologicznej wymaganych do uzyskania certyfikatu USP Class VI. ↩
-
Dostęp do przeglądu serii norm ISO 10993 dotyczących biologicznej oceny wyrobów medycznych. ↩
-
Zapoznaj się z oficjalnymi wytycznymi i przepisami FDA dotyczącymi bieżących dobrych praktyk produkcyjnych (cGMP). ↩
-
Zapoznaj się ze szczegółowym przewodnikiem po normach ISO 14644 dotyczących klasyfikacji czystości powietrza w pomieszczeniach czystych. ↩
-
Zrozumienie zasad sterylizacji parowej, w tym roli czasu, temperatury i ciśnienia. ↩



