Jaarlijks kost het mislukken van de sterilisatie van medische hulpmiddelen fabrikanten miljoenen. 15-20% van de mislukkingen wordt toegeschreven aan onvoldoende ontluchting waardoor sterilisatie niet goed kan plaatsvinden. Standaard ontluchtingspluggen falen onder autoclaaf1 temperaturen van 121-134°C of degraderen bij blootstelling aan ethyleenoxide (ETO) sterilisatie2 chemicaliën, waardoor de steriliteitsgarantie en de naleving van de regelgeving in gevaar komen.
Steriliseerbare ontluchtingspluggen maken effectieve sterilisatie mogelijk door stoom of ETO-gas door te laten terwijl steriele barrières na sterilisatie behouden blijven. Ventilatieopeningen met een PTFE-membraan zijn bestand tegen autoclaaftemperaturen tot 150 °C en tegen chemische afbraak door ETO, zodat medische hulpmiddelen, farmaceutische apparatuur en laboratoriuminstrumenten die gevalideerde sterilisatieprocessen vereisen, betrouwbaar steriel blijven.
Vorig jaar werkte ik samen met Dr. Sarah Mitchell, kwaliteitsdirecteur bij een toonaangevende fabrikant van medische hulpmiddelen in Boston. Hun standaard nylon ontluchtingspluggen smolten tijdens autoclaafcycli en blokkeerden een goede stoompenetratie. Nadat ze waren overgeschakeld op onze steriliseerbare ontluchtingspluggen van farmaceutische kwaliteit PTFE met gevalideerde temperatuurbestendigheid, bereikten ze een sterilisatie-efficiëntie van 100% gedurende 1000 validatiecycli - waardoor ze aan de FDA voldeden en de veiligheid van de patiënt garandeerden! 🏥
Inhoudsopgave
- Wat zijn steriliseerbare ventilatiepluggen en waarom zijn ze zo belangrijk?
- Welke invloed hebben verschillende sterilisatiemethoden op ventilatieplugmaterialen?
- Welke materialen zijn het beste voor sterilisatie in een autoclaaf?
- Welke materialen werken het beste voor ETO-sterilisatieprocessen?
- Hoe selecteer en valideer je steriliseerbare ventilatiepluggen?
- Veelgestelde vragen over steriliseerbare ventilatiepluggen
Wat zijn steriliseerbare ventilatiepluggen en waarom zijn ze zo belangrijk?
Inzicht in de rol van steriliseerbare ontluchtingspluggen bij de productie van medische hulpmiddelen en farmaceutische producten is essentieel voor het behoud van steriliteit en naleving van de regelgeving.
Steriliseerbare ontluchtingspluggen zijn speciale ademende ontluchtingspluggen die ontworpen zijn om sterilisatieprocessen te doorstaan, terwijl ze sterilisatie doorlaten en steriele barrières in stand houden. Ze zorgen voor luchtverplaatsing tijdens sterilisatie, voorkomen vacuümvorming tijdens koeling en handhaven steriele omstandigheden na sterilisatie. Kritische toepassingen zijn onder meer verpakking van medische apparatuur, farmaceutische containers, laboratoriumapparatuur en steriele verwerkingsapparatuur.
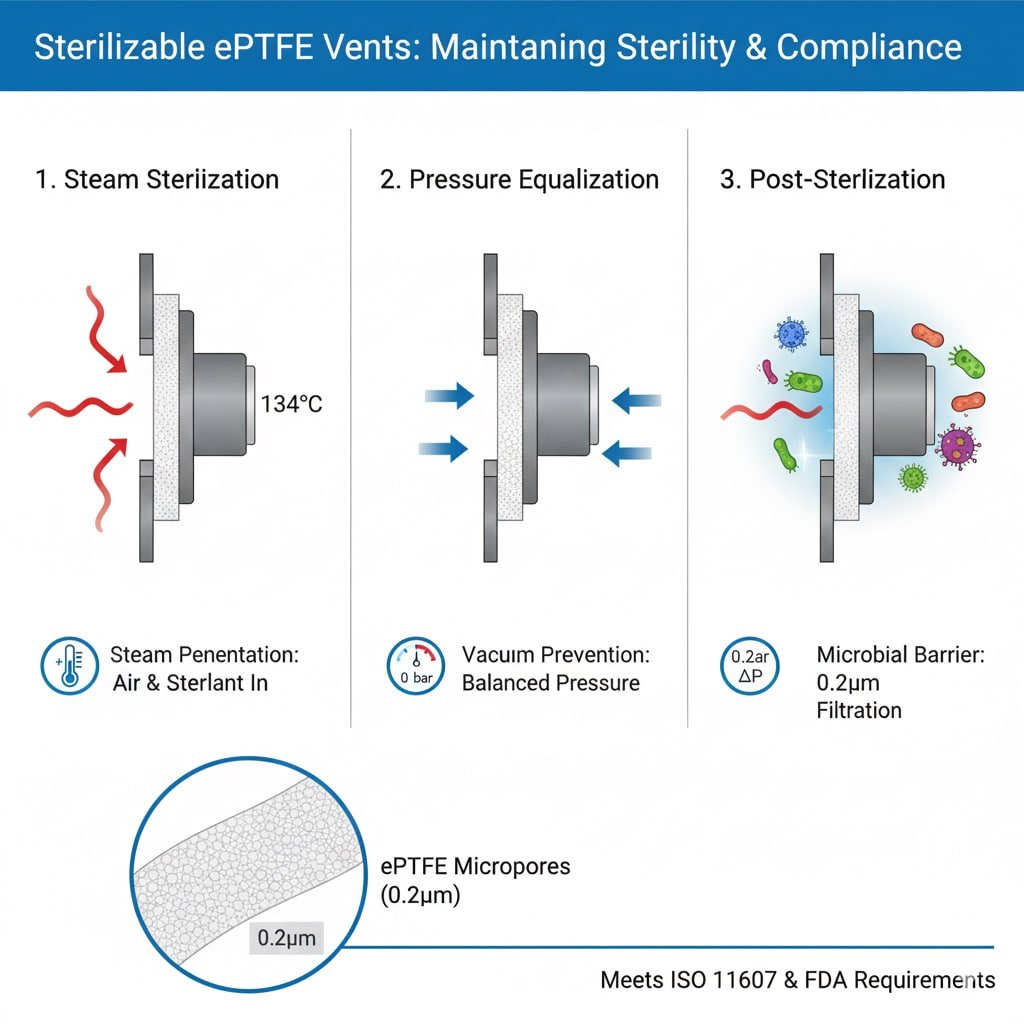
Vereisten voor sterilisatieproces
Stoompenetratie: Autoclaafsterilisatie vereist dat stoom door de verpakking dringt en in contact komt met alle oppervlakken, waardoor ventilatieopeningen nodig zijn die gas laten stromen terwijl microbiële barrières behouden blijven.
Luchtverplaatsing: Effectieve sterilisatie vereist volledige verwijdering van lucht en vervanging door sterilisatiemiddel, wat ventilatieopeningen mogelijk maken door gecontroleerde gasuitwisseling.
Druknivellering: Sterilisatiecycli creëren drukverschillen die ventilatieopeningen moeten opvangen zonder de steriele barrières of de integriteit van de verpakking aan te tasten.
Kritische prestatieparameters
Temperatuurbestendigheid: Steriliseerbare ventilatieopeningen moeten hun structurele integriteit en filtratievermogen behouden bij sterilisatietemperaturen van 121 °C tot 150 °C.
Chemische compatibiliteit: Materialen moeten bestand zijn tegen degradatie door sterilisatiechemicaliën zoals stoom, ethyleenoxide, waterstofperoxide en ozon.
Microbiële barrière-efficiëntie: Na sterilisatie moeten de ventilatieopeningen een betrouwbaar microbiële barrière3 met een poriegrootte van meestal 0,2-0,22 micron voor bacteriële retentie.
Overwegingen met betrekking tot naleving van regelgeving
FDA-validatievereisten: Toepassingen voor medische hulpmiddelen vereisen gevalideerde sterilisatieprocessen met gedocumenteerde ventingprestaties gedurende de sterilisatiecycli.
Voldoen aan ISO-normen: Steriliseerbare ventilatieopeningen moeten voldoen aan ISO 116074 verpakkingsnormen en ISO 17665 stoomsterilisatievereisten voor medische toepassingen.
Biocompatibiliteitstesten: Toepassingen waarbij medische apparatuur in contact komt met de huid kunnen USP klasse VI biocompatibiliteitstesten vereisen om de veiligheid van de patiënt te garanderen.
Toepassingscategorieën
Verpakkingen voor medische hulpmiddelen: Steriele verpakking voor implantaten, chirurgische instrumenten en medische wegwerphulpmiddelen die tot gebruik steriel moeten blijven.
Farmaceutische productie: Steriele verwerkingsapparatuur, bioreactoren en farmaceutische containers die gevalideerde sterilisatieprocessen vereisen.
Laboratoriumapparatuur: Autoclaveerbare laboratoriumcontainers, kweekvaten en analyseapparatuur die steriele omstandigheden vereisen voor nauwkeurige resultaten.
Welke invloed hebben verschillende sterilisatiemethoden op ventilatieplugmaterialen?
Verschillende sterilisatiemethoden creëren unieke uitdagingen voor ventplugmaterialen, waardoor specifieke materiaaleigenschappen en ontwerpoverwegingen nodig zijn voor optimale prestaties.
Stoomsterilisatie onderwerpt materialen aan hoge temperaturen (121-134°C) en verzadigde stoomcondities die thermische degradatie, dimensionale veranderingen en membraanschade kunnen veroorzaken. ETO-sterilisatie stelt materialen bloot aan reactieve chemicaliën bij lagere temperaturen (37-63°C) maar langere blootstellingstijden die chemische degradatie en uitgassing kunnen veroorzaken. Elke methode vereist een specifieke materiaalselectie voor betrouwbare prestaties.
Effecten van stoomsterilisatie
Thermische stress: Hoge temperaturen veroorzaken thermische uitzetting, mogelijk smelten van thermoplastische onderdelen en degradatie van temperatuurgevoelige materialen.
Hydrolyse reacties5: Blootstelling aan stoom kan hydrolytische afbraak van bepaalde polymeren veroorzaken, met name polyesters en sommige polyamiden.
Dimensionale stabiliteit: Herhaalde thermische cycli kunnen dimensionale veranderingen veroorzaken die de afdichtingsprestaties en filtratie-efficiëntie beïnvloeden.
ETO Sterilisatie Uitdagingen
Chemische reactiviteit: Ethyleenoxide reageert met materialen die actieve waterstofatomen bevatten, waardoor materiaaleigenschappen kunnen veranderen en giftige residuen kunnen ontstaan.
Vereisten voor uitgassing: ETO-gesteriliseerde producten vereisen een langere beluchtingsperiode om geabsorbeerde ETO en reactieproducten te verwijderen voordat ze veilig gebruikt kunnen worden.
Penetratie Kenmerken: ETO vereist specifieke vochtigheids- en temperatuursomstandigheden voor effectieve penetratie, wat van invloed is op de ontwerpeisen voor ventilatoren.
Plasma-effecten van waterstofperoxide
Oxidatieve afbraak: H2O2 plasma creëert zeer reactieve stoffen die organische materialen kunnen afbreken door oxidatiereacties.
Materiaal compatibiliteit: Veel elastomeren en sommige kunststoffen zijn onverenigbaar met H2O2-plasmasterilisatie vanwege de snelle afbraak.
Voordelen bij lage temperaturen: Plasmasterilisatie werkt bij lage temperaturen (45-55°C), waardoor de thermische stress op temperatuurgevoelige materialen wordt verminderd.
Overwegingen met betrekking tot gammastraling
Stralingsschade: Hoog-energetische gammastraling kan kettingsplitsing of verknoping van polymeren veroorzaken, waardoor de materiaaleigenschappen aanzienlijk veranderen.
Accumulatie van doses: Herhaalde gammasterilisatie kan cumulatieve schade veroorzaken, waardoor het aantal sterilisatiecycli dat materialen kunnen doorstaan beperkt wordt.
Behoefte aan antioxidanten: Stralingsbestendige formules hebben vaak antioxidanten nodig om oxidatieve degradatie tijdens en na bestraling te voorkomen.
Onlangs heb ik Ahmed Al-Rashid, operations manager bij een farmaceutische fabriek in Dubai, geholpen bij het oplossen van ETO-sterilisatie validatieproblemen met hun bioreactor ontluchtingssystemen. Hun standaard ontluchtingspluggen absorbeerden ETO en vereisten verlengde beluchtingsperioden van 14 dagen die de productieschema's verstoorden. Door onze ETO-compatibele PTFE-ontluchtingspluggen met minimale absorptiekenmerken te implementeren, hebben ze de beluchtingstijd teruggebracht tot 24 uur met behoud van volledige steriliteitsgarantie - waardoor de productie-efficiëntie drastisch is verbeterd! 🚀
Welke materialen zijn het beste voor sterilisatie in een autoclaaf?
Het selecteren van geschikte materialen voor sterilisatie in een autoclaaf vereist inzicht in thermische stabiliteit, weerstand tegen hydrolyse en prestaties op lange termijn bij herhaalde blootstelling aan stoom.
PTFE (polytetrafluorethyleen) biedt superieure autoclaafprestaties met continue gebruikstemperaturen tot 260°C, uitstekende chemische inertie en hydrolyseweerstand. PVDF (polyvinylideenfluoride) biedt een goede thermische stabiliteit tot 150 °C tegen lagere kosten. Vermijd nylon, standaard polyethyleen en de meeste elastomeren die afbreken onder autoclaveeromstandigheden, waardoor de filtratie- en afdichtingsprestaties in gevaar komen.
Voordelen van PTFE-membranen
Uitzonderlijke temperatuurbestendigheid: PTFE behoudt zijn structurele integriteit en filterprestaties bij temperaturen ver boven de typische autoclaafcondities (121-134°C).
Chemische traagheid: PTFE is bestand tegen degradatie door stoom, reinigingschemicaliën en sterilisatiebijproducten, waardoor langdurige consistente prestaties gegarandeerd zijn.
Hydrofobe eigenschappen: De hydrofobe aard van PTFE voorkomt waterabsorptie en behoudt dimensionale stabiliteit tijdens sterilisatiecycli.
Vergelijking van materiaalprestaties
| Materiaal | Maximumtemperatuur (°C) | Stoom Weerstand | Weerstand tegen hydrolyse | Kostenfactor |
|---|---|---|---|---|
| PTFE | 260 | Uitstekend | Uitstekend | Hoog |
| PVDF | 150 | Goed | Goed | Medium |
| PP (polypropyleen) | 135 | Eerlijk | Eerlijk | Laag |
| Nylon | 80-100 | Slecht | Slecht | Laag |
Materiaalkeuze behuizing
Roestvrij staal 316L: Biedt uitstekende corrosiebestendigheid, thermische stabiliteit en reinigbaarheid voor farmaceutische en medische toepassingen die gevalideerde reinigingsprocedures vereisen.
PEEK (polyetheretherketon): Biedt een uitstekende thermische stabiliteit (continu gebruik tot 250°C) met een uitstekende chemische weerstand voor veeleisende autoclaventoepassingen.
Polypropyleen: Kosteneffectieve optie voor toepassingen voor eenmalig gebruik met toereikende prestaties voor standaard autoclaafcycli bij 121°C.
Overwegingen voor afdichtingscomponenten
EPDM O-ringen: Biedt goede weerstand tegen stoom en thermische stabiliteit voor temperaturen tot 150°C met uitstekende afdichtingsprestaties.
Siliconen afdichtingen: Bieden een superieure temperatuurbestendigheid (tot 200°C), maar kunnen compatibiliteitsproblemen hebben met bepaalde reinigingschemicaliën.
PTFE ingekapselde O-ringen: Combineer de chemische weerstand van PTFE met elastomeer afdichtingseigenschappen voor veeleisende toepassingen die beide prestatiekenmerken vereisen.
Ontwerpoptimalisatie voor gebruik in een autoclaaf
Thermische expansie Accommodatie: Ventilatieontwerpen moeten rekening houden met de differentiële thermische uitzetting tussen materialen om te voorkomen dat de afdichting faalt tijdens temperatuurschommelingen.
Afwatering: Een goed afwateringsontwerp voorkomt ophoping van condensaat dat de filtratieprestaties in gevaar kan brengen of verontreinigingsrisico's kan veroorzaken.
Ondersteuning voor validatie: Ontwerpkenmerken moeten validatietests vergemakkelijken, waaronder drukverval, microbiële uitdaging en verificatie van thermische prestaties.
Welke materialen werken het beste voor ETO-sterilisatieprocessen?
ETO-sterilisatie stelt unieke materiaaluitdagingen die chemische compatibiliteit, minimale absorptie en snelle uitgassing vereisen voor een efficiënte verwerking.
PTFE en PVDF bieden uitstekende ETO-compatibiliteit met minimale chemische absorptie en snelle uitgassing. Vermijd materialen met actieve waterstofsites zoals nylon, PVC en natuurrubber die reageren met ETO en toxische verbindingen vormen. Roestvrijstalen behuizingen bieden optimale chemische weerstand, terwijl siliconen afdichtingen goede ETO-compatibiliteit bieden met acceptabele uitgassingseigenschappen voor de meeste toepassingen.
Chemische compatibiliteit met ETO
Reactiemechanismen: ETO reageert met materialen die hydroxyl-, amino-, carboxyl- en sulfhydrylgroepen bevatten, waarbij ethyleenglycolderivaten en andere potentieel giftige verbindingen worden gevormd.
Absorptiekenmerken: Materialen met een hoge ETO-absorptie vereisen langere beluchtingsperioden, waardoor de verwerkingstijd en -kosten aanzienlijk toenemen.
Uitgaskinetiek: Materialen met een snelle uitgassing maken kortere beluchtingscycli mogelijk, waardoor de procesefficiëntie verbetert en voorraden minder lang hoeven te worden aangehouden.
Materiaal ETO prestatieklassementen
Uitstekende ETO-compatibiliteit:
- PTFE: minimale absorptie, snelle uitgassing, geen chemische reactiviteit
- PVDF: Lage absorptie, goede uitgassing, uitstekende chemische weerstand
- Roestvrij staal: Geen absorptie, onmiddellijk bruikbaar
Goede ETO-compatibiliteit:
- Polypropyleen: Matige absorptie, aanvaardbare uitgassing
- Silicone: Lage reactiviteit, vereisten voor matige uitgassing
Slechte ETO-compatibiliteit:
- Nylon: Hoge reactiviteit, langdurige beluchting vereist
- PVC: Chemische afbraak, vorming van giftige verbindingen
- Natuurlijk rubber: hoge absorptie, potentiële degradatie
Vereiste beluchtingstijd
| Materiaal | Typische beluchtingstijd | ETO-absorptieniveau | Uitstroomsnelheid |
|---|---|---|---|
| PTFE | 8-24 uur | Minimaal | Snel |
| PVDF | 24-48 uur | Laag | Goed |
| Polypropyleen | 48-72 uur | Matig | Matig |
| Nylon | 7-14 dagen | Hoog | Langzaam |
Optimalisatie van procesparameters
Temperatuurregeling: ETO-sterilisatie werkt meestal bij 37-63 °C en vereist materialen die over dit temperatuurbereik goed blijven presteren.
Vochtigheidsvereisten: De effectiviteit van ETO vereist een relatieve vochtigheid van 40-80%, waardoor materialen nodig zijn die consistent presteren onder deze vochtomstandigheden.
Beheer van gasconcentraties: Voor ETO-concentraties van 450-1200 mg/L zijn materialen nodig die bestand zijn tegen chemische aantasting terwijl ze toch de penetratie van het sterilisatiemiddel mogelijk maken.
Overwegingen met betrekking tot validatie
Residu testen: ETO-gesteriliseerde producten moeten getest worden op ETO-residuen en reactieproducten om ervoor te zorgen dat de veiligheidslimieten worden nageleefd.
Onderhoud van biocompatibiliteit: Materialen moeten biocompatibel blijven na blootstelling aan ETO en beluchting, wat een gevalideerde materiaalselectie vereist.
Procesbewaking: ETO-sterilisatie vereist een continue controle van temperatuur, vochtigheid, druk en gasconcentratie tijdens de hele cyclus.
Hoe selecteer en valideer je steriliseerbare ventilatiepluggen?
Een juiste selectie en validatie van steriliseerbare ontluchtingspluggen garandeert betrouwbare sterilisatieprestaties, naleving van regelgeving en operationeel succes op de lange termijn.
Selectie vereist het afstemmen van materiaaleigenschappen op de sterilisatiemethode, het definiëren van prestatievereisten en het overwegen van regelgevende normen. Validatie omvat thermische prestatietests, microbiële onderzoeken, beoordeling van chemische compatibiliteit en stabiliteitsbeoordeling op lange termijn. Documenteer alle tests volgens FDA- en ISO-normen voor indiening bij de regelgevende instanties en naleving van het kwaliteitssysteem.
Selectiecriteria
Compatibiliteit met sterilisatiemethode: Stem ventielmaterialen af op specifieke sterilisatiemethoden (stoom, ETO, H2O2-plasma, gamma) op basis van de vereisten voor temperatuur, chemicaliën en stralingsbestendigheid.
Prestatiespecificaties: Bepaal de vereiste doorstroomsnelheden, drukwaarden, filtratie-efficiëntie en microbiële barrière-eigenschappen op basis van de toepassingsvereisten.
Wettelijke vereisten: Houd rekening met de classificatie van FDA-apparaten, naleving van ISO-normen en biocompatibiliteitseisen voor beoogde gebruikstoepassingen.
Toepassingsbeoordelingsparameters
Gebruiksomgeving: Evalueer temperatuurbereiken, chemische blootstelling, drukcondities en verontreinigingsrisico's gedurende de levenscyclus van het product.
Sterilisatiefrequentie: Overweeg eenmalig gebruik versus meerdere sterilisatiecycli en de cumulatieve effecten op de prestaties en betrouwbaarheid van het materiaal.
Validatiebereik: Bepaal de testvereisten op basis van risicobeoordeling, de route van de regelgeving en de vereisten van het kwaliteitssysteem.
Protocol voor validatietests
Testen van thermische prestaties:
- Temperatuurwisselingen bij sterilisatiecondities
- Dimensionale stabiliteitsmeting
- Controle van filterefficiëntie na thermische blootstelling
Microbiële uitdagingstests:
- Bacteriële uitdaging met geschikte testorganismen
- Verificatie van steriliteitsbehoud
- Beoordeling van de integriteit van de barrière op lange termijn
Chemische compatibiliteitsbeoordeling:
- Evaluatie van materiaaldegradatie
- Testen op extraheerbare en uitloogbare stoffen
- Verificatie onderhoud biocompatibiliteit
Documentatie-eisen
Materiaalspecificaties: Complete materiaalinformatiebladen inclusief chemische samenstelling, thermische eigenschappen en wettelijke certificeringen.
Testprotocollen: Gedetailleerde validatieprotocollen volgens FDA-richtlijnen en ISO-normen voor sterilisatievalidatie.
Prestatiegegevens: Uitgebreide testresultaten die de prestaties onder gespecificeerde bedrijfsomstandigheden en sterilisatiecycli aantonen.
Integratie kwaliteitssysteem
Kwalificatie van leveranciers: Opstellen van kwaliteitsovereenkomsten met leveranciers, inclusief traceerbaarheid van materialen, wijzigingsbeheer en vereisten voor kwaliteitsdocumentatie.
Inkomende inspectie: Ontwikkelen van inspectieprocedures voor verificatie van kritische afmetingen, materiaaleigenschappen en prestatiekenmerken.
Procesvalidatie: De prestaties van de ontluchting integreren in de algehele validatie van het sterilisatieproces, inclusief tests op basis van het slechtst denkbare scenario.
Overwegingen met betrekking tot risicobeheer
Faalmode-analyse: Identificeer mogelijke defecten, waaronder materiaaldegradatie, defecte afdichting en compromittering van filtratie met de juiste strategieën om deze te beperken.
Wijzigingsbeheer: Stel procedures op voor het beheer van materiaalwijzigingen, leverancierswijzigingen en specificatiewijzigingen met de juiste revalidatievereisten.
Continue bewaking: Implementeer doorlopende bewakingsprogramma's om de prestaties te controleren en potentiële problemen te identificeren voordat ze de productkwaliteit beïnvloeden.
Conclusie
Steriliseerbare ontluchtingspluggen spelen een cruciale rol bij het garanderen van effectieve sterilisatie met behoud van steriele barrières in medische apparatuur en farmaceutische toepassingen. Het begrijpen van de unieke uitdagingen van verschillende sterilisatiemethoden en het selecteren van de juiste materialen is essentieel voor betrouwbare prestaties en naleving van de regelgeving.
Ontluchtingspluggen op basis van PTFE bieden superieure prestaties bij meerdere sterilisatiemethoden, met een uitstekende temperatuurbestendigheid, chemische compatibiliteit en betrouwbaarheid op de lange termijn. Een juiste selectie en validatie zorgen voor een optimale sterilisatie-effectiviteit terwijl de verwerkingstijd en -kosten tot een minimum worden beperkt.
Bepto biedt een uitgebreid assortiment steriliseerbare ontluchtingspluggen met PTFE-membranen van farmaceutische kwaliteit, gevalideerde temperatuurprestaties en complete documentatiepakketten voor wettelijke vereisten. Met meer dan tien jaar ervaring in gespecialiseerde ontluchtingstoepassingen en ISO-gecertificeerde productiecapaciteiten bieden wij de betrouwbare, kosteneffectieve oplossingen die u nodig hebt voor kritieke sterilisatietoepassingen. Vertrouw op ons om uw sterilisatieprocessen gevalideerd en uw producten veilig te houden! 🔬
Veelgestelde vragen over steriliseerbare ventilatiepluggen
V: Kan dezelfde ontluchtingsplug worden gebruikt voor zowel autoclaaf- als ETO-sterilisatie?
A: Ja, ontluchtingspluggen met een PTFE-membraan kunnen zowel autoclaaf- als ETO-sterilisatie aan. PTFE biedt een uitstekende temperatuurbestendigheid voor autoclaafcycli en minimale ETO-absorptie voor snelle beluchting, waardoor het ideaal is voor faciliteiten die meerdere sterilisatiemethoden gebruiken.
V: Hoeveel sterilisatiecycli kan een ontluchtingsplug weerstaan?
A: PTFE-ontluchtingspluggen van hoge kwaliteit zijn gewoonlijk bestand tegen meer dan 100 autoclaafcycli of meer dan 50 ETO-cycli met behoud van filtratieprestaties. De werkelijke levensduur hangt af van sterilisatieparameters, behandelingsprocedures en acceptatiecriteria voor de prestaties van uw specifieke toepassing.
V: Welke poriegrootte is vereist voor steriele filtratie in medische toepassingen?
A: Medische toepassingen vereisen meestal een poriegrootte van 0,2 of 0,22 micron voor betrouwbare bacteriële retentie. Deze poriegrootte biedt een gevalideerde steriliteitsgarantie terwijl er voldoende gasstroom is voor effectieve sterilisatie en druknivellering.
V: Zijn er speciale validatietests nodig voor steriliseerbare ontluchtingspluggen?
A: Ja, steriliseerbare ontluchtingspluggen vereisen validatietests, waaronder thermische prestaties, microbiële uitdaging en onderzoeken naar materiaalcompatibiliteit. Tests moeten worden uitgevoerd volgens de richtlijnen van de FDA en ISO-normen, met documentatie ter ondersteuning van de validatie van uw sterilisatieproces en indiening van regelgevende documenten.
V: Hoe voorkom je contaminatie door ontluchtingspluggen tijdens sterilisatie?
A: Voorkom besmetting door een juiste installatie, beschermende afdekkingen tijdens het hanteren, gevalideerde sterilisatieparameters en de juiste opslag na sterilisatie. Gebruik steriele technieken tijdens de installatie en zorg ervoor dat de ontluchtingspluggen ontworpen zijn voor uw specifieke sterilisatiemethode en toepassingsvereisten.
-
Leer de wetenschappelijke principes van autoclaafsterilisatie en hoe verzadigde stoom onder druk wordt gebruikt om micro-organismen effectief te doden. ↩
-
Verken het chemische proces van ethyleenoxide (ETO) sterilisatie, een methode bij lage temperatuur die wordt gebruikt voor het steriliseren van warmte- en vochtgevoelige medische hulpmiddelen. ↩
-
Ontdek de methoden die worden gebruikt om de effectiviteit van een microbiële barrière te testen en te valideren, zodat deze het binnendringen van micro-organismen voorkomt en steriel blijft. ↩
-
Bekijk de belangrijkste vereisten van de norm ISO 11607, die de materialen en tests voor steriele barrièresystemen voor medische hulpmiddelen specificeert. ↩
-
De chemische reactie van hydrolyse begrijpen en begrijpen hoe deze de degradatie van bepaalde polymeermaterialen kan veroorzaken wanneer deze worden blootgesteld aan water of stoom bij hoge temperaturen. ↩



