Een onjuiste selectie van wartels in medische en cleanroomomgevingen veroorzaakt vervuilingsrisico's, het niet voldoen aan regelgeving en apparatuurstoringen die leiden tot gevaren voor de veiligheid van patiënten, kostbare fabriekssluitingen en FDA-overtredingen, terwijl een onjuiste afdichting, ongeschikte materialen en slechte reinigbaarheid leiden tot bacteriegroei, deeltjesvervuiling en steriliteitsschendingen die kritieke activiteiten in de gezondheidszorg in gevaar brengen. Veel facilitair managers worstelen met het selecteren van wartels die voldoen aan strenge medische normen en tegelijkertijd betrouwbare elektrische prestaties leveren.
Voor het selecteren van wartels voor medische apparatuur en cleanrooms is inzicht nodig in de FDA-voorschriften, USP klasse VI1 materiaalvereisten, IP68+ afdichtingsnormen en vereisten voor cleanroomclassificatie, met roestvrij staal van medische kwaliteit of een constructie van gespecialiseerd polymeer die biocompatibiliteit, chemische weerstand en gladde oppervlakken biedt voor effectieve reiniging en sterilisatie met behoud van elektrische integriteit in kritieke toepassingen in de gezondheidszorg. Het succes hangt af van het evenwicht tussen naleving van de regelgeving en operationele betrouwbaarheid.
Ik heb gewerkt met ziekenhuisingenieurs van grote medische centra in Boston, farmaceutische fabrikanten in Zwitserland en cleanroomfaciliteiten in Singapore. Ik heb geleerd dat wartels van medische kwaliteit essentieel zijn voor het handhaven van steriele omgevingen en het waarborgen van de veiligheid van patiënten. Laat me u de cruciale kennis delen voor het selecteren van optimale wartels voor uw medische en cleanroomtoepassingen.
Inhoudsopgave
- Wat maakt medische wartels anders dan standaard wartels?
- Hoe voldoet u aan de voorschriften van de FDA en medische hulpmiddelen?
- Welke materialen zijn nodig voor cleanroomtoepassingen?
- Hoe zorg je voor de juiste reinigings- en sterilisatiecompatibiliteit?
- Wat zijn de belangrijkste selectiecriteria voor verschillende medische toepassingen?
- Veelgestelde vragen over medische wartels
Wat maakt medische wartels anders dan standaard wartels?
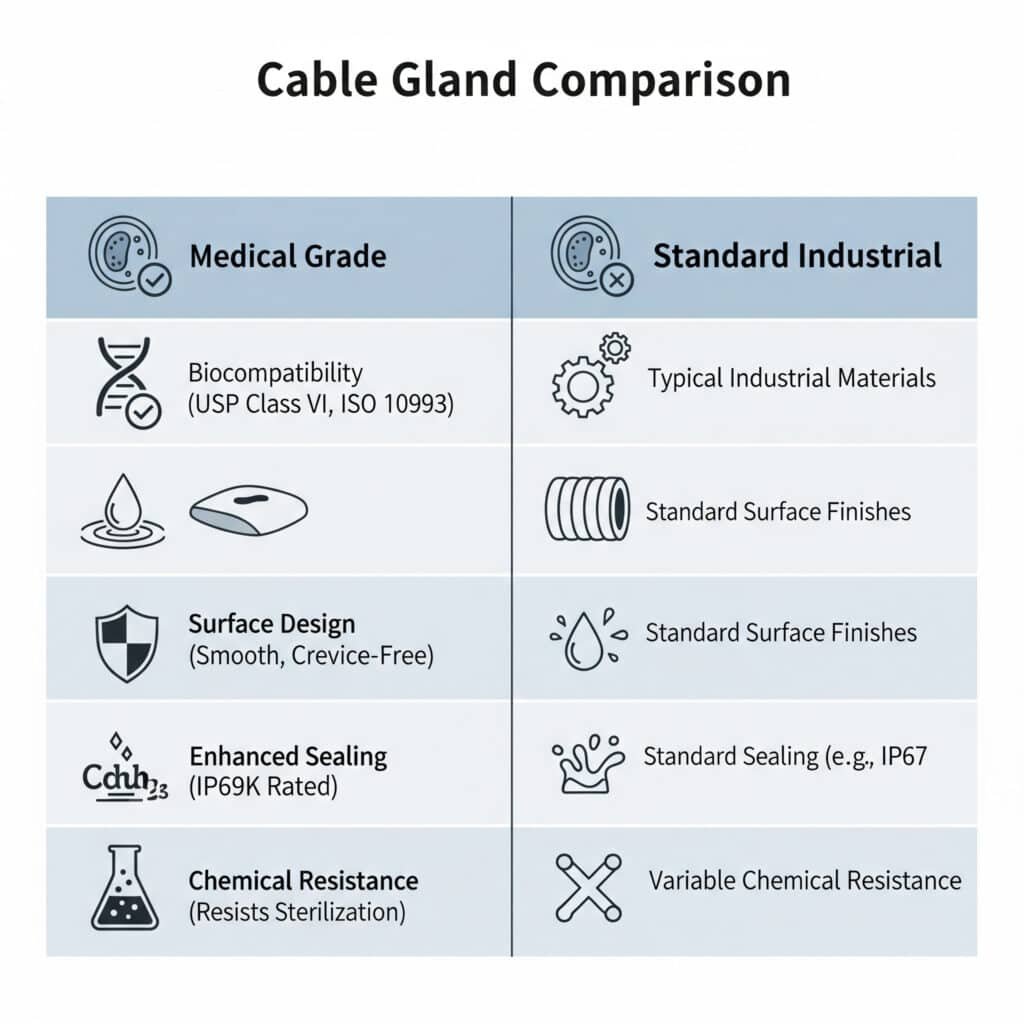
Medische wartels verschillen van standaard wartels door het gebruik van biocompatibele materialen, gladde, reinigbare oppervlakken die voldoen aan de FDA-voorschriften, verbeterde afdichting ter voorkoming van besmetting en chemische weerstand tegen reinigingsmiddelen en sterilisatieprocessen, met speciale ontwerpen die spleten elimineren waar bacteriën zich kunnen nestelen terwijl de elektrische prestaties in kritieke zorgomgevingen behouden blijven.
Inzicht in deze verschillen is cruciaal omdat medische toepassingen unieke veiligheids- en regelgevingsvereisten hebben waaraan standaard industriële wartels niet adequaat kunnen voldoen.
Biocompatibiliteitseisen
Voldoet aan USP klasse VI: Voor medische wartels moeten materialen worden gebruikt die voldoen aan de biologische tests van klasse VI van de United States Pharmacopeia voor biocompatibiliteit en veiligheid in toepassingen met medische apparatuur.
ISO 10993-normen: Materialen moeten voldoen aan ISO 109932 biologische evaluatiestandaarden voor medische hulpmiddelen, die garanderen dat er geen cytotoxische, sensibiliserende of irriterende effecten zijn op menselijk weefsel.
FDA 21 CFR 177 Goedkeuring: Food-grade materialen die voldoen aan de FDA-voorschriften voor direct en indirect contact met voedingsmiddelen zijn vaak vereist voor farmaceutische toepassingen en toepassingen met medische apparatuur.
Biocompatibele polymeren: Gespecialiseerde materialen zoals PEEK van medische kwaliteit, PTFE of nylons van farmaceutische kwaliteit bieden biocompatibiliteit zonder afbreuk te doen aan de mechanische eigenschappen.
Oppervlakteontwerp voor reinigbaarheid
Glad oppervlak: Medische wartels hebben ultragladde oppervlakken met Ra-waarden van doorgaans minder dan 0,8 micrometer om bacteriële aanhechting te voorkomen en effectieve reiniging mogelijk te maken.
Spleetvrij ontwerp: Eliminatie van scherpe hoeken, diepe draden en complexe geometrieën die bacteriën kunnen herbergen of bestand zijn tegen reinigings- en sterilisatieprocessen.
Afgeronde randen: Alle externe oppervlakken hebben afgeronde hoeken en vloeiende overgangen om het reinigen te vergemakkelijken en schade aan handschoenen voor cleanrooms of steriele verpakkingen te voorkomen.
Minimaal oppervlak: Gestroomlijnde ontwerpen minimaliseren het oppervlak dat blootgesteld wordt aan vervuiling, terwijl de noodzakelijke mechanische en elektrische prestaties behouden blijven.
Verbeterde afdichtingsprestaties
IP68+ Beoordelingen: Superieure milieubescherming dan standaard IP68, vaak IP69K voor reinigingstoepassingen onder hoge druk en hoge temperaturen.
Barrières tegen vervuiling: Meerdere afdichtingsfasen voorkomen dat deeltjes, bacteriën en reinigingschemicaliën binnendringen die een steriele omgeving in gevaar kunnen brengen.
Drukbestendigheid: Verbeterde drukwaarden om bestand te zijn tegen agressieve reinigingsprocedures en sterilisatieprocessen zonder dat de afdichting defect raakt.
Betrouwbaarheid op lange termijn: Afdichtingsmaterialen behouden hun integriteit door herhaalde sterilisatiecycli en blootstelling aan agressieve reinigingschemicaliën.
Eigenschappen chemische weerstand
Compatibiliteit reinigingsmiddel: Bestand tegen ziekenhuisontsmettingsmiddelen, quaternaire ammoniumverbindingen, waterstofperoxide en andere agressieve reinigingschemicaliën.
Sterilisatieweerstand: Materialen zijn bestand tegen gammastraling, ethyleenoxide, autoclaveren met stoom en andere sterilisatiemethoden zonder afbraak.
Farmaceutische chemicaliën: Bestand tegen oplosmiddelen, zuren, basen en farmaceutische verbindingen die vaak voorkomen in medische productieomgevingen.
Temperatuurstabiliteit: Behoud van eigenschappen door middel van sterilisatietemperatuurcycli en vereisten voor temperatuurregeling in cleanrooms.
David, een facilitair manager bij een grote farmaceutische fabriek in New Jersey, werd geconfronteerd met terugkerende verontreinigingsproblemen in hun steriele afvullijnen waar standaard wartels bacteriën herbergden ondanks strenge reinigingsprotocollen. De bestaande messing wartels hadden complexe draadpatronen en oppervlakteafwerkingen die niet goed gesteriliseerd konden worden, wat leidde tot afkeur van batches en problemen met de naleving van de FDA-voorschriften. We specificeerden roestvrijstalen wartels van medische kwaliteit met elektrolytisch gepolijste oppervlakken en spleetvrije ontwerpen die voldeden aan de vereisten van USP Class VI. De upgrade elimineerde verontreinigingsbronnen, bereikte een reinigingseffectiviteit van 99,9% en hielp de fabriek door de FDA-inspecties te komen terwijl het aantal afgekeurde producten met 85% werd verlaagd. 😊
Hoe voldoet u aan de voorschriften van de FDA en medische hulpmiddelen?
Om te voldoen aan de voorschriften van de FDA en medische hulpmiddelen moeten materialen met de juiste certificeringen worden gebruikt, moet gedetailleerde documentatie worden bijgehouden en moeten de volgende regels worden gevolgd Goede productiepraktijken (GMP)3De kwaliteitssystemen moeten voldoen aan 21 CFR Part 820, waarbij medische wartels door de FDA goedgekeurde materialen, biocompatibiliteitstests en productiecontroles vereisen die een consistente kwaliteit en veiligheid garanderen in toepassingen voor medische hulpmiddelen.
Naleving van de regelgeving is onontkoombaar bij medische toepassingen omdat fouten kunnen leiden tot schade aan patiënten, terugroepingen van producten en ernstige juridische gevolgen.
FDA materiaalvereisten
21 CFR Deel 177: Materialen die in contact komen met farmaceutische producten of medische hulpmiddelen moeten voldoen aan de FDA-voorschriften voor voedingsadditieven voor stoffen die indirect in contact komen met voedingsmiddelen.
Master Access File (MAF): Leveranciers moeten FDA Master Access Files bijhouden met documenten over materiaalveiligheid, fabricageprocessen en procedures voor kwaliteitscontrole.
Drug Master File (DMF): Voor farmaceutische toepassingen kunnen materialen een Drug Master File-registratie vereisen met gedetailleerde informatie over de samenstelling en productie.
Certificaat van naleving: Leveranciers moeten certificaten overleggen waarin wordt bevestigd dat de materialen voldoen aan alle toepasselijke FDA-voorschriften en specificaties.
Kwaliteitsnormen voor medische hulpmiddelen
Voldoet aan ISO 13485: Productie moet ISO 13485 systemen voor kwaliteitsbeheer van medische hulpmiddelen volgen voor ontwerp, productie en postmarket surveillance.
21 CFR Deel 820 (QSR): Naleving van de regels van het kwaliteitssysteem om te zorgen voor de juiste ontwerpcontroles, documentcontrole en corrigerende/preventieve maatregelen.
Risicobeheer: ISO 14971 risicobeheerprocessen voor medische hulpmiddelen, inclusief risicoanalyse, evaluatie en controlemaatregelen.
Ontwerpcontroles: Formele ontwerpcontroleprocessen, waaronder ontwerpplanning, invoer-/uitvoereisen, beoordelingen, verificatie en validatie.

Documentatie en traceerbaarheid
Materiaalcertificaten: Volledige traceerbaarheid van materialen met analysecertificaten, resultaten van biocompatibiliteitstests en documentatie over naleving van regelgeving.
Productiegegevens: Gedetailleerde productieregistraties, inclusief procesparameters, kwaliteitscontroletests en documentatie van batches voor volledige traceerbaarheid.
Wijzigingsbeheer: Formele procedures voor wijzigingsbeheer voor alle wijzigingen aan materialen, processen of specificaties die van invloed zijn op naleving van de regelgeving.
Kwalificatie van leveranciers: Uitgebreide kwalificatieprogramma's voor leveranciers om ervoor te zorgen dat alle materialen en onderdelen voldoen aan de vereisten voor medische hulpmiddelen.
Validatievereisten
Biocompatibiliteitstesten: USP klasse VI-tests inclusief systemische injectie-, intracutane en implantatietests om de biologische veiligheid te verifiëren.
Reinigingsvalidatie: Gedocumenteerde reinigingsprocedures met validatiegegevens die aantonen dat verontreinigingen effectief worden verwijderd en de bioburden worden verlaagd.
Sterilisatievalidatie: Validatie van sterilisatieprocessen, inclusief het in kaart brengen van doses, steriliteitsniveaus en compatibiliteitsstudies van materialen.
Prestatietests: Elektrische, mechanische en milieutests om te controleren of de prestaties voldoen aan de vereisten voor medische hulpmiddelen gedurende de gehele levenscyclus van het product.
Ondersteuning bij indiening regelgeving
510(k) Documentatie: Technische documentatie ter ondersteuning van FDA 510(k) aanvragen voor medische hulpmiddelen met wartels.
Technische bestanden: Uitgebreide technische dossiers voor CE-markering onder Medical Device Regulation (MDR) op Europese markten.
Kwaliteitsovereenkomsten: Formele kwaliteitsovereenkomsten met leveranciers waarin verantwoordelijkheden, specificaties en nalevingsvereisten zijn vastgelegd.
Auditondersteuning: Ondersteuning bij audits door FDA, aangemelde instanties en klanten, waaronder beoordeling van documentatie en inspecties van faciliteiten.
Welke materialen zijn nodig voor cleanroomtoepassingen?
Cleanroomtoepassingen vereisen materialen met lage uitgassingseigenschappen, weerstand tegen het genereren van deeltjes, chemische compatibiliteit met reinigingsmiddelen, gladde niet-poreuze oppervlakken en de juiste geleidingsniveaus. Roestvrij staal van medische kwaliteit 316L, PEEK, PTFE en gespecialiseerde polymeren die zijn goedgekeurd voor cleanroomtoepassingen leveren optimale prestaties en voldoen aan de volgende eisen ISO 146444 normen voor cleanrooms en behoud van elektrische integriteit in gecontroleerde omgevingen.
De materiaalselectie is cruciaal omdat cleanrooms een strikte controle vereisen van deeltjes en moleculaire verontreiniging die de productkwaliteit of steriele omstandigheden in gevaar kunnen brengen.
Vereisten voor roestvrij staal
316L medische kwaliteit: Austenitisch roestvrij staal met een laag koolstofgehalte dat superieure corrosiebestendigheid en biocompatibiliteit biedt voor medische toepassingen.
Elektrolytisch gepolijst Afwerking: Elektrolytisch polijsten verwijdert oneffenheden in het oppervlak, vermindert het ontstaan van deeltjes en creëert gladde oppervlakken voor een effectieve reiniging.
Passiveringsbehandeling: Chemische passivering verbetert de corrosiebestendigheid en verwijdert ijzervervuiling die verkleuring of het ontstaan van deeltjes kan veroorzaken.
Oppervlakteruwheid: Ra-waarden onder 0,8 micrometer (32 microinches) minimaliseren bacteriële hechting en vergemakkelijken reinigings- en sterilisatieprocessen.
Hoogwaardige polymeren
PEEK (polyetheretherketon): Dankzij de uitstekende chemische weerstand, lage uitgassing en biocompatibiliteit is PEEK ideaal voor toepassingen in de farmaceutische industrie en medische apparatuur.
PTFE (polytetrafluorethyleen): Superieure chemische inertie en antikleefeigenschappen bieden uitstekende weerstand tegen reinigingschemicaliën en biologische materialen.
Nylons van medische kwaliteit: Speciaal geformuleerde nylons met USP klasse VI goedkeuring bieden goede mechanische eigenschappen met biocompatibiliteit voor medische toepassingen.
Voor cleanrooms goedgekeurd POM: Polyoxymethyleen met lage deeltjesvorming en goede maatvastheid voor cleanroomtoepassingen.
Compatibiliteit met cleanroomclassificatie
ISO-klasse 5 (klasse 100): Ultragladde oppervlakken met minimale deeltjesvorming voor halfgeleider- en farmaceutische productietoepassingen.
ISO klasse 6 (klasse 1000): Matige deeltjescontrole voor de productie van medische apparatuur en sommige farmaceutische processen.
ISO-klasse 7 (klasse 10000): Standaardvereisten voor cleanrooms voor algemene assemblagewerkzaamheden in de farmaceutische industrie en medische hulpmiddelen.
ISO-klasse 8 (klasse 100000): Basisvereisten voor cleanrooms voor verpakking en sommige productieprocessen van medische hulpmiddelen.
Uitstoot en verontreinigingscontrole
Materialen met lage uitgassing: Materialen met een minimale uitstoot van vluchtige organische stoffen (VOS) die gevoelige processen of producten kunnen verontreinigen.
Moleculaire besmetting: Controle van moleculaire verontreinigingen zoals siliconen, weekmakers en andere organische verbindingen die de productkwaliteit kunnen beïnvloeden.
Ionische verontreiniging: Materialen met een laag ionisch gehalte om contaminatie van elektronische componenten en farmaceutische producten te voorkomen.
Extraheerbare stoffen: Minimaal extraheerbare stoffen die tijdens gebruik kunnen lekken naar farmaceutische producten of reinigingsoplossingen.
Matrix chemische compatibiliteit
| Reinigingsmiddel | 316L SS | PEEK | PTFE | Medisch nylon |
|---|---|---|---|---|
| Isopropyl alcohol | Uitstekend | Uitstekend | Uitstekend | Goed |
| Waterstofperoxide | Uitstekend | Uitstekend | Uitstekend | Eerlijk |
| Quaternair ammonium | Uitstekend | Uitstekend | Uitstekend | Goed |
| Natriumhypochloriet | Goed | Uitstekend | Uitstekend | Slecht |
| Perazijnzuur | Goed | Uitstekend | Uitstekend | Slecht |
Hassan, die de leiding heeft over een ultramoderne farmaceutische faciliteit in Zwitserland, moest de wartels upgraden in hun ISO klasse 5 cleanroom voor de steriele productie van injectables. De bestaande wartels genereerden deeltjes tijdens reinigingscycli en waren niet bestand tegen de agressieve sterilisatieprotocollen die vereist zijn voor hun nieuwe biologische producten. We leverden elektrolytisch gepolijste 316L roestvrijstalen wartels met een gevalideerde lage deeltjesgeneratie en volledige chemische compatibiliteit met hun reinigings- en sterilisatieprocessen. De upgrade bereikte deeltjesaantallen van 90% onder de ISO Klasse 5 limieten, elimineerde reinigingsgerelateerde verontreinigingen en ondersteunde een succesvolle validatie van hun nieuwe steriele productielijn.
Hoe zorg je voor de juiste reinigings- en sterilisatiecompatibiliteit?
Om een goede reiniging en sterilisatiecompatibiliteit te garanderen, moeten materialen worden geselecteerd die bestand zijn tegen herhaalde blootstelling aan reinigingschemicaliën en sterilisatiemethoden, moeten oppervlakken worden ontworpen voor volledige reinigbaarheid, moeten reinigingsprocedures worden gevalideerd en moet een gedetailleerde documentatie worden bijgehouden, waarbij medische kabelwartels gladde, spleetvrije oppervlakken, chemicaliënbestendige materialen en gevalideerde reinigingsprotocollen vereisen die de vereiste steriliteitsniveaus halen.
De compatibiliteit van reiniging en sterilisatie is essentieel omdat onvoldoende ontsmetting kan leiden tot productcontaminatie, risico's voor de patiëntveiligheid en overtredingen van de regelgeving.
Compatibiliteit sterilisatiemethode
Autoclaveren met stoom: Materialen moeten bestand zijn tegen 121°C-134°C autoclaveren met stoom5 cycli zonder degradatie, dimensionale veranderingen of defecten aan de afdichting.
Gammastraling: Bestand tegen gammastralingsdoses van 25-50 kGy die gewoonlijk worden gebruikt voor sterilisatie van medische hulpmiddelen zonder materiaaldegradatie.
Ethyleenoxide (EtO): Chemische compatibiliteit met EtO-sterilisatie, inclusief weerstand tegen het sterilisatiemiddel en goede ontgassingseigenschappen.
Waterstofperoxide Plasma: Compatibiliteit met plasmasterilisatiesystemen bij lage temperaturen, inclusief materiaalstabiliteit en volledige penetratie van het sterilisatiemiddel.
Reinigingsvalidatievereisten
Reinigingsprocedures: Gedocumenteerde reinigingsprocedures met chemicaliën, concentraties, contacttijden en mechanische handelingen die nodig zijn voor effectieve decontaminatie.
Validatieprotocollen: Formele validatiestudies die de effectiviteit van de reiniging aantonen met behulp van worst-case vervuilingsscenario's en analytische tests.
Acceptatiecriteria: Vastgestelde acceptatiecriteria voor reinheid, waaronder visuele inspectie, deeltjesaantallen, bioburdeniveaus en limieten voor chemische residuen.
Routinematige controle: Voortdurende controleprogramma's om de blijvende effectiviteit van de reiniging te verifiëren en eventuele achteruitgang in prestaties vast te stellen.
Overwegingen bij het ontwerp van het oppervlak
Afwatering: Ontwerpkenmerken die een volledige afvoer van reinigingsoplossingen bevorderen en plasvorming van verontreinigingen voorkomen.
Toegankelijkheid: Alle oppervlakken moeten kunnen worden gereinigd met standaard reinigingsgereedschap en -procedures die in medische instellingen worden gebruikt.
Vereisten voor demontage: Overweeg of wartels gedemonteerd moeten worden voor reiniging of dat intacte reiniging voldoende is voor de toepassing.
Pakking vervangen: Procedures voor het vervangen van pakkingen en validatie wanneer afdichtingscomponenten periodiek moeten worden vervangen vanwege blootstelling aan reinigingsmiddelen.
Documentatie en naleving
Reinigingsinstructies: Gedetailleerde reinigingsinstructies inclusief stapsgewijze procedures, chemische specificaties en veiligheidsmaatregelen.
Materiaalveiligheidsgegevens: Volledige informatie over materiaalveiligheid, inclusief chemische compatibiliteit, temperatuurlimieten en sterilisatiecompatibiliteit.
Validatierapporten: Reinigingsvalidatierapporten die de effectiviteit aantonen en routinematige controlevereisten vaststellen.
Trainingsmateriaal: Trainingsmateriaal voor facilitair personeel over de juiste schoonmaak-, hanterings- en onderhoudsprocedures voor medische kabelwartels.
Kwaliteitscontrole
Bioburden testen: Regelmatig testen op microbiële verontreiniging om de effectiviteit van de reiniging te controleren en mogelijke probleemgebieden te identificeren.
Endotoxinetests: Testen op bacteriële endotoxines die pyrogene reacties kunnen veroorzaken in farmaceutische toepassingen en toepassingen voor medische apparatuur.
Tellen van deeltjes: Testen van het aantal deeltjes om te controleren of de cleanroomvereisten worden nageleefd na reinigings- en onderhoudsactiviteiten.
Chemische residu-analyse: Testen op chemische reinigingsresten die producten kunnen verontreinigen of de biocompatibiliteit kunnen beïnvloeden.
Wat zijn de belangrijkste selectiecriteria voor verschillende medische toepassingen?
De belangrijkste selectiecriteria variëren per toepassing, maar omvatten vereisten voor naleving van regelgeving, biocompatibiliteitsniveaus, cleanroomclassificaties, sterilisatiemethoden, chemische blootstelling en elektrische prestatiebehoeften, waarbij chirurgische apparatuur de hoogste biocompatibiliteit vereist, farmaceutische productie chemische resistentie nodig heeft en diagnostische apparatuur zich richt op elektrische integriteit, terwijl voor alle toepassingen de juiste regelgevende certificeringen en reinigingscompatibiliteit vereist zijn.
Verschillende medische toepassingen hebben unieke vereisten die zorgvuldig overwogen moeten worden tijdens de selectie van de kabeldoorvoer om optimale prestaties en naleving van de regelgeving te garanderen.
Chirurgische apparatuur en apparatuur voor patiëntcontact
Vereisten voor direct contact: USP klasse VI biocompatibiliteit met aanvullende cytotoxiciteitstests voor materialen die in direct contact komen met de patiënt tijdens chirurgische procedures.
Sterilisatiefrequentie: Het vermogen om veelvuldige sterilisatiecycli te doorstaan zonder degradatie, waarbij meestal materialen nodig zijn die honderden sterilisatiecycli doorstaan.
Elektrische veiligheid: Verbeterde elektrische veiligheidsvereisten, waaronder een lage lekstroom en betrouwbare isolatie voor op de patiënt aangesloten apparatuur.
Betrouwbaarheid in noodgevallen: Kritische betrouwbaarheidseisen voor levensinstandhoudings- en medische noodapparatuur waarbij falen de veiligheid van de patiënt direct kan beïnvloeden.
Farmaceutische Productie
Naleving van GMP: Good Manufacturing Practice-vereisten, inclusief traceerbaarheid van materialen, wijzigingsbeheer en validatiedocumentatie.
Productcontactveiligheid: Materialen die farmaceutische producten niet verontreinigen door uitloging, deeltjesvorming of chemische interactie.
Reinigingsvalidatie: Uitgebreide validatievereisten voor reiniging met gedocumenteerde procedures en acceptatiecriteria voor farmaceutische productie.
Batchdocumentatie: Volledige batchedocumentatie en traceerbaarheid voor materialen die worden gebruikt in farmaceutische productieapparatuur.
Diagnostische en laboratoriumapparatuur
Precisievereisten: Dimensionale stabiliteit en precisie voor analytische instrumenten die consistente mechanische en elektrische prestaties vereisen.
Chemische weerstand: Bestand tegen laboratoriumchemicaliën, reagentia en reinigingsmiddelen die vaak worden gebruikt in diagnostische toepassingen.
EMC-prestaties: Eisen voor elektromagnetische compatibiliteit voor gevoelige analytische instrumenten en diagnostische apparatuur.
Stabiliteit van kalibratie: Mechanische stabiliteit die de kalibratie van het instrument of de meetnauwkeurigheid na verloop van tijd niet beïnvloedt.
Productie medische apparatuur
Procesvalidatie: Materialen en componenten die de vereisten voor procesvalidatie voor de productie van medische hulpmiddelen ondersteunen.
Kwaliteitssystemen: Integratie met ISO 13485 kwaliteitssystemen, inclusief leverancierskwalificatie en inkomende inspectieprocedures.
Risicobeheer: Materialen die de vereisten voor risicobeheer van medische hulpmiddelen ondersteunen, inclusief faalmodeanalyse en strategieën voor risicobeperking.
Ondersteuning bij regelgeving: Leveranciersondersteuning voor regelgevingsaanvragen, inclusief technische documentatie en regelgevingsdeskundigheid.
Matrix voor selectiebeslissing
| Type toepassing | Primaire criteria | Secundaire criteria | Kritische normen |
|---|---|---|---|
| Chirurgische apparatuur | Biocompatibiliteit | Sterilisatie | USP klasse VI, ISO 10993 |
| Farmaceutisch | Chemische weerstand | Naleving GMP | FDA 21 CFR, cGMP |
| Diagnostisch | Precisie | EMC-prestaties | IEC 61326, ISO 15189 |
| Productie | Procesvalidatie | Kwaliteitssystemen | ISO 13485, 21 CFR 820 |
Kosten-batenanalyse
Initiële kosten vs. levenscyclus: Houd rekening met de totale eigendomskosten, inclusief kosten voor onderhoud, vervanging en naleving gedurende de levensduur van de apparatuur.
Regelgevingsrisico: Materiële kosten afwegen tegen risico's op naleving van regelgeving en potentiële kosten van niet-naleving.
Prestatievereisten: Zorg ervoor dat de geselecteerde materialen voldoen aan de minimale prestatievereisten zonder overspecificatie die de kosten onnodig verhoogt.
Leverancierscapaciteiten: Evalueer de mogelijkheden van leveranciers voor doorlopende ondersteuning, documentatie en hulp bij naleving van regelgeving.
Conclusie
Het selecteren van wartels voor medische apparatuur en cleanrooms vereist inzicht in de unieke regelgeving, materialen en prestatie-eisen die deze toepassingen onderscheiden van standaard industrieel gebruik. Het succes hangt af van de balans tussen biocompatibiliteit, reinigbaarheid, naleving van regelgeving en elektrische prestaties.
De sleutel tot betrouwbare prestaties van medische wartels ligt in het werken met leveranciers die de regelgeving voor medische hulpmiddelen begrijpen en die de juiste materialen, documentatie en voortdurende ondersteuning kunnen bieden gedurende de gehele levenscyclus van het product. Bij Bepto zijn we gespecialiseerd in wartels van medische kwaliteit die voldoen aan de vereisten van de FDA en internationale normen voor medische hulpmiddelen en bieden we de kwaliteitsborging en ondersteuning bij regelgeving die nodig is voor kritieke toepassingen in de gezondheidszorg.
Veelgestelde vragen over medische wartels
V: Welke certificeringen heb ik nodig voor medische wartels?
A: Medische wartels vereisen doorgaans USP klasse VI biocompatibiliteitscertificering, FDA 21 CFR naleving voor materialen en ISO 13485 productiekwaliteitssystemen. Specifieke vereisten zijn afhankelijk van uw toepassing en de jurisdictie van de regelgevende instanties.
V: Kunnen gewone roestvrijstalen wartels worden gebruikt in medische toepassingen?
A: Gewoon roestvrij staal voldoet mogelijk niet aan de medische vereisten. Medische toepassingen vereisen 316L roestvast staal van medische kwaliteit met elektrolytisch gepolijste afwerking, biocompatibiliteitstesten en de juiste documentatie voor naleving van de regelgeving.
V: Hoe reinig en steriliseer ik medische wartels?
A: Volg de gevalideerde reinigingsprocedures van de fabrikant met goedgekeurde reinigingsmiddelen en sterilisatiemethoden. De meeste medische klieren zijn geschikt voor autoclaveren met stoom, gammastraling of chemische sterilisatie met de juiste materiaalcompatibiliteit.
V: Wat is het verschil tussen cleanroom- en medische wartels?
A: Medische kwaliteit omvat biocompatibiliteitsvereisten en FDA-conformiteit, terwijl cleanroomkwaliteit zich richt op deeltjesbeheersing en chemische weerstand. Voor sommige toepassingen zijn zowel medische als cleanroomspecificaties vereist.
V: Hoe vaak moeten medische wartels worden vervangen?
A: De vervangingsfrequentie is afhankelijk van sterilisatiecycli, chemische blootstelling en aanbevelingen van de fabrikant. Inspecteer gewoonlijk na elke 100-200 sterilisatiecycli en vervang op basis van conditiebeoordeling en validatievereisten.
-
Lees meer over de specifieke biologische reactiviteitstests die vereist zijn voor USP klasse VI certificering. ↩
-
Een overzicht van de ISO 10993-serie normen voor de biologische evaluatie van medische hulpmiddelen. ↩
-
Bekijk de officiële richtlijnen en voorschriften van de FDA voor Current Good Manufacturing Practices (cGMP). ↩
-
Bekijk een gedetailleerde gids voor de ISO 14644-normen voor het classificeren van de luchtzuiverheid in cleanrooms. ↩
-
De principes van stoomsterilisatie begrijpen, inclusief de rol van tijd, temperatuur en druk. ↩



