医療やクリーンルーム環境における不適切なケーブルグランド選定は、汚染リスク、規制遵守の失敗、機器の誤作動を引き起こし、患者の安全への危険、費用のかかる施設のシャットダウン、FDA違反を招きます。一方、不適切なシーリング、不適切な材料、清掃性の悪さは、細菌の増殖、微粒子汚染、重要な医療業務を危険にさらす無菌違反につながります。多くの施設管理者は、信頼性の高い電気的性能を維持しながら、厳しい医療基準を満たす腺の選定に苦慮しています。
医療機器やクリーンルーム用のケーブルグランドを選択するには、FDAの規制を理解する必要があります、 USPクラスVI1 医療グレードのステンレス鋼や特殊ポリマー構造により、重要なヘルスケア・アプリケーションで電気的完全性を維持しながら、生体適合性、耐薬品性、効果的な洗浄と滅菌のための滑らかな表面を提供します。 成功するかどうかは、規制遵守と操業の信頼性とのバランスにかかっている。
ボストンの主要医療センター、スイスの製薬メーカー、シンガポールのクリーンルーム施設で病院のエンジニアと仕事をしてきた経験から、医療グレードのケーブルグランドは無菌環境を維持し、患者の安全を確保するために不可欠であることを学びました。お客様の医療及びクリーンルーム用途に最適なケーブルグランドを選択するための重要な知識を共有させてください。
目次
- 医療用ケーブル・グランドと標準的なグランドの違いは?
- FDAと医療機器規制を満たすには?
- クリーンルーム用途に必要な材料とは?
- 適切な洗浄と滅菌の適合性を確保するには?
- 医療用途別の主な選択基準とは?
- 医療用ケーブルグランドに関するFAQ
医療用ケーブル・グランドと標準的なグランドの違いは?
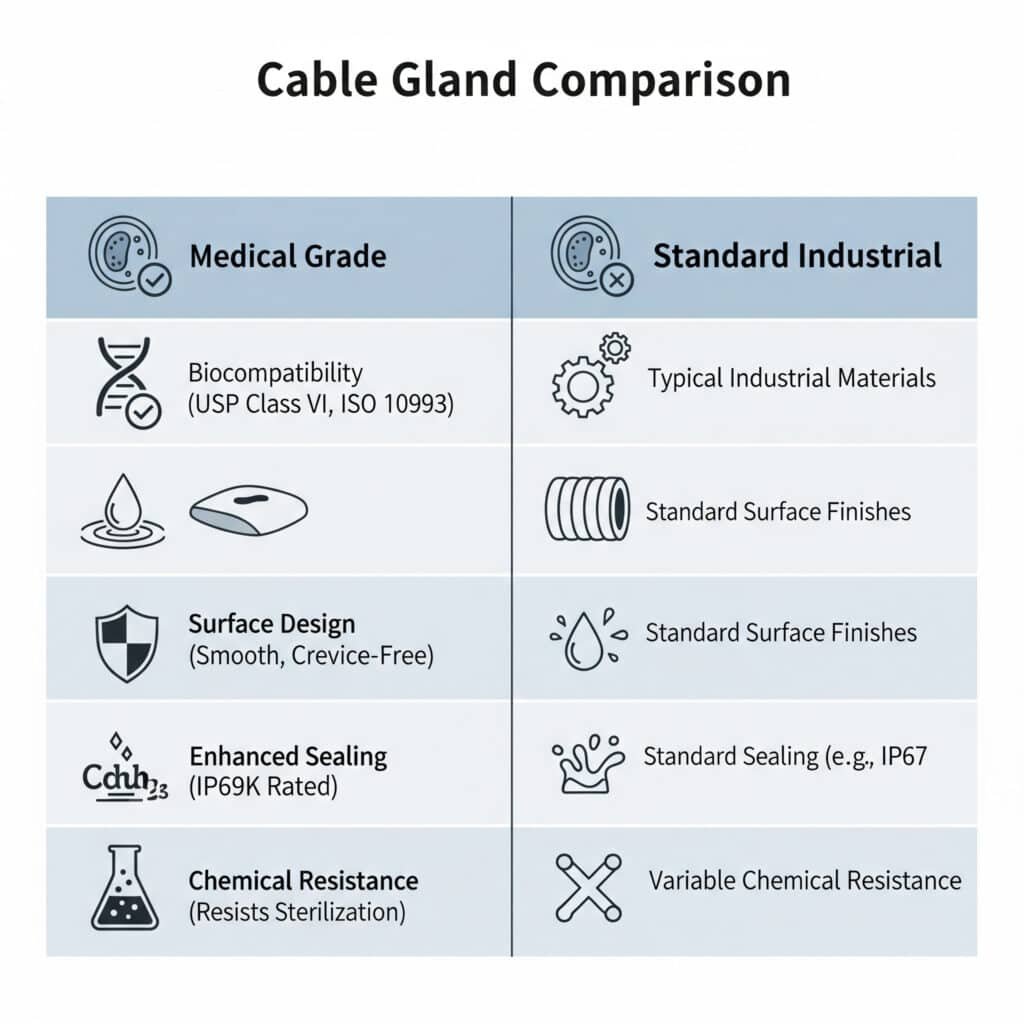
医療用ケーブルグランドは、標準的なグランドとは異なり、生体適合材料を使用し、滑らかでクリーニング可能な表面を特徴とし、FDA規制を満たし、汚染防止のために強化された密閉性を提供し、洗浄剤や滅菌プロセスに対する耐薬品性を提供し、重要な医療環境において電気的性能を維持しながら細菌が繁殖する隙間をなくす特殊な設計となっています。
医療用途には、標準的な工業用グランドでは十分に対応できない独自の安全性と規制要件があるため、これらの違いを理解することは極めて重要です。
生体適合性の要件
USPクラスVI準拠: 医療用ケーブルグランドは、医療機器用途における生体適合性と安全性のための米国薬局方クラスVI生物学的試験に合格した材料を使用しなければならない。
ISO 10993規格: 材料は以下の条件を満たしていなければならない。 ISO 109932 医療機器の生物学的評価基準であり、ヒト組織に対する細胞毒性、感作性、刺激性の影響がないことを保証する。
FDA 21 CFR 177承認: 直接および間接的な食品接触に関するFDAの規制を満たす食品グレードの材料は、医薬品や医療機器の用途でしばしば必要とされます。
生体適合性ポリマー: 医療グレードのPEEK、PTFE、製薬グレードのナイロンなどの特殊素材は、機械的特性を損なうことなく生体適合性を提供します。
清掃性を考慮した表面デザイン
滑らかな表面仕上げ: 医療用腺は、細菌の付着を防ぎ、効果的な洗浄を可能にするため、Ra値が通常0.8マイクロメートル以下の超平滑な表面を特徴としている。
隙間のないデザイン: 細菌が繁殖したり、洗浄や滅菌処理に抵抗したりする可能性のある鋭角、深いスレッド、複雑な形状の排除。
丸みを帯びたエッジ: すべての外面は、洗浄を容易にし、クリーンルーム用手袋や無菌包装への損傷を防ぐために、丸みを帯びたエッジと滑らかな移行部を備えています。
最小表面積: 流線型の設計は、必要な機械的・電気的性能を維持しながら、汚染にさらされる表面積を最小限に抑える。
シーリング性能の向上
IP68+等級: 標準的なIP68を超える優れた環境保護性能で、高圧・高温洗浄用途ではIP69Kを達成することもあります。
汚染の障壁: 複数の密閉段階が、無菌環境を損なう可能性のある粒子、バクテリア、洗浄薬品の侵入を防ぐ。
耐圧性: 圧力定格が強化され、シールに不具合を生じることなく積極的な洗浄手順や滅菌処理に耐える。
長期的な信頼性: シーリング材は、繰り返される滅菌サイクルや過酷な洗浄化学薬品への暴露にも完全性を維持します。
耐薬品性特性
洗浄剤の適合性: ホスピタルグレードの消毒剤、第4級アンモニウム化合物、過酸化水素水、その他の刺激の強い洗浄薬品に対する耐性。
滅菌耐性: ガンマ線、エチレンオキサイド、蒸気オートクレーブ、その他の滅菌方法にも劣化することなく耐える。
医薬化学品: 溶媒、酸、塩基、医薬化合物など、医療製造環境で一般的に見られるものに対する耐性。
温度安定性: 滅菌温度サイクルおよびクリーンルームの温度管理要件を通じて特性を維持する。
ニュージャージー州の大手製薬工場の設備管理者であるデイビッド氏は、無菌充填ラインにおいて、標準的なケーブルグランドが厳格な洗浄プロトコールにもかかわらず細菌を保有していたため、繰り返し発生する汚染の問題に直面していた。既存の真鍮製ケーブルグランドは、複雑なスレッドパターンと表面仕上げが施されていたため、十分な滅菌ができず、バッチの不合格やFDAコンプライアンス上の懸念につながっていました。私たちは、電解研磨された表面とUSPクラスVIの要件を満たす隙間のないデザインを持つ医療グレードのステンレス鋼ケーブルグランドを指定しました。このアップグレードにより、汚染源が除去され、99.9%の洗浄効果が達成され、FDAの検査に合格し、製品の不合格率が85%減少しました。
FDAと医療機器規制を満たすには?
FDAと医療機器の規制を満たすには、適切な認証を受けた材料を使用し、詳細な文書を管理し、次のことを行う必要があります。 適正製造基準(GMP)3医療用ケーブルグランドは、FDA承認の材料、生体適合性試験、医療機器用途における一貫した品質と安全性を保証する製造管理を必要とし、トレーサビリティを確保し、21 CFR Part 820に準拠した品質システムを導入しています。
医療用アプリケーションでは、規制遵守は譲れないものです。なぜなら、失敗すると患者への危害、製品リコール、深刻な法的結果を招く可能性があるからです。
FDA材料要件
21 CFR Part 177: 医薬品または医療機器と接触する材料は、間接的食品接触物質に関するFDA食品添加物規制を満たさなければならない。
マスター・アクセス・ファイル(MAF): サプライヤーは、材料の安全性、製造工程、品質管理手順を文書化したFDAマスターアクセスファイルを保持しなければならない。
医薬品マスターファイル(DMF): 医薬品用途の場合、材料は詳細な組成と製造情報を記載した医薬品マスターファイル登録が必要となる場合がある。
適合証明書: サプライヤーは、材料が適用されるすべてのFDA規制および仕様に適合していることを確認する証明書を提出しなければならない。
医療機器品質基準
ISO13485準拠: 製造は、設計、製造、市販後調査においてISO 13485医療機器品質管理システムに従わなければならない。
21 CFR Part 820 (QSR): 適切な設計管理、文書管理、是正措置/予防措置を保証する品質システム規則の遵守。
リスク管理: ISO 14971 医療機器のリスクマネジメントプロセス(リスク分析、評価、管理策を含む)。
デザインコントロール: 設計計画、入出力要件、レビュー、検証、妥当性確認を含む正式な設計管理プロセス。

文書化とトレーサビリティ
材料証明書: 分析証明書、生体適合性試験結果、規制遵守文書による完全な材料トレーサビリティ。
製造記録: 完全なトレーサビリティのためのプロセスパラメータ、品質管理試験、バッチ文書などの詳細な製造記録。
チェンジ・コントロール: 規制遵守に影響を及ぼす材料、工程、仕様の変更に対する正式な変更管理手順。
サプライヤー資格: すべての材料とコンポーネントが医療機器の要件を満たすことを保証する包括的なサプライヤー認定プログラム。
バリデーション要件
生体適合性試験: 生物学的安全性を確認するための全身注射、皮内注射、移植試験を含むUSPクラスVI試験。
クリーニングの検証: 汚染物質の効果的な除去および生物負荷の低減を証明する検証データを伴う、文書化された洗浄手順。
滅菌バリデーション: 線量マッピング、無菌保証レベル、材料適合性試験を含む滅菌プロセスのバリデーション。
パフォーマンステスト: 電気的、機械的、環境的試験を実施し、製品のライフサイクルを通じて医療機器の要件を満たす性能を検証する。
薬事申請サポート
510(k) ドキュメンテーション: ケーブルグランドを組み込んだ医療機器のFDA 510(k)申請をサポートする技術文書。
テクニカルファイル: 欧州市場における医療機器規制(MDR)に基づくCEマーキングのための包括的な技術ファイル。
品質協定: 責任、仕様、およびコンプライアンス要件を定義する、サプライヤーとの正式な品質協定。
監査サポート: FDA、ノーティファイドボディ、顧客監査(文書審査、施設検査を含む)のサポート
クリーンルーム用途に必要な材料とは?
クリーンルーム用途では、低アウトガス特性、耐パーティクル発生性、洗浄剤との化学的適合性、滑らかな非多孔質表面、適切な導電性レベルを備えた材料が必要とされ、医療グレードのステンレス鋼316L、PEEK、PTFE、およびクリーンルーム認可の特殊ポリマーが、以下を満たしながら最適な性能を提供します。 ISO 146444 クリーンルーム規格と、管理された環境における電気的完全性の維持。
クリーンルームでは、製品の品質や無菌状態を損なう可能性のある微粒子や分子の汚染を厳密に管理する必要があるため、材料の選択は非常に重要である。
ステンレス鋼の要件
316Lメディカルグレード: 炭素含有量の少ないオーステナイト系ステンレス鋼で、医療用途に優れた耐食性と生体適合性を提供します。
電解研磨仕上げ: 電解研磨は、表面の凹凸を取り除き、パーティクルの発生を抑え、効果的な洗浄ができる滑らかな表面を作ります。
不動態化処理: 化学不動態化処理は耐食性を高め、変色やパーティクル発生の原因となる鉄汚染を除去する。
表面粗さ: 0.8マイクロメートル(32マイクロインチ)以下のRa値は、細菌の付着を最小限に抑え、洗浄および滅菌プロセスを容易にする。
高性能ポリマー
PEEK(ポリエーテルエーテルケトン): 優れた耐薬品性、低アウトガス性、生体適合性により、PEEKは医薬品および医療機器用途に理想的です。
PTFE(ポリテトラフルオロエチレン): 優れた耐薬品性と非粘着性により、洗浄用化学薬品や生物学的物質に対して優れた耐性を発揮します。
医療用ナイロン: USPクラスVIの認可を受けた特別調合ナイロンは、医療用途に優れた機械的特性と生体適合性を提供する。
クリーンルーム認定のPOM: パーティクルの発生が少なく、寸法安定性に優れたポリオキシメチレンは、精密クリーンルーム用途に適しています。
クリーンルーム分類適合性
ISOクラス5(クラス100): 半導体および医薬品製造用途向けに、パーティクルの発生を最小限に抑えた超平滑表面を実現。
ISOクラス6(クラス1000): 医療機器製造および一部の製薬工程における中程度の粒子制御。
ISOクラス7(クラス10000): 一般的な医薬品および医療機器の組立作業における標準的なクリーンルームの要件。
ISOクラス8(クラス100000): 包装および一部の医療機器製造工程における基本的なクリーンルーム要件。
アウトガスと汚染制御
低アウトガス素材: 繊細な工程や製品を汚染する可能性のある揮発性有機化合物(VOC)の排出を最小限に抑えた材料。
分子汚染: シリコーン、可塑剤、その他の有機化合物など、製品の品質に影響を及ぼす可能性のある分子汚染物質の管理。
イオン汚染: 電子部品や医薬品の汚染を防ぐため、イオン含有量の少ない材料を使用。
抽出可能な物質: 使用中に医薬品や洗浄液に溶出する可能性のある抽出性物質を最小限に抑える。
化学適合性マトリックス
| 洗浄剤 | 316L SS | 覗き見 | PTFE | メディカル・ナイロン |
|---|---|---|---|---|
| イソプロピルアルコール | 素晴らしい | 素晴らしい | 素晴らしい | グッド |
| 過酸化水素 | 素晴らしい | 素晴らしい | 素晴らしい | フェア |
| 第4級アンモニウム | 素晴らしい | 素晴らしい | 素晴らしい | グッド |
| 次亜塩素酸ナトリウム | グッド | 素晴らしい | 素晴らしい | 貧しい |
| 過酢酸 | グッド | 素晴らしい | 素晴らしい | 貧しい |
スイスの最先端製薬施設でオペレーションを管理するハッサン氏は、無菌注射剤製造用のISOクラス5クリーンルームのケーブルグランドをアップグレードする必要がありました。既存のケーブルグランドは、洗浄サイクル中に粒子を発生させ、新しい生物学的製剤に必要な積極的な滅菌プロトコルに耐えることができませんでした。私たちは、低パーティクル発生と洗浄・滅菌プロセスとの完全な化学的適合性が検証された電解研磨316Lステンレス鋼ケーブルグランドを提供しました。このアップグレードにより、粒子数はISOクラス5制限値以下の90%を達成し、洗浄関連の汚染事象を排除し、同社の新しい無菌製造ラインのバリデーションの成功をサポートしました。
適切な洗浄と滅菌の適合性を確保するには?
適切な洗浄と滅菌の適合性を確保するには、洗浄薬品や滅菌方法に繰り返しさらされることに耐える材料の選択、完全な洗浄性を実現する表面の設計、洗浄手順の検証、詳細な文書の管理が必要であり、医療用ケーブルグランドには、滑らかな隙間のない表面、耐薬品性のある材料、必要な無菌保証レベルを達成する検証済みの洗浄手順が求められます。
不適切な除染は、製品の汚染、患者の安全リスク、規制違反につながる可能性があるため、洗浄と滅菌の互換性は不可欠である。
滅菌方法の適合性
蒸気オートクレーブ: 材料は121℃~134℃に耐えること 蒸気オートクレーブ5 サイクルを、劣化や寸法変化、シールの不具合なしに行うことができる。
ガンマ線: 医療機器の滅菌に一般的に使用される25~50kGyのガンマ線量に対して、材料の劣化なしに耐性を示す。
エチレンオキシド(EtO): 滅菌剤に対する耐性や適切な脱気特性など、EtO滅菌との化学的適合性。
過酸化水素プラズマ: 材料の安定性と完全な滅菌剤の浸透を含む、低温プラズマ滅菌システムとの適合性。
洗浄バリデーション要件
クリーニングの手順: 効果的な除染に必要な化学物質、濃度、接触時間、機械的作用を明記した洗浄手順を文書化。
検証プロトコル: 最悪の汚染シナリオと分析試験を用いて、洗浄効果を実証する正式な検証研究。
合格基準: 目視検査、粒子数、バイオバーデン・レベル、化学物質残留限界など、清浄度の受け入れ基準を定義。
定期的なモニタリング: 継続的なモニタリングプログラムにより、洗浄効果の継続を確認し、性能の低下を特定する。
サーフェスデザインに関する考察
排水機能: 洗浄液の完全な排出を促し、汚染物質を溜め込まない設計。
アクセシビリティ: すべての表面は、医療施設で使用される標準的な清掃用具と手順で清掃できるようにしなければならない。
分解条件: 洗浄のためにグランドを分解する必要があるのか、そのままの洗浄で十分なのかを検討する。
ガスケットの交換: ガスケット交換の手順と、洗浄薬品への暴露によりシール部品の定期的な交換が必要な場合の検証。
ドキュメンテーションとコンプライアンス
洗浄方法: ステップごとの手順、薬品の仕様、安全上の注意を含む詳細な洗浄方法。
製品安全データ: 化学的適合性、温度限界、滅菌適合性を含む完全な材料安全情報。
検証レポート: 有効性を実証し、定期的なモニタリング要件を確立する洗浄バリデーション報告書。
トレーニング教材: 医療用ケーブル・グランドの適切な洗浄、取り扱い、保守手順に関する施設職員向け研修資料。
品質管理試験
バイオバーデン検査: 洗浄効果を検証し、潜在的な問題領域を特定するために、微生物汚染を定期的に検査する。
エンドトキシン検査: 医薬品や医療機器の用途において、発熱反応を引き起こす可能性のある細菌性内毒素の検査。
粒子計数: クリーンルームの要件が清掃・保守作業後も維持されていることを確認するための粒子数検査。
化学残留物の分析: 製品を汚染したり、生体適合性に影響を及ぼす可能性のある洗浄残留化学物質の試験。
医療用途別の主な選択基準とは?
主な選択基準は用途によって異なるが、規制遵守要件、生体適合性レベル、クリーンルームの分類、滅菌方法、化学物質への暴露、電気的性能のニーズなどがあり、外科用機器は最高の生体適合性を必要とし、医薬品製造は耐薬品性を必要とし、診断機器は電気的完全性を重視する一方、すべての用途で適切な規制認証と洗浄適合性が必要となる。
様々な医療用途には、最適な性能と規制遵守を確保するためにケーブルグランドを選択する際に注意深く考慮しなければならない独自の要件があります。
手術器具および患者接触器具
直接接触の要件: USPクラスVIの生体適合性を有し、外科手術中に患者に直接接触する材料については細胞毒性試験を追加。
滅菌の頻度: 劣化することなく頻繁な滅菌サイクルに耐える能力。通常、何百回もの滅菌サイクルを通して安定した材料を必要とする。
電気安全: 患者に接続される機器に対する低漏れ電流や信頼性の高い絶縁など、電気安全要件が強化されている。
緊急時の信頼性: 生命維持装置や救急医療装置など、故障が患者の安全に直接影響を及ぼす可能性のある装置に対する重要な信頼性要件。
医薬品製造
GMPコンプライアンス: 材料のトレーサビリティ、変更管理、バリデーション文書などの適正製造規範の要件。
製品接触の安全性: 溶出、粒子生成、化学的相互作用によって医薬品を汚染しない材料。
クリーニングの検証: 医薬品製造のための、文書化された手順と受入基準を伴う広範な洗浄バリデーション要件。
バッチドキュメンテーション: 医薬品製造装置で使用される材料の完全なバッチドキュメンテーションとトレーサビリティ。
診断・検査機器
精度の要件: 安定した機械的・電気的性能を必要とする分析機器向けの寸法安定性と精度。
耐薬品性: 診断用途で一般的に使用される実験用化学薬品、試薬、洗浄用溶剤に対する耐性。
EMCのパフォーマンス: 高感度分析機器および診断機器に対する電磁両立性要件。
校正の安定性: 長期にわたって機器の校正や測定精度に影響を与えない機械的安定性。
医療機器製造
プロセス・バリデーション: 医療機器製造のプロセスバリデーション要件をサポートする材料およびコンポーネント。
品質システム: サプライヤーの認定や受入検査手順を含むISO 13485品質システムとの統合。
リスク管理: 故障モード解析や緩和戦略など、医療機器のリスク管理要件をサポートする資料。
規制支援: 技術文書や規制に関する専門知識を含む、規制当局への申請に関するサプライヤーのサポート。
選考決定マトリクス
| アプリケーション・タイプ | 主要基準 | 二次基準 | クリティカル・スタンダード |
|---|---|---|---|
| 外科用機器 | 生体適合性 | 滅菌 | USPクラスVI、ISO 10993 |
| 医薬品 | 耐薬品性 | GMPコンプライアンス | FDA 21 CFR、cGMP |
| 診断 | 精密 | EMCパフォーマンス | IEC 61326, ISO 15189 |
| 製造業 | プロセス・バリデーション | 品質システム | ISO 13485、21 CFR 820 |
コスト・ベネフィット分析
イニシャルコストとライフサイクルの比較: 機器の耐用年数にわたって、メンテナンス、交換、コンプライアンスなどのコストを含めた総所有コストを検討する。
規制リスク: 法規制遵守のリスクおよび非遵守の潜在的コストと、材料コストのバランスをとる。
パフォーマンス要件: 選択した材料が、不必要にコストを増加させるようなオーバースペックになることなく、最低限の性能要件を満たすようにする。
サプライヤーの能力: 継続的なサポート、文書化、規制遵守の支援について、サプライヤーの能力を評価する。
結論
医療機器やクリーンルーム用のケーブルグランドを選択するには、これらの用途が標準的な工業用途とは異なる独自の規制、材料、および性能要件を理解する必要があります。成功するかどうかは、生体適合性、清浄性、規制遵守、および電気的性能のバランスにかかっています。
信頼性の高い医療用ケーブルグランド性能の鍵は、医療機器規制を理解し、適切な材料、文書、および製品ライフサイクル全体にわたる継続的サポートを提供できるサプライヤーと協力することにあります。Beptoでは、FDA要件および国際医療機器規格を満たす医療グレードのケーブルグランドを専門に扱っており、重要なヘルスケア用途に必要な品質保証と規制サポートを提供しています。
医療用ケーブルグランドに関するFAQ
Q: 医療用ケーブルグランドにはどのような資格が必要ですか?
A: 医療用ケーブルグランドは通常、USPクラスVI生体適合性認証、材料に関するFDA 21 CFRコンプライアンス、およびISO 13485製造品質システムを必要とします。具体的な要件は、お客様のアプリケーションと規制管轄区域によって異なります。
Q: 通常のステンレス鋼ケーブルグランドは、医療用途に使用できますか?
A: 通常のステンレス鋼は、医療要件を満たさない場合があります。医療用途では、電解研磨仕上げの医療用316Lステンレス鋼、生体適合性試験、規制遵守のための適切な文書が必要です。
Q: 医療用ケーブル・グランドの洗浄・滅菌方法は?
A: 承認された洗浄剤および滅菌方法を使用し、メーカーの検証済み洗浄手順に従ってください。ほとんどの医療用腺は、適切な材料適合性で蒸気オートクレーブ、ガンマ線照射、または化学滅菌に対応しています。
Q: クリーンルームと医療グレードのケーブルグランドの違いは何ですか?
A: メディカルグレードは生体適合性要件とFDAコンプライアンスを含み、クリーンルームグレードは粒子制御と耐薬品性に重点を置いている。用途によっては、医療用とクリーンルーム用の両方の仕様が必要となります。
Q: 医療用ケーブル腺はどれくらいの頻度で交換する必要がありますか?
A: 交換頻度は、滅菌サイクル、化学物質への曝露、メーカーの推奨事項によって異なる。通常、100~200滅菌サイクルごとに検査し、状態評価とバリデーション要件に基づいて交換する。



