Kegagalan sterilisasi perangkat medis merugikan produsen jutaan dolar per tahun, dengan 15-20% kegagalan disebabkan oleh ventilasi yang tidak memadai yang mencegah penetrasi sterilisasi yang tepat. Sumbat ventilasi standar gagal di bawah ini autoklaf1 suhu 121-134 ° C atau terdegradasi saat terkena sterilisasi etilen oksida (ETO)2 bahan kimia, yang mengorbankan jaminan sterilitas dan kepatuhan terhadap peraturan.
Sumbat ventilasi yang dapat disterilkan memungkinkan sterilisasi yang efektif dengan memungkinkan penetrasi uap atau gas ETO sambil mempertahankan penghalang steril setelah sterilisasi. Ventilasi membran PTFE tahan terhadap suhu autoklaf hingga 150 ° C dan tahan terhadap degradasi bahan kimia ETO, memastikan pemeliharaan sterilitas yang andal untuk peralatan medis, peralatan farmasi, dan instrumen laboratorium yang memerlukan proses sterilisasi yang divalidasi.
Tahun lalu, saya bekerja dengan Dr. Sarah Mitchell, direktur kualitas di produsen perangkat medis terkemuka di Boston, yang mengalami kegagalan validasi sterilisasi pada kemasan perangkat implan mereka. Sumbat ventilasi nilon standar mereka meleleh selama siklus autoklaf dan menghalangi penetrasi uap yang tepat. Setelah beralih ke sumbat ventilasi sterilisasi PTFE kelas farmasi kami dengan ketahanan suhu yang tervalidasi, mereka mencapai kemanjuran sterilisasi 100% di 1.000 siklus validasi - memastikan kepatuhan FDA dan keselamatan pasien! 🏥
Daftar Isi
- Apa Itu Sumbat Ventilasi yang Dapat Disterilkan dan Mengapa Sangat Penting?
- Bagaimana Metode Sterilisasi yang Berbeda Mempengaruhi Bahan Sumbat Ventilasi?
- Bahan Apa yang Terbaik untuk Sterilisasi Autoklaf?
- Bahan Apa yang Paling Cocok untuk Proses Sterilisasi ETO?
- Bagaimana Cara Memilih dan Memvalidasi Sumbat Ventilasi yang Dapat Disterilkan?
- Tanya Jawab Tentang Sumbat Ventilasi yang Dapat Disterilkan
Apa Itu Sumbat Ventilasi yang Dapat Disterilkan dan Mengapa Sangat Penting?
Memahami peran sumbat ventilasi yang dapat disterilkan dalam perangkat medis dan manufaktur farmasi sangat penting untuk menjaga jaminan sterilitas dan kepatuhan terhadap peraturan.
Sumbat ventilasi yang dapat disterilkan adalah ventilasi bernapas khusus yang dirancang untuk menahan proses sterilisasi sekaligus memungkinkan penetrasi steril dan mempertahankan penghalang steril. Sumbat ini memungkinkan perpindahan udara selama sterilisasi, mencegah pembentukan vakum selama pendinginan, dan mempertahankan kondisi steril setelah sterilisasi. Aplikasi penting termasuk pengemasan perangkat medis, wadah farmasi, peralatan laboratorium, dan peralatan pemrosesan steril.
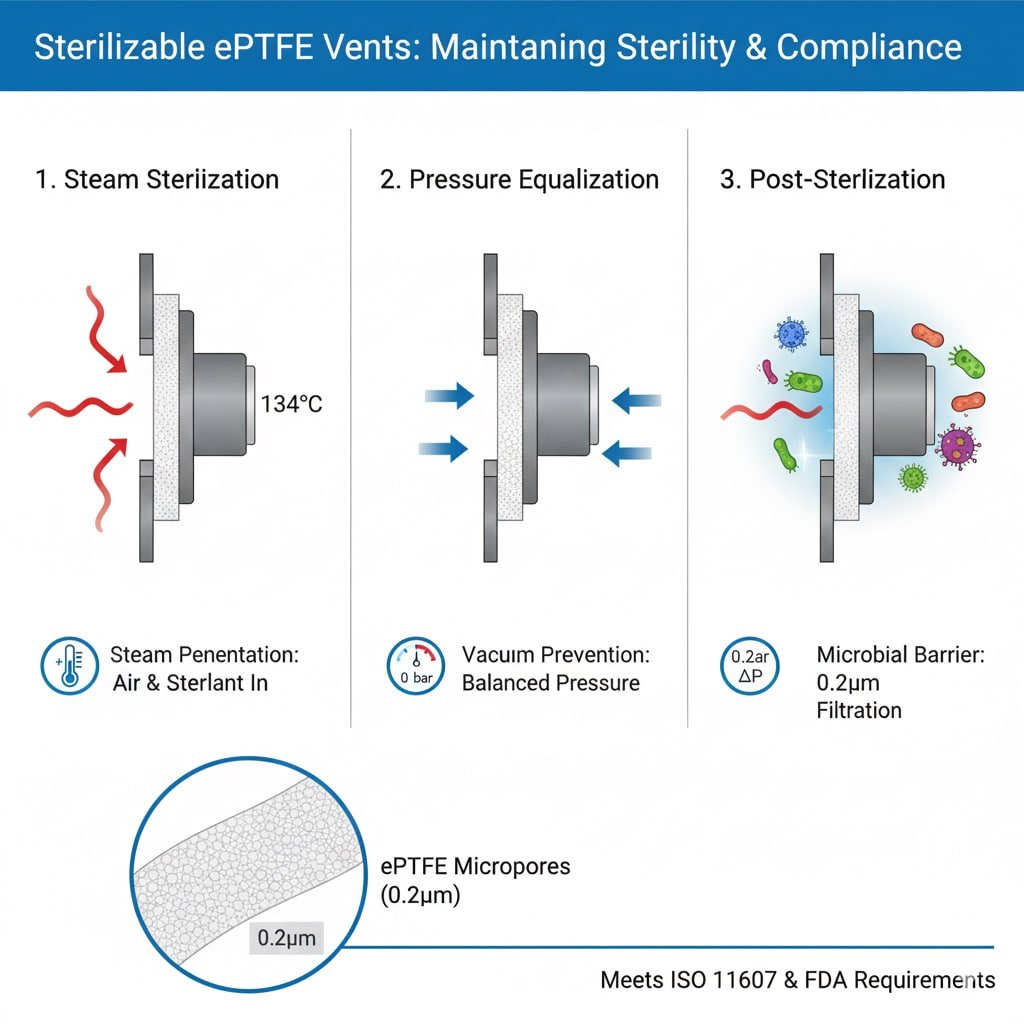
Persyaratan Proses Sterilisasi
Penetrasi Uap: Sterilisasi autoklaf membutuhkan uap untuk menembus kemasan dan menyentuh semua permukaan, sehingga membutuhkan ventilasi yang memungkinkan aliran gas sambil mempertahankan penghalang mikroba.
Perpindahan Udara: Sterilisasi yang efektif membutuhkan pembuangan udara secara menyeluruh dan penggantian dengan bahan steril, yang difasilitasi oleh ventilasi melalui pertukaran gas yang terkendali.
Pemerataan Tekanan: Siklus sterilisasi menciptakan perbedaan tekanan yang harus diakomodasi oleh ventilasi tanpa mengorbankan penghalang steril atau integritas kemasan.
Parameter Kinerja Kritis
Tahan Suhu: Ventilasi yang dapat disterilkan harus menjaga integritas struktural dan kinerja filtrasi pada suhu sterilisasi mulai dari 121°C hingga 150°C.
Kompatibilitas Bahan Kimia: Bahan harus tahan terhadap degradasi dari bahan kimia sterilisasi termasuk uap, etilen oksida, hidrogen peroksida, dan ozon.
Efisiensi Penghalang Mikroba: Pasca sterilisasi, ventilasi harus menyediakan penghalang mikroba3 dengan ukuran pori-pori biasanya 0,2-0,22 mikron untuk retensi bakteri.
Pertimbangan Kepatuhan terhadap Peraturan
Persyaratan Validasi FDA: Aplikasi perangkat medis memerlukan proses sterilisasi yang divalidasi dengan kinerja ventilasi yang terdokumentasi di seluruh siklus sterilisasi.
Kepatuhan terhadap Standar ISO: Ventilasi yang dapat disterilkan harus memenuhi ISO 116074 standar pengemasan dan persyaratan sterilisasi uap ISO 17665 untuk aplikasi medis.
Pengujian Biokompatibilitas: Aplikasi kontak perangkat medis mungkin memerlukan pengujian biokompatibilitas USP Kelas VI untuk jaminan keselamatan pasien.
Kategori Aplikasi
Pengemasan Perangkat Medis: Kemasan steril untuk implan, instrumen bedah, dan perangkat medis sekali pakai yang membutuhkan pemeliharaan sterilitas hingga digunakan.
Manufaktur Farmasi: Peralatan pemrosesan steril, bioreaktor, dan wadah farmasi yang membutuhkan proses sterilisasi yang tervalidasi.
Peralatan Laboratorium: Wadah laboratorium yang dapat diautoklaf, bejana kultur, dan peralatan analitik yang membutuhkan kondisi steril untuk hasil yang akurat.
Bagaimana Metode Sterilisasi yang Berbeda Mempengaruhi Bahan Sumbat Ventilasi?
Metode sterilisasi yang berbeda menciptakan tantangan unik untuk bahan sumbat ventilasi, yang membutuhkan sifat bahan tertentu dan pertimbangan desain untuk kinerja yang optimal.
Sterilisasi uap membuat bahan terkena suhu tinggi (121-134 ° C) dan kondisi uap jenuh yang dapat menyebabkan degradasi termal, perubahan dimensi, dan kerusakan membran. Sterilisasi ETO memaparkan bahan pada bahan kimia reaktif pada suhu yang lebih rendah (37-63°C) tetapi waktu pemaparan lebih lama yang dapat menyebabkan degradasi bahan kimia dan gas buang. Setiap metode memerlukan pemilihan bahan khusus untuk kinerja yang andal.
Efek Sterilisasi Uap
Tekanan Panas: Suhu tinggi menyebabkan ekspansi termal, potensi melelehnya komponen termoplastik, dan degradasi bahan yang sensitif terhadap suhu.
Reaksi Hidrolisis5: Paparan uap dapat menyebabkan degradasi hidrolitik pada polimer tertentu, terutama poliester dan beberapa poliamida.
Stabilitas Dimensi: Siklus termal berulang dapat menyebabkan perubahan dimensi yang memengaruhi kinerja penyegelan dan efisiensi penyaringan.
Tantangan Sterilisasi ETO
Reaktivitas Kimia: Etilen oksida bereaksi dengan bahan yang mengandung atom hidrogen aktif, yang berpotensi mengubah sifat bahan dan menciptakan residu beracun.
Persyaratan Pembuangan Gas Buang: Produk yang disterilkan dengan ETO memerlukan periode aerasi yang lebih lama untuk menghilangkan ETO yang terserap dan produk reaksi sebelum digunakan dengan aman.
Karakteristik Penetrasi: ETO memerlukan kondisi kelembapan dan suhu tertentu untuk penetrasi yang efektif, yang memengaruhi persyaratan desain ventilasi.
Efek Plasma Hidrogen Peroksida
Degradasi Oksidatif: Plasma H2O2 menciptakan spesies yang sangat reaktif yang dapat mendegradasi bahan organik melalui reaksi oksidasi.
Kompatibilitas Material: Banyak elastomer dan beberapa plastik tidak cocok dengan sterilisasi plasma H2O2 karena degradasi yang cepat.
Manfaat Suhu Rendah: Sterilisasi plasma beroperasi pada suhu rendah (45-55°C), sehingga mengurangi tekanan termal pada bahan yang sensitif terhadap suhu.
Pertimbangan Radiasi Gamma
Kerusakan Radiasi: Radiasi gamma berenergi tinggi dapat menyebabkan pemutusan rantai polimer atau ikatan silang, sehingga mengubah sifat material secara signifikan.
Akumulasi Dosis: Sterilisasi gamma berulang dapat menyebabkan kerusakan kumulatif, sehingga membatasi jumlah siklus sterilisasi yang dapat ditahan oleh bahan.
Persyaratan Antioksidan: Formulasi tahan radiasi sering kali membutuhkan antioksidan untuk mencegah degradasi oksidatif selama dan setelah penyinaran.
Baru-baru ini saya membantu Ahmed Al-Rashid, manajer operasi di sebuah fasilitas farmasi di Dubai, memecahkan masalah validasi sterilisasi ETO dengan sistem ventilasi bioreaktor mereka. Sumbat ventilasi standar mereka menyerap ETO dan membutuhkan periode aerasi 14 hari yang diperpanjang sehingga mengganggu jadwal produksi. Dengan menerapkan sumbat ventilasi PTFE kami yang kompatibel dengan ETO dengan karakteristik penyerapan minimal, mereka mengurangi waktu aerasi menjadi 24 jam sambil mempertahankan jaminan sterilitas penuh - secara dramatis meningkatkan efisiensi produksi! 🚀
Bahan Apa yang Terbaik untuk Sterilisasi Autoklaf?
Memilih bahan yang sesuai untuk sterilisasi autoklaf memerlukan pemahaman tentang stabilitas termal, ketahanan hidrolisis, dan kinerja jangka panjang dalam paparan uap berulang.
PTFE (polytetrafluoroethylene) menawarkan kinerja autoklaf yang unggul dengan suhu layanan terus menerus hingga 260 ° C, kelembaman kimiawi yang sangat baik, dan ketahanan terhadap hidrolisis. PVDF (polivinilidena fluorida) memberikan stabilitas termal yang baik hingga 150°C dengan biaya yang lebih rendah. Hindari nilon, polietilen standar, dan sebagian besar elastomer yang terdegradasi dalam kondisi autoklaf, sehingga mengorbankan kinerja penyaringan dan penyegelan.
Keuntungan Membran PTFE
Ketahanan Suhu yang Luar Biasa: PTFE mempertahankan integritas struktural dan kinerja filtrasi pada suhu yang jauh di atas kondisi autoklaf pada umumnya (121-134 ° C).
Kelambanan Kimiawi: PTFE tahan terhadap degradasi dari uap, bahan kimia pembersih, dan produk sampingan sterilisasi, sehingga memastikan kinerja jangka panjang yang konsisten.
Sifat Hidrofobik: Sifat hidrofobik PTFE mencegah penyerapan air dan menjaga stabilitas dimensi selama siklus sterilisasi.
Perbandingan Kinerja Material
| Bahan | Suhu Maks (°C) | Tahan Uap | Resistensi Hidrolisis | Faktor Biaya |
|---|---|---|---|---|
| PTFE | 260 | Luar biasa | Luar biasa | Tinggi |
| PVDF | 150 | Bagus. | Bagus. | Sedang |
| PP (Polypropylene) | 135 | Adil | Adil | Rendah |
| Nilon | 80-100 | Miskin | Miskin | Rendah |
Pemilihan Bahan Perumahan
Baja Tahan Karat 316L: Memberikan ketahanan korosi, stabilitas termal, dan kebersihan yang sangat baik untuk aplikasi farmasi dan medis yang memerlukan prosedur pembersihan yang tervalidasi.
MENGINTIP (Polietereterketon): Menawarkan stabilitas termal yang luar biasa (penggunaan terus menerus hingga 250°C) dengan ketahanan kimia yang sangat baik untuk aplikasi autoklaf yang berat.
Polypropylene: Pilihan hemat biaya untuk aplikasi sekali pakai dengan kinerja yang memadai untuk siklus autoklaf standar pada suhu 121°C.
Pertimbangan Komponen Penyegelan
Cincin-O EPDM: Memberikan ketahanan uap yang baik dan stabilitas termal untuk suhu hingga 150°C dengan kinerja penyegelan yang sangat baik.
Segel Silikon: Menawarkan ketahanan suhu yang unggul (hingga 200°C) tetapi mungkin memiliki masalah kompatibilitas dengan bahan kimia pembersih tertentu.
Cincin-O yang dienkapsulasi PTFE: Gabungkan ketahanan kimia PTFE dengan sifat penyegelan elastomer untuk aplikasi berat yang membutuhkan kedua karakteristik kinerja tersebut.
Optimalisasi Desain untuk Penggunaan Autoklaf
Akomodasi Ekspansi Termal: Desain ventilasi harus mengakomodasi ekspansi termal diferensial antara material untuk mencegah kegagalan seal selama siklus suhu.
Fitur Drainase: Desain drainase yang tepat mencegah akumulasi kondensat yang dapat mengganggu kinerja filtrasi atau menimbulkan risiko kontaminasi.
Dukungan Validasi: Fitur desain harus memfasilitasi pengujian validasi termasuk peluruhan tekanan, tantangan mikroba, dan verifikasi kinerja termal.
Bahan Apa yang Paling Cocok untuk Proses Sterilisasi ETO?
Sterilisasi ETO menghadirkan tantangan material unik yang membutuhkan kompatibilitas bahan kimia, penyerapan minimal, dan karakteristik gas buang yang cepat untuk pemrosesan yang efisien.
PTFE dan PVDF menawarkan kompatibilitas ETO yang sangat baik dengan penyerapan bahan kimia minimal dan gas buang yang cepat. Hindari bahan dengan situs hidrogen aktif seperti nilon, PVC, dan karet alam yang bereaksi dengan ETO membentuk senyawa beracun. Rumah baja tahan karat memberikan ketahanan kimiawi yang optimal, sementara segel silikon menawarkan kompatibilitas ETO yang baik dengan karakteristik gas buang yang dapat diterima untuk sebagian besar aplikasi.
Kompatibilitas Bahan Kimia ETO
Mekanisme Reaksi: ETO bereaksi dengan bahan yang mengandung gugus hidroksil, amino, karboksil, dan sulfhidril, membentuk turunan etilen glikol dan senyawa lain yang berpotensi beracun.
Karakteristik Penyerapan: Bahan dengan penyerapan ETO yang tinggi membutuhkan periode aerasi yang lebih lama, sehingga meningkatkan waktu dan biaya secara signifikan.
Kinetika Pembuangan Gas Buang: Bahan-bahan yang cepat mengeluarkan gas memungkinkan siklus aerasi yang lebih pendek, meningkatkan efisiensi proses dan mengurangi waktu penyimpanan inventaris.
Peringkat Kinerja ETO Material
Kompatibilitas ETO yang sangat baik:
- PTFE: Penyerapan minimal, pembuangan gas yang cepat, tidak ada reaktivitas kimiawi
- PVDF: Penyerapan rendah, pembuangan gas yang baik, ketahanan kimia yang sangat baik
- Baja Tahan Karat: Tidak ada penyerapan, kemampuan penggunaan langsung
Kompatibilitas ETO yang baik:
- Polypropylene: Penyerapan sedang, gas buang yang dapat diterima
- Silikon: Reaktivitas rendah, persyaratan gas buang sedang
Kompatibilitas ETO yang buruk:
- Nilon: Reaktivitas tinggi, diperlukan aerasi yang lebih lama
- PVC: Degradasi kimiawi, pembentukan senyawa beracun
- Karet Alam: Daya serap tinggi, potensi degradasi
Persyaratan Waktu Aerasi
| Bahan | Waktu Aerasi Khas | Tingkat Penyerapan ETO | Laju Gas Buang |
|---|---|---|---|
| PTFE | 8-24 jam | Minimal | Cepat |
| PVDF | 24-48 jam | Rendah | Bagus. |
| Polypropylene | 48-72 jam | Sedang | Sedang |
| Nilon | 7-14 hari | Tinggi | Lambat |
Pengoptimalan Parameter Proses
Kontrol Suhu: Sterilisasi ETO biasanya beroperasi pada suhu 37-63°C, sehingga membutuhkan bahan yang dapat mempertahankan performa pada rentang suhu ini.
Persyaratan Kelembaban: Efektivitas ETO memerlukan kelembaban relatif 40-80%, sehingga membutuhkan bahan yang bekerja secara konsisten dalam kondisi kelembaban ini.
Manajemen Konsentrasi Gas: Konsentrasi ETO 450-1200 mg/L membutuhkan bahan yang tahan terhadap serangan kimia sekaligus memungkinkan penetrasi sterilisasi.
Pertimbangan Validasi
Pengujian Residu: Produk yang disterilkan dengan ETO memerlukan pengujian residu ETO dan produk reaksi untuk memastikan kepatuhan terhadap batas keamanan.
Pemeliharaan Biokompatibilitas: Bahan harus mempertahankan biokompatibilitas setelah paparan ETO dan aerasi, sehingga membutuhkan pemilihan bahan yang tervalidasi.
Pemantauan Proses: Sterilisasi ETO memerlukan pemantauan suhu, kelembapan, tekanan, dan konsentrasi gas secara terus menerus selama siklus berlangsung.
Bagaimana Cara Memilih dan Memvalidasi Sumbat Ventilasi yang Dapat Disterilkan?
Pemilihan dan validasi sumbat ventilasi yang dapat disterilkan secara tepat memastikan kinerja sterilisasi yang andal, kepatuhan terhadap peraturan, dan keberhasilan operasional jangka panjang.
Pemilihan memerlukan pencocokan sifat material dengan metode sterilisasi, menentukan persyaratan kinerja, dan mempertimbangkan standar peraturan. Validasi melibatkan pengujian kinerja termal, studi tantangan mikroba, penilaian kompatibilitas bahan kimia, dan evaluasi stabilitas jangka panjang. Dokumentasikan semua pengujian sesuai dengan standar FDA dan ISO untuk pengajuan peraturan dan kepatuhan sistem mutu.
Kerangka Kerja Kriteria Seleksi
Kompatibilitas Metode Sterilisasi: Sesuaikan bahan ventilasi dengan metode sterilisasi tertentu (uap, ETO, plasma H2O2, gamma) berdasarkan persyaratan suhu, bahan kimia, dan ketahanan terhadap radiasi.
Spesifikasi Kinerja: Tentukan laju aliran yang diperlukan, peringkat tekanan, efisiensi filtrasi, dan sifat penghalang mikroba berdasarkan persyaratan aplikasi.
Persyaratan Peraturan: Pertimbangkan klasifikasi perangkat FDA, kepatuhan standar ISO, dan persyaratan biokompatibilitas untuk aplikasi penggunaan yang dimaksudkan.
Parameter Penilaian Aplikasi
Lingkungan Operasi: Mengevaluasi rentang suhu, paparan bahan kimia, kondisi tekanan, dan risiko kontaminasi di sepanjang siklus hidup produk.
Frekuensi Sterilisasi: Pertimbangkan penggunaan sekali pakai versus beberapa siklus sterilisasi dan efek kumulatif pada kinerja dan keandalan material.
Lingkup Validasi: Tentukan persyaratan pengujian berdasarkan penilaian risiko, jalur peraturan, dan persyaratan sistem mutu.
Protokol Pengujian Validasi
Pengujian Kinerja Termal:
- Siklus suhu pada kondisi sterilisasi
- Pengukuran stabilitas dimensi
- Verifikasi efisiensi filtrasi pasca-paparan termal
Pengujian Tantangan Mikroba:
- Tantangan bakteri dengan organisme uji yang sesuai
- Verifikasi pemeliharaan sterilitas
- Penilaian integritas penghalang jangka panjang
Penilaian Kompatibilitas Bahan Kimia:
- Evaluasi degradasi material
- Pengujian yang dapat diekstrak dan yang dapat dilindi
- Verifikasi pemeliharaan biokompatibilitas
Persyaratan Dokumentasi
Spesifikasi Bahan: Lembar data material yang lengkap termasuk komposisi kimia, sifat termal, dan sertifikasi peraturan.
Protokol Uji: Protokol validasi terperinci yang mengikuti panduan FDA dan standar ISO untuk validasi sterilisasi.
Data Kinerja: Hasil pengujian komprehensif yang menunjukkan kinerja di seluruh kondisi operasi dan siklus sterilisasi yang ditentukan.
Integrasi Sistem Mutu
Kualifikasi Pemasok: Menetapkan perjanjian kualitas pemasok termasuk ketertelusuran material, kontrol perubahan, dan persyaratan dokumentasi kualitas.
Inspeksi Masuk: Mengembangkan prosedur pemeriksaan untuk dimensi kritis, sifat material, dan verifikasi karakteristik kinerja.
Validasi Proses: Mengintegrasikan kinerja ventilasi ke dalam validasi proses sterilisasi secara keseluruhan termasuk pengujian skenario terburuk.
Pertimbangan Manajemen Risiko
Analisis Mode Kegagalan: Identifikasi mode kegagalan potensial termasuk degradasi material, kegagalan seal, dan kompromi filtrasi dengan strategi mitigasi yang tepat.
Kontrol Perubahan: Menetapkan prosedur untuk mengelola perubahan material, perubahan pemasok, dan modifikasi spesifikasi dengan persyaratan validasi ulang yang sesuai.
Pemantauan Berkelanjutan: Menerapkan program pemantauan berkelanjutan untuk memverifikasi kinerja yang berkelanjutan dan mengidentifikasi masalah potensial sebelum mempengaruhi kualitas produk.
Kesimpulan
Sumbat ventilasi yang dapat disterilkan memainkan peran penting dalam memastikan sterilisasi yang efektif sekaligus mempertahankan penghalang steril dalam aplikasi perangkat medis dan farmasi. Memahami tantangan unik dari berbagai metode sterilisasi dan memilih bahan yang sesuai sangat penting untuk kinerja yang andal dan kepatuhan terhadap peraturan.
Sumbat ventilasi berbasis PTFE menawarkan kinerja yang unggul di berbagai metode sterilisasi, memberikan ketahanan suhu yang sangat baik, kompatibilitas bahan kimia, dan keandalan jangka panjang. Pemilihan dan validasi yang tepat memastikan efektivitas sterilisasi yang optimal sekaligus meminimalkan waktu dan biaya pemrosesan.
Di Bepto, rangkaian lengkap sumbat ventilasi yang dapat disterilkan mencakup membran PTFE tingkat farmasi, kinerja suhu yang divalidasi, dan paket dokumentasi lengkap untuk pengajuan peraturan. Dengan pengalaman lebih dari satu dekade dalam aplikasi ventilasi khusus dan kemampuan manufaktur bersertifikasi ISO, kami menyediakan solusi andal dan hemat biaya yang Anda butuhkan untuk aplikasi sterilisasi kritis. Percayakan kepada kami untuk menjaga proses sterilisasi Anda tetap tervalidasi dan produk Anda tetap aman! 🔬
Tanya Jawab Tentang Sumbat Ventilasi yang Dapat Disterilkan
T: Dapatkah sumbat ventilasi yang sama digunakan untuk sterilisasi autoklaf dan ETO?
A: Ya, sumbat ventilasi membran PTFE dapat menangani sterilisasi autoklaf dan ETO secara efektif. PTFE menawarkan ketahanan suhu yang sangat baik untuk siklus autoklaf dan penyerapan ETO minimal untuk aerasi cepat, sehingga ideal untuk fasilitas yang menggunakan berbagai metode sterilisasi.
T: Berapa banyak siklus sterilisasi yang dapat ditahan oleh sumbat ventilasi?
A: Sumbat ventilasi PTFE berkualitas tinggi biasanya tahan terhadap 100+ siklus autoklaf atau 50+ siklus ETO dengan tetap mempertahankan kinerja penyaringan. Masa pakai siklus aktual tergantung pada parameter sterilisasi, prosedur penanganan, dan kriteria penerimaan kinerja untuk aplikasi spesifik Anda.
T: Berapa ukuran pori yang diperlukan untuk penyaringan steril dalam aplikasi medis?
A: Aplikasi medis biasanya membutuhkan ukuran pori 0,2 atau 0,22 mikron untuk retensi bakteri yang andal. Ukuran pori ini memberikan jaminan sterilitas yang tervalidasi sekaligus memungkinkan aliran gas yang memadai untuk sterilisasi yang efektif dan pemerataan tekanan.
T: Apakah sumbat ventilasi yang dapat disterilkan memerlukan pengujian validasi khusus?
A: Ya, sumbat ventilasi yang dapat disterilkan memerlukan pengujian validasi termasuk kinerja termal, tantangan mikroba, dan studi kompatibilitas bahan. Pengujian harus mengikuti panduan FDA dan standar ISO, dengan dokumentasi yang mendukung validasi proses sterilisasi dan pengajuan peraturan Anda.
T: Bagaimana Anda mencegah kontaminasi sumbat ventilasi selama sterilisasi?
A: Cegah kontaminasi melalui pemasangan yang benar, penutup pelindung selama penanganan, parameter sterilisasi yang divalidasi, dan penyimpanan pasca sterilisasi yang tepat. Gunakan teknik steril selama pemasangan dan pastikan sumbat ventilasi dirancang untuk metode sterilisasi spesifik dan persyaratan aplikasi Anda.
-
Pelajari prinsip-prinsip ilmiah sterilisasi autoklaf dan bagaimana uap jenuh di bawah tekanan digunakan untuk membunuh mikroorganisme secara efektif. ↩
-
Jelajahi proses kimiawi sterilisasi etilen oksida (ETO), metode suhu rendah yang digunakan untuk mensterilkan perangkat medis yang peka terhadap panas dan kelembapan. ↩
-
Temukan metode yang digunakan untuk menguji dan memvalidasi keefektifan penghalang mikroba, memastikan penghalang tersebut mencegah masuknya mikroorganisme dan menjaga sterilitas. ↩
-
Tinjau persyaratan utama standar ISO 11607, yang menetapkan bahan dan pengujian untuk sistem penghalang steril untuk perangkat medis. ↩
-
Memahami reaksi kimia hidrolisis dan bagaimana reaksi tersebut dapat menyebabkan degradasi bahan polimer tertentu ketika terpapar air atau uap pada suhu tinggi. ↩



