Pemilihan kelenjar kabel yang tidak tepat di lingkungan medis dan ruang bersih menyebabkan risiko kontaminasi, kegagalan kepatuhan terhadap peraturan, dan kerusakan peralatan yang mengakibatkan bahaya keselamatan pasien, penghentian fasilitas yang mahal, dan pelanggaran FDA, sementara penyegelan yang tidak memadai, bahan yang tidak sesuai, dan kebersihan yang buruk menyebabkan pertumbuhan bakteri, kontaminasi partikulat, dan pelanggaran sterilitas yang mengganggu operasi perawatan kesehatan yang kritis. Banyak manajer fasilitas yang kesulitan dalam memilih kelenjar yang memenuhi standar medis yang ketat sambil mempertahankan kinerja listrik yang andal.
Memilih kelenjar kabel untuk peralatan medis dan ruang bersih memerlukan pemahaman tentang peraturan FDA, USP Kelas VI1 persyaratan material, standar penyegelan IP68+, dan kebutuhan klasifikasi ruang bersih, dengan baja tahan karat kelas medis atau konstruksi polimer khusus yang memberikan biokompatibilitas, ketahanan terhadap bahan kimia, dan permukaan yang halus untuk pembersihan dan sterilisasi yang efektif sekaligus menjaga integritas listrik dalam aplikasi perawatan kesehatan yang kritis. Keberhasilan bergantung pada keseimbangan antara kepatuhan terhadap peraturan dengan keandalan operasional.
Setelah bekerja dengan para insinyur rumah sakit di berbagai pusat medis besar di Boston, produsen farmasi di Swiss, dan fasilitas kamar bersih di seluruh Singapura, saya telah belajar bahwa kelenjar kabel kelas medis sangat penting untuk menjaga lingkungan yang steril dan memastikan keselamatan pasien. Izinkan saya berbagi pengetahuan penting untuk memilih kelenjar yang optimal untuk aplikasi medis dan ruang bersih Anda.
Daftar Isi
- Apa yang Membuat Kelenjar Kabel Medis Berbeda dari Kelenjar Standar?
- Bagaimana Anda Memenuhi Peraturan FDA dan Perangkat Medis?
- Bahan Apa yang Diperlukan untuk Aplikasi Cleanroom?
- Bagaimana Anda Memastikan Kompatibilitas Pembersihan dan Sterilisasi yang Tepat?
- Apa Saja Kriteria Pemilihan Utama untuk Aplikasi Medis yang Berbeda?
- Tanya Jawab Tentang Kelenjar Kabel Medis
Apa yang Membuat Kelenjar Kabel Medis Berbeda dari Kelenjar Standar?
Kelenjar kabel medis berbeda dari kelenjar standar dengan menggunakan bahan yang biokompatibel, menampilkan permukaan yang dapat dibersihkan secara halus, memenuhi peraturan FDA, memberikan penyegelan yang disempurnakan untuk pencegahan kontaminasi, dan menawarkan ketahanan kimiawi terhadap bahan pembersih dan proses sterilisasi, dengan desain khusus yang menghilangkan celah di mana bakteri dapat bersarang sambil mempertahankan kinerja listrik di lingkungan perawatan kesehatan yang kritis.
Memahami perbedaan ini sangat penting karena aplikasi medis memiliki persyaratan keselamatan dan peraturan yang unik yang tidak dapat ditangani oleh kelenjar industri standar.
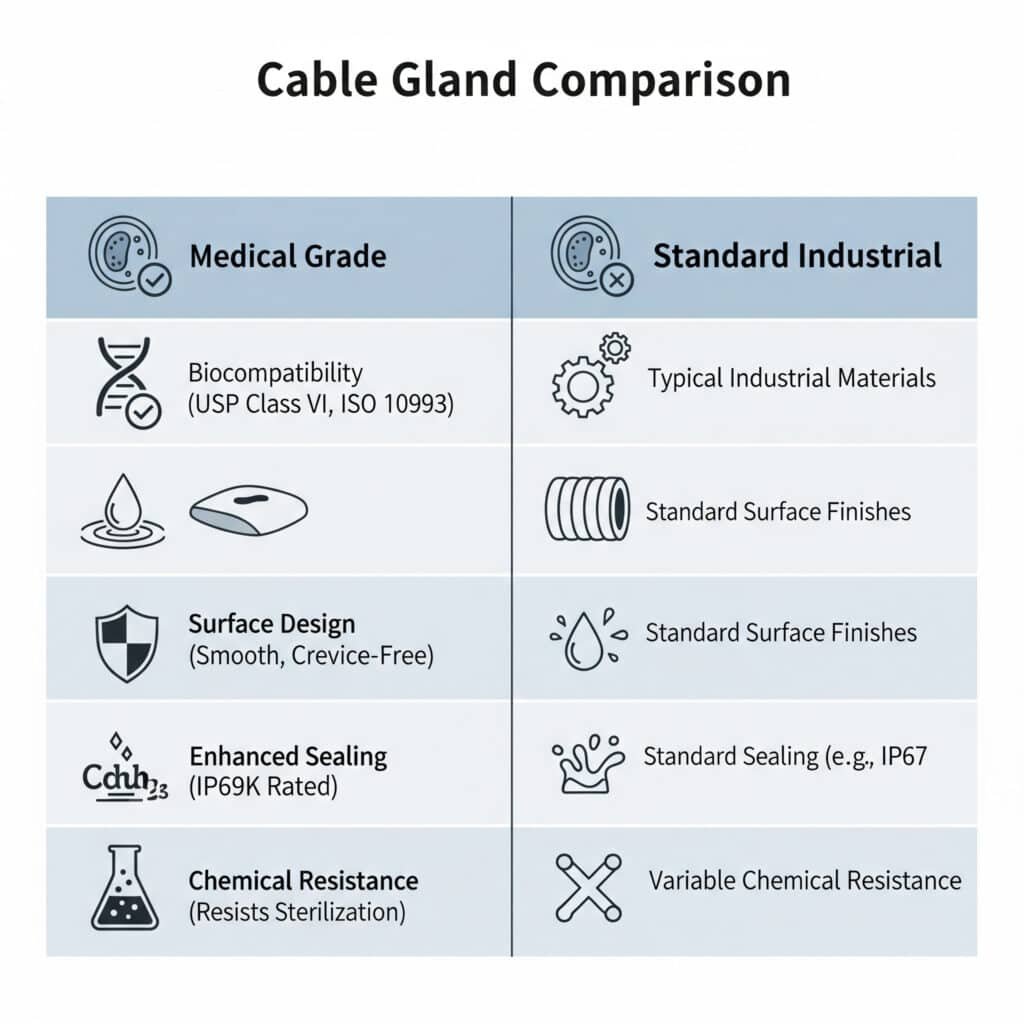
Persyaratan Biokompatibilitas
Kepatuhan USP Kelas VI: Kelenjar kabel medis harus menggunakan bahan yang lulus pengujian biologis United States Pharmacopeia Kelas VI untuk biokompatibilitas dan keamanan dalam aplikasi perangkat medis.
Standar ISO 10993: Bahan harus memenuhi ISO 109932 standar evaluasi biologis untuk perangkat medis, memastikan tidak ada efek sitotoksik, kepekaan, atau iritasi pada jaringan manusia.
Persetujuan FDA 21 CFR 177: Bahan food grade yang memenuhi peraturan FDA untuk kontak langsung dan tidak langsung dengan makanan sering kali diperlukan untuk aplikasi farmasi dan perangkat medis.
Polimer Biokompatibel: Bahan khusus seperti PEEK kelas medis, PTFE, atau nilon kelas farmasi memberikan biokompatibilitas tanpa mengorbankan sifat mekanis.
Desain Permukaan untuk Kebersihan
Permukaan akhir yang halus: Kelenjar medis memiliki permukaan yang sangat halus dengan nilai Ra biasanya di bawah 0,8 mikrometer untuk mencegah perlekatan bakteri dan memungkinkan pembersihan yang efektif.
Desain Bebas Celah: Menghilangkan sudut tajam, ulir yang dalam, dan geometri rumit yang dapat menampung bakteri atau menolak proses pembersihan dan sterilisasi.
Tepi Bulat: Semua permukaan eksternal memiliki tepi yang membulat dan transisi yang mulus untuk memudahkan pembersihan dan mencegah kerusakan pada sarung tangan kamar bersih atau kemasan steril.
Luas Permukaan Minimal: Desain yang ramping meminimalkan area permukaan yang terpapar kontaminasi sekaligus mempertahankan kinerja mekanis dan elektrik yang diperlukan.
Kinerja Penyegelan yang Ditingkatkan
Peringkat IP68+: Perlindungan lingkungan yang unggul melebihi standar IP68, sering kali mencapai IP69K untuk aplikasi pembersihan bertekanan tinggi dan bersuhu tinggi.
Hambatan Kontaminasi: Beberapa tahap penyegelan mencegah masuknya partikel, bakteri, dan bahan kimia pembersih yang dapat membahayakan lingkungan steril.
Tahan Tekanan: Peringkat tekanan yang ditingkatkan untuk menahan prosedur pembersihan yang agresif dan proses sterilisasi tanpa kegagalan seal.
Keandalan Jangka Panjang: Bahan penyegel menjaga integritas melalui siklus sterilisasi berulang dan paparan bahan kimia pembersih yang keras.
Sifat Ketahanan Kimia
Kompatibilitas Bahan Pembersih: Tahan terhadap disinfektan tingkat rumah sakit, senyawa amonium kuaterner, hidrogen peroksida, dan bahan kimia pembersih agresif lainnya.
Resistensi Sterilisasi: Bahan tahan terhadap radiasi gamma, etilen oksida, autoklaf uap, dan metode sterilisasi lainnya tanpa degradasi.
Bahan Kimia Farmasi: Ketahanan terhadap pelarut, asam, basa, dan senyawa farmasi yang biasa ditemukan di lingkungan manufaktur medis.
Stabilitas Suhu: Menjaga properti melalui siklus suhu sterilisasi dan persyaratan kontrol suhu ruang bersih.
David, seorang manajer fasilitas di pabrik manufaktur farmasi besar di New Jersey, menghadapi masalah kontaminasi yang berulang di jalur pengisian steril mereka di mana kelenjar kabel standar mengandung bakteri meskipun protokol pembersihan yang ketat. Kelenjar kuningan yang ada memiliki pola benang yang rumit dan permukaan akhir yang tidak dapat disterilkan secara memadai, yang menyebabkan penolakan batch dan masalah kepatuhan FDA. Kami menetapkan kelenjar kabel baja tahan karat kelas medis dengan permukaan yang dipoles listrik dan desain bebas celah yang memenuhi persyaratan USP Kelas VI. Peningkatan ini menghilangkan sumber kontaminasi, mencapai efektivitas pembersihan 99,9%, dan membantu fasilitas tersebut lulus inspeksi FDA sekaligus mengurangi tingkat penolakan produk sebesar 85%. 😊
Bagaimana Anda Memenuhi Peraturan FDA dan Perangkat Medis?
Memenuhi peraturan FDA dan perangkat medis mengharuskan penggunaan bahan dengan sertifikasi yang tepat, memelihara dokumentasi terperinci, berikut ini Praktik Produksi yang Baik (GMP)3memastikan ketertelusuran, dan menerapkan sistem kualitas yang sesuai dengan 21 CFR Bagian 820, dengan kelenjar kabel medis yang memerlukan bahan yang disetujui FDA, pengujian biokompatibilitas, dan kontrol produksi yang memastikan kualitas dan keamanan yang konsisten dalam aplikasi perangkat medis.
Kepatuhan terhadap peraturan tidak dapat dinegosiasikan dalam aplikasi medis karena kegagalan dapat menyebabkan bahaya bagi pasien, penarikan produk, dan konsekuensi hukum yang berat.
Persyaratan Bahan FDA
21 CFR Bagian 177: Bahan yang bersentuhan dengan obat-obatan atau perangkat medis harus memenuhi peraturan aditif makanan FDA untuk bahan yang bersentuhan dengan makanan secara tidak langsung.
Master Access File (MAF): Pemasok harus menyimpan File Akses Master FDA yang mendokumentasikan keamanan bahan, proses produksi, dan prosedur kontrol kualitas.
Berkas Induk Obat (Drug Master File, DMF): Untuk aplikasi farmasi, bahan mungkin memerlukan registrasi File Induk Obat dengan komposisi terperinci dan informasi manufaktur.
Sertifikat Kepatuhan: Pemasok harus memberikan sertifikat yang mengonfirmasi bahwa bahan memenuhi semua peraturan dan spesifikasi FDA yang berlaku.
Standar Kualitas Perangkat Medis
Kepatuhan ISO 13485: Manufaktur harus mengikuti sistem manajemen mutu perangkat medis ISO 13485 untuk desain, produksi, dan pengawasan pascapasar.
21 CFR Bagian 820 (QSR): Kepatuhan terhadap Peraturan Sistem Mutu yang memastikan kontrol desain yang tepat, kontrol dokumen, dan tindakan perbaikan/pencegahan.
Manajemen Risiko: Proses manajemen risiko ISO 14971 untuk perangkat medis, termasuk analisis risiko, evaluasi, dan tindakan pengendalian.
Kontrol Desain: Proses kontrol desain formal termasuk perencanaan desain, persyaratan input/output, tinjauan, verifikasi, dan validasi.

Dokumentasi dan Penelusuran
Sertifikat Material: Ketertelusuran bahan lengkap dengan sertifikat analisis, hasil uji biokompatibilitas, dan dokumentasi kepatuhan terhadap peraturan.
Catatan Manufaktur: Catatan produksi yang terperinci termasuk parameter proses, pengujian kontrol kualitas, dan dokumentasi batch untuk penelusuran penuh.
Kontrol Perubahan: Prosedur pengendalian perubahan formal untuk setiap modifikasi bahan, proses, atau spesifikasi yang memengaruhi kepatuhan terhadap peraturan.
Kualifikasi Pemasok: Program kualifikasi pemasok yang komprehensif untuk memastikan semua bahan dan komponen memenuhi persyaratan perangkat medis.
Persyaratan Validasi
Pengujian Biokompatibilitas: Pengujian USP Kelas VI termasuk uji injeksi sistemik, intrakutan, dan implantasi untuk memverifikasi keamanan biologis.
Validasi Pembersihan: Prosedur pembersihan yang terdokumentasi dengan data validasi yang membuktikan pembuangan kontaminan dan pengurangan beban biologis yang efektif.
Validasi Sterilisasi: Validasi proses sterilisasi termasuk pemetaan dosis, tingkat jaminan sterilitas, dan studi kompatibilitas bahan.
Pengujian Kinerja: Pengujian kelistrikan, mekanis, dan lingkungan untuk memverifikasi kinerja yang memenuhi persyaratan perangkat medis di seluruh siklus hidup produk.
Dukungan Pengajuan Peraturan
Dokumentasi 510(k): Dokumentasi teknis yang mendukung pengajuan FDA 510(k) untuk perangkat medis yang menggunakan kelenjar kabel.
File Teknis: File teknis yang komprehensif untuk penandaan CE berdasarkan Peraturan Perangkat Medis (Medical Device Regulation/MDR) di pasar Eropa.
Perjanjian Kualitas: Perjanjian kualitas formal dengan pemasok yang menetapkan tanggung jawab, spesifikasi, dan persyaratan kepatuhan.
Dukungan Audit: Dukungan untuk audit FDA, badan yang diberitahukan, dan audit pelanggan termasuk tinjauan dokumentasi dan inspeksi fasilitas.
Bahan Apa yang Diperlukan untuk Aplikasi Cleanroom?
Aplikasi ruang bersih memerlukan bahan dengan sifat gas buang rendah, ketahanan terhadap pembentukan partikel, kompatibilitas bahan kimia dengan bahan pembersih, permukaan tidak berpori yang halus, dan tingkat konduktivitas yang sesuai, dengan baja tahan karat kelas medis 316L, PEEK, PTFE, dan polimer khusus yang disetujui ruang bersih yang memberikan kinerja optimal sekaligus memenuhi ISO 146444 standar ruang bersih dan menjaga integritas listrik di lingkungan yang terkendali.
Pemilihan bahan sangat penting karena ruang bersih memerlukan kontrol ketat terhadap kontaminasi partikulat dan molekuler yang dapat membahayakan kualitas produk atau kondisi steril.
Persyaratan Baja Tahan Karat
Kelas Medis 316L: Baja tahan karat austenitik dengan kandungan karbon rendah yang memberikan ketahanan korosi dan biokompatibilitas yang unggul untuk aplikasi medis.
Hasil akhir yang dipoles dengan listrik: Electropolishing menghilangkan ketidaksempurnaan permukaan, mengurangi pembentukan partikel, dan menciptakan permukaan yang halus untuk pembersihan yang efektif.
Perawatan Pasif: Pasifasi kimiawi meningkatkan ketahanan terhadap korosi dan menghilangkan kontaminasi besi yang dapat menyebabkan perubahan warna atau pembentukan partikel.
Kekasaran Permukaan: Nilai Ra di bawah 0,8 mikrometer (32 mikroinchi) meminimalkan perlekatan bakteri dan memudahkan proses pembersihan dan sterilisasi.
Polimer Berkinerja Tinggi
MENGINTIP (Polietereterketon): Ketahanan kimiawi yang sangat baik, gas buang yang rendah, dan biokompatibilitas membuat PEEK ideal untuk aplikasi perangkat farmasi dan medis.
PTFE (Polytetrafluoroethylene): Sifat kelembaman kimiawi dan anti lengket yang unggul memberikan ketahanan yang sangat baik terhadap bahan kimia pembersih dan bahan biologis.
Nilon Kelas Medis: Nilon yang diformulasikan secara khusus dengan persetujuan USP Kelas VI menawarkan sifat mekanik yang baik dengan biokompatibilitas untuk aplikasi medis.
POM yang Disetujui di Ruang Bersih: Polioksimetilena dengan generasi partikel rendah dan stabilitas dimensi yang baik untuk aplikasi ruang bersih yang presisi.
Kompatibilitas Klasifikasi Ruang Bersih
ISO Kelas 5 (Kelas 100): Permukaan yang sangat halus dengan partikel yang dihasilkan minimal untuk aplikasi manufaktur semikonduktor dan farmasi.
ISO Kelas 6 (Kelas 1000): Kontrol partikel sedang untuk pembuatan perangkat medis dan beberapa proses farmasi.
ISO Kelas 7 (Kelas 10000): Persyaratan ruang bersih standar untuk operasi perakitan perangkat farmasi dan medis secara umum.
ISO Kelas 8 (Kelas 100000): Persyaratan ruang bersih dasar untuk pengemasan dan beberapa proses pembuatan perangkat medis.
Pengendalian Gas Buang dan Kontaminasi
Bahan-bahan yang menghasilkan gas buang rendah: Bahan dengan emisi senyawa organik mudah menguap (VOC) minimal yang dapat mencemari proses atau produk yang sensitif.
Kontaminasi Molekuler: Pengendalian kontaminan molekuler termasuk silikon, pemlastis, dan senyawa organik lainnya yang dapat memengaruhi kualitas produk.
Kontaminasi Ionik: Bahan dengan kandungan ionik rendah untuk mencegah kontaminasi komponen elektronik dan produk farmasi.
Zat yang Dapat Diekstraksi: Zat yang dapat diekstraksi minimal yang dapat larut ke dalam produk farmasi atau larutan pembersih selama penggunaan.
Matriks Kompatibilitas Bahan Kimia
| Agen Pembersih | 316L SS | MENGINTIP | PTFE | Nilon Medis |
|---|---|---|---|---|
| Isopropil Alkohol | Luar biasa | Luar biasa | Luar biasa | Bagus. |
| Hidrogen Peroksida | Luar biasa | Luar biasa | Luar biasa | Adil |
| Amonium Kuarter | Luar biasa | Luar biasa | Luar biasa | Bagus. |
| Natrium Hipoklorit | Bagus. | Luar biasa | Luar biasa | Miskin |
| Asam Perasetat | Bagus. | Luar biasa | Luar biasa | Miskin |
Hassan, yang mengelola operasi di fasilitas farmasi canggih di Swiss, perlu meningkatkan kelenjar kabel di kamar bersih ISO Kelas 5 untuk pembuatan injeksi steril. Kelenjar yang ada menghasilkan partikel selama siklus pembersihan dan tidak dapat menahan protokol sterilisasi agresif yang diperlukan untuk produk biologis baru mereka. Kami menyediakan kelenjar kabel baja tahan karat 316L yang dipoles secara elektropolesan dengan generasi partikel rendah yang tervalidasi dan kompatibilitas bahan kimia yang lengkap dengan proses pembersihan dan sterilisasi. Peningkatan ini mencapai jumlah partikel 90% di bawah batas ISO Kelas 5, menghilangkan peristiwa kontaminasi terkait pembersihan, dan mendukung validasi yang berhasil dari lini produksi steril mereka yang baru.
Bagaimana Anda Memastikan Kompatibilitas Pembersihan dan Sterilisasi yang Tepat?
Memastikan kompatibilitas pembersihan dan sterilisasi yang tepat memerlukan pemilihan bahan yang tahan terhadap paparan berulang terhadap bahan kimia pembersih dan metode sterilisasi, mendesain permukaan agar dapat dibersihkan secara menyeluruh, memvalidasi prosedur pembersihan, dan memelihara dokumentasi terperinci, dengan kelenjar kabel medis yang memerlukan permukaan bebas celah yang halus, bahan tahan bahan kimia, dan protokol pembersihan tervalidasi yang mencapai tingkat jaminan kemandulan yang diperlukan.
Kompatibilitas pembersihan dan sterilisasi sangat penting karena dekontaminasi yang tidak memadai dapat menyebabkan kontaminasi produk, risiko keselamatan pasien, dan pelanggaran peraturan.
Kompatibilitas Metode Sterilisasi
Autoklaf Uap: Bahan harus tahan terhadap suhu 121°C-134°C autoklaf uap5 siklus tanpa degradasi, perubahan dimensi, atau kegagalan seal.
Radiasi Gamma: Ketahanan terhadap dosis radiasi gamma 25-50 kGy yang biasa digunakan untuk sterilisasi perangkat medis tanpa degradasi material.
Etilen Oksida (EtO): Kompatibilitas kimiawi dengan sterilisasi EtO termasuk ketahanan terhadap sterilisasi dan karakteristik degassing yang tepat.
Plasma Hidrogen Peroksida: Kompatibilitas dengan sistem sterilisasi plasma suhu rendah termasuk stabilitas material dan penetrasi sterilisasi yang lengkap.
Persyaratan Validasi Pembersihan
Prosedur Pembersihan: Prosedur pembersihan terdokumentasi yang menetapkan bahan kimia, konsentrasi, waktu kontak, dan tindakan mekanis yang diperlukan untuk dekontaminasi yang efektif.
Protokol Validasi: Studi validasi formal yang menunjukkan efektivitas pembersihan dengan menggunakan skenario kontaminasi terburuk dan pengujian analitis.
Kriteria Penerimaan: Kriteria penerimaan yang ditetapkan untuk kebersihan termasuk inspeksi visual, jumlah partikel, tingkat bioburden, dan batas residu bahan kimia.
Pemantauan Rutin: Program pemantauan yang sedang berlangsung untuk memverifikasi efektivitas pembersihan yang berkelanjutan dan mengidentifikasi penurunan kinerja.
Pertimbangan Desain Permukaan
Fitur Drainase: Fitur desain yang mendorong pengurasan larutan pembersih secara menyeluruh dan mencegah terjadinya genangan air yang dapat menimbulkan kontaminan.
Aksesibilitas: Semua permukaan harus dapat diakses untuk dibersihkan dengan alat dan prosedur pembersihan standar yang digunakan di fasilitas medis.
Persyaratan Pembongkaran: Pertimbangkan apakah kelenjar perlu dibongkar untuk dibersihkan atau apakah pembersihan secara utuh sudah cukup untuk aplikasi tersebut.
Penggantian Gasket: Prosedur untuk penggantian gasket dan validasi ketika komponen penyegelan memerlukan penggantian secara berkala karena paparan bahan kimia pembersih.
Dokumentasi dan Kepatuhan
Petunjuk Pembersihan: Petunjuk pembersihan terperinci termasuk prosedur langkah demi langkah, spesifikasi bahan kimia, dan tindakan pencegahan keselamatan.
Data Keamanan Bahan: Informasi keamanan material yang lengkap termasuk kompatibilitas bahan kimia, batas suhu, dan kompatibilitas sterilisasi.
Laporan Validasi: Membersihkan laporan validasi yang menunjukkan efektivitas dan menetapkan persyaratan pemantauan rutin.
Materi Pelatihan: Materi pelatihan untuk personel fasilitas tentang prosedur pembersihan, penanganan, dan pemeliharaan yang tepat untuk kelenjar kabel medis.
Pengujian Kontrol Kualitas
Pengujian Bioburden: Pengujian rutin untuk kontaminasi mikroba untuk memverifikasi efektivitas pembersihan dan mengidentifikasi area yang berpotensi menimbulkan masalah.
Pengujian Endotoksin: Pengujian endotoksin bakteri yang dapat menyebabkan reaksi pirogenik pada aplikasi farmasi dan perangkat medis.
Penghitungan Partikel: Pengujian jumlah partikel untuk memverifikasi persyaratan ruang bersih dipertahankan setelah kegiatan pembersihan dan pemeliharaan.
Analisis Residu Kimia: Pengujian untuk membersihkan residu bahan kimia yang dapat mencemari produk atau memengaruhi biokompatibilitas.
Apa Saja Kriteria Pemilihan Utama untuk Aplikasi Medis yang Berbeda?
Kriteria pemilihan utama bervariasi berdasarkan aplikasi, tetapi mencakup persyaratan kepatuhan terhadap peraturan, tingkat biokompatibilitas, klasifikasi ruang bersih, metode sterilisasi, paparan bahan kimia, dan kebutuhan kinerja kelistrikan, dengan peralatan bedah yang membutuhkan biokompatibilitas tertinggi, manufaktur farmasi yang membutuhkan ketahanan terhadap bahan kimia, dan peralatan diagnostik yang berfokus pada integritas kelistrikan, sementara semua aplikasi memerlukan sertifikasi peraturan yang sesuai dan kompatibilitas pembersihan.
Aplikasi medis yang berbeda memiliki persyaratan unik yang harus dipertimbangkan dengan cermat selama pemilihan kelenjar kabel untuk memastikan kinerja yang optimal dan kepatuhan terhadap peraturan.
Peralatan Bedah dan Kontak Pasien
Persyaratan Kontak Langsung: Biokompatibilitas USP Kelas VI dengan pengujian sitotoksisitas tambahan untuk bahan yang bersentuhan langsung dengan pasien selama prosedur pembedahan.
Frekuensi Sterilisasi: Kemampuan untuk menahan siklus sterilisasi yang sering tanpa degradasi, biasanya membutuhkan bahan yang stabil melalui ratusan siklus sterilisasi.
Keamanan Listrik: Persyaratan keselamatan listrik yang ditingkatkan termasuk arus bocor yang rendah dan insulasi yang andal untuk peralatan yang terhubung dengan pasien.
Keandalan Darurat: Persyaratan keandalan yang penting untuk peralatan medis penunjang kehidupan dan darurat di mana kegagalan dapat berdampak langsung pada keselamatan pasien.
Manufaktur Farmasi
Kepatuhan GMP: Persyaratan Praktik Manufaktur yang Baik termasuk penelusuran material, kontrol perubahan, dan dokumentasi validasi.
Keamanan Kontak Produk: Bahan yang tidak akan mencemari produk farmasi melalui pencucian, pembentukan partikel, atau interaksi kimiawi.
Validasi Pembersihan: Persyaratan validasi pembersihan yang ekstensif dengan prosedur terdokumentasi dan kriteria penerimaan untuk manufaktur farmasi.
Dokumentasi Batch: Dokumentasi dan penelusuran bets lengkap untuk bahan yang digunakan dalam peralatan manufaktur farmasi.
Peralatan Diagnostik dan Laboratorium
Persyaratan Presisi: Stabilitas dan presisi dimensi untuk instrumen analitik yang membutuhkan performa mekanik dan elektrik yang konsisten.
Resistensi Kimia: Ketahanan terhadap bahan kimia laboratorium, reagen, dan pelarut pembersih yang biasa digunakan dalam aplikasi diagnostik.
Kinerja EMC: Persyaratan kompatibilitas elektromagnetik untuk instrumen analitik dan peralatan diagnostik yang sensitif.
Stabilitas Kalibrasi: Stabilitas mekanis yang tidak akan memengaruhi kalibrasi instrumen atau akurasi pengukuran dari waktu ke waktu.
Manufaktur Alat Kesehatan
Validasi Proses: Bahan dan komponen yang mendukung persyaratan validasi proses untuk pembuatan perangkat medis.
Sistem Kualitas: Integrasi dengan sistem mutu ISO 13485 termasuk kualifikasi pemasok dan prosedur inspeksi masuk.
Manajemen Risiko: Materi yang mendukung persyaratan manajemen risiko perangkat medis, termasuk analisis modus kegagalan dan strategi mitigasi.
Dukungan Regulasi: Dukungan pemasok untuk pengajuan peraturan termasuk dokumentasi teknis dan keahlian peraturan.
Matriks Keputusan Pemilihan
| Jenis Aplikasi | Kriteria Utama | Kriteria Sekunder | Standar Kritis |
|---|---|---|---|
| Peralatan Bedah | Biokompatibilitas | Sterilisasi | USP Kelas VI, ISO 10993 |
| Farmasi | Resistensi Kimia | Kepatuhan GMP | FDA 21 CFR, cGMP |
| Diagnostik | Presisi | Kinerja EMC | IEC 61326, ISO 15189 |
| Manufaktur | Validasi Proses | Sistem Kualitas | ISO 13485, 21 CFR 820 |
Analisis Biaya-Manfaat
Biaya Awal vs Siklus Hidup: Pertimbangkan total biaya kepemilikan termasuk biaya pemeliharaan, penggantian, dan kepatuhan selama masa pakai peralatan.
Risiko Regulasi: Menyeimbangkan biaya material terhadap risiko kepatuhan terhadap peraturan dan potensi biaya ketidakpatuhan.
Persyaratan Kinerja: Pastikan bahan yang dipilih memenuhi persyaratan kinerja minimum tanpa spesifikasi berlebihan yang meningkatkan biaya yang tidak perlu.
Kemampuan Pemasok: Mengevaluasi kemampuan pemasok untuk mendapatkan dukungan, dokumentasi, dan bantuan kepatuhan terhadap peraturan yang berkelanjutan.
Kesimpulan
Memilih kelenjar kabel untuk peralatan medis dan ruang bersih membutuhkan pemahaman tentang persyaratan peraturan, material, dan kinerja yang unik yang membedakan aplikasi ini dari penggunaan industri standar. Keberhasilan bergantung pada keseimbangan biokompatibilitas, kebersihan, kepatuhan terhadap peraturan, dan kinerja kelistrikan.
Kunci kinerja kelenjar kabel medis yang andal terletak pada kerja sama dengan pemasok yang memahami peraturan perangkat medis dan dapat menyediakan bahan, dokumentasi, dan dukungan berkelanjutan yang sesuai selama siklus hidup produk. Di Bepto, kami mengkhususkan diri pada kelenjar kabel kelas medis yang memenuhi persyaratan FDA dan standar perangkat medis internasional, memberikan jaminan kualitas dan dukungan regulasi yang diperlukan untuk aplikasi perawatan kesehatan yang kritis.
Tanya Jawab Tentang Kelenjar Kabel Medis
T: Sertifikasi apa yang saya perlukan untuk kelenjar kabel medis?
A: Kelenjar kabel medis biasanya memerlukan sertifikasi biokompatibilitas USP Kelas VI, kepatuhan FDA 21 CFR untuk bahan, dan sistem kualitas manufaktur ISO 13485. Persyaratan khusus tergantung pada aplikasi dan yurisdiksi peraturan Anda.
T: Dapatkah kelenjar kabel baja tahan karat biasa digunakan dalam aplikasi medis?
A: Baja tahan karat biasa mungkin tidak memenuhi persyaratan medis. Aplikasi medis membutuhkan baja tahan karat kelas medis 316L dengan lapisan akhir yang dipoles listrik, pengujian biokompatibilitas, dan dokumentasi yang tepat untuk kepatuhan terhadap peraturan.
T: Bagaimana cara membersihkan dan mensterilkan kelenjar kabel medis?
A: Ikuti prosedur pembersihan yang telah divalidasi oleh produsen dengan menggunakan bahan pembersih dan metode sterilisasi yang disetujui. Sebagian besar kelenjar medis mendukung autoklaf uap, radiasi gamma, atau sterilisasi kimiawi dengan kompatibilitas bahan yang tepat.
T: Apa perbedaan antara kelenjar kabel ruang bersih dan kelas medis?
A: Kelas medis mencakup persyaratan biokompatibilitas dan kepatuhan terhadap FDA, sedangkan kelas ruang bersih berfokus pada kontrol partikel dan ketahanan terhadap bahan kimia. Beberapa aplikasi memerlukan spesifikasi medis dan ruang bersih.
T: Seberapa sering kelenjar kabel medis harus diganti?
A: Frekuensi penggantian tergantung pada siklus sterilisasi, paparan bahan kimia, dan rekomendasi produsen. Biasanya, periksa setelah setiap 100-200 siklus sterilisasi dan ganti berdasarkan penilaian kondisi dan persyaratan validasi.
-
Pelajari tentang uji reaktivitas biologis spesifik yang diperlukan untuk sertifikasi USP Kelas VI. ↩
-
Akses ikhtisar seri standar ISO 10993 untuk evaluasi biologis perangkat medis. ↩
-
Tinjau pedoman dan peraturan resmi FDA untuk Praktik Produksi yang Baik (cGMP) saat ini. ↩
-
Jelajahi panduan terperinci tentang standar ISO 14644 untuk mengklasifikasikan kebersihan udara di kamar bersih. ↩
-
Memahami prinsip-prinsip sterilisasi uap, termasuk peran waktu, suhu, dan tekanan. ↩



