Les échecs de stérilisation des dispositifs médicaux coûtent des millions de dollars aux fabricants chaque année, 15-20% des échecs étant attribués à une ventilation inadéquate qui empêche la pénétration correcte de l'agent stérilisant. Les bouchons d'aération standard échouent sous autoclave1 des températures de 121-134°C ou se dégrader lorsqu'il est exposé à des stérilisation à l'oxyde d'éthylène (ETO)2 des produits chimiques, ce qui compromet l'assurance de la stérilité et la conformité aux réglementations.
Les bouchons d'évent stérilisables permettent une stérilisation efficace en autorisant la pénétration de vapeur ou de gaz ETO tout en maintenant des barrières stériles après la stérilisation. Les évents à membrane PTFE supportent des températures d'autoclave allant jusqu'à 150°C et résistent à la dégradation chimique de l'ETO, ce qui garantit un maintien fiable de la stérilité des dispositifs médicaux, des équipements pharmaceutiques et des instruments de laboratoire nécessitant des processus de stérilisation validés.
L'année dernière, j'ai travaillé avec le Dr Sarah Mitchell, directrice de la qualité d'un grand fabricant de dispositifs médicaux à Boston, qui connaissait des échecs de validation de la stérilisation sur l'emballage de ses dispositifs implantables. Leurs bouchons d'évent en nylon standard fondaient pendant les cycles d'autoclave et empêchaient la pénétration correcte de la vapeur. Après avoir opté pour nos bouchons d'évent stérilisables en PTFE de qualité pharmaceutique, dont la résistance à la température a été validée, ils ont obtenu une efficacité de stérilisation de 100% sur 1 000 cycles de validation - garantissant ainsi la conformité à la FDA et la sécurité des patients ! 🏥
Table des matières
- Qu'est-ce qu'un bouchon d'évent stérilisable et pourquoi est-il essentiel ?
- Comment les différentes méthodes de stérilisation affectent-elles les matériaux des bouchons d'évent ?
- Quels sont les meilleurs matériaux pour la stérilisation en autoclave ?
- Quels sont les matériaux qui conviennent le mieux aux processus de stérilisation ETO ?
- Comment sélectionner et valider les bouchons d'évent stérilisables ?
- FAQ sur les bouchons d'évent stérilisables
Qu'est-ce qu'un bouchon d'évent stérilisable et pourquoi est-il essentiel ?
Il est essentiel de comprendre le rôle des bouchons d'évent stérilisables dans la fabrication des dispositifs médicaux et des produits pharmaceutiques pour maintenir l'assurance de la stérilité et la conformité aux réglementations.
Les bouchons d'évent stérilisables sont des évents respirants spécialisés conçus pour résister aux processus de stérilisation tout en permettant la pénétration des stérilisants et en maintenant les barrières stériles. Ils permettent le déplacement de l'air pendant la stérilisation, empêchent la formation de vide pendant le refroidissement et maintiennent des conditions stériles après la stérilisation. Les applications critiques comprennent l'emballage des dispositifs médicaux, les conteneurs pharmaceutiques, l'équipement de laboratoire et l'équipement de traitement stérile.
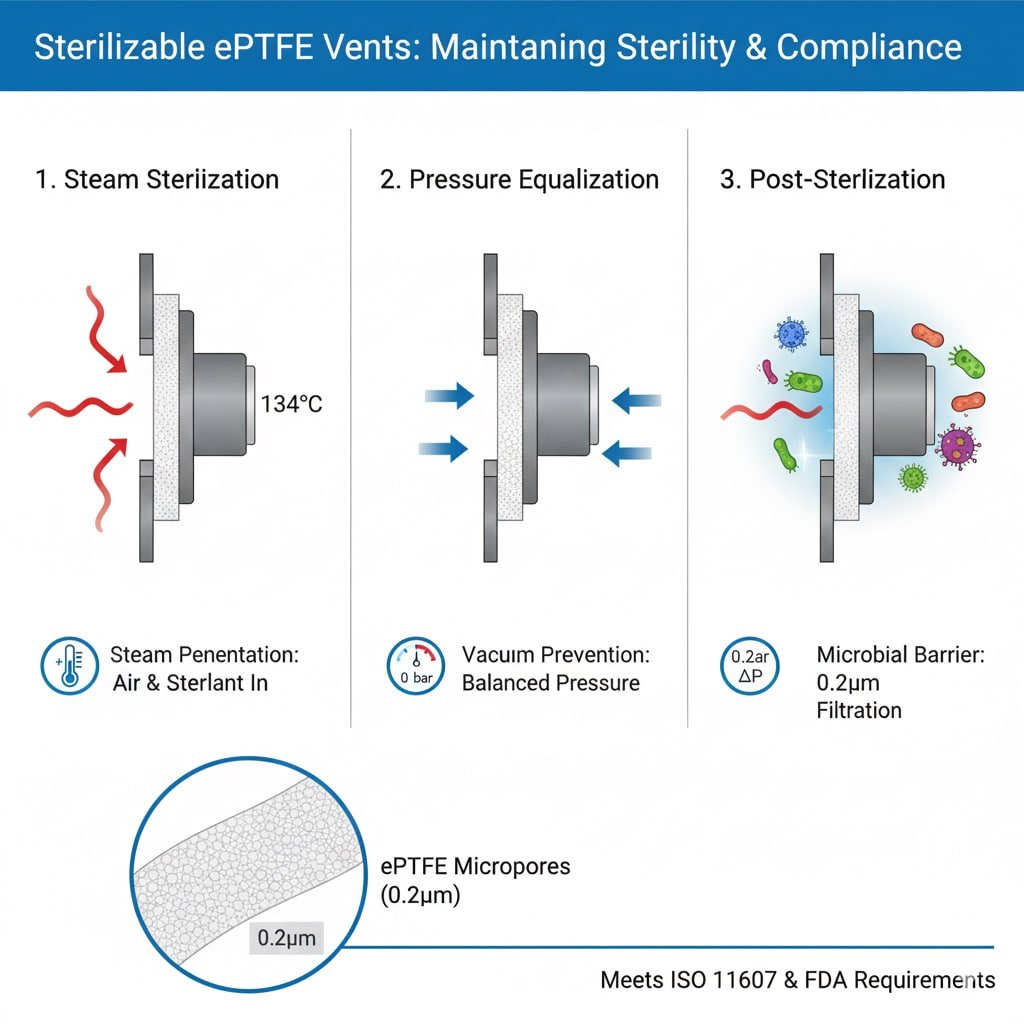
Exigences du processus de stérilisation
Pénétration de la vapeur : La stérilisation par autoclave exige que la vapeur pénètre l'emballage et entre en contact avec toutes les surfaces, ce qui nécessite des évents permettant la circulation du gaz tout en maintenant des barrières microbiennes.
Déplacement d'air : Une stérilisation efficace nécessite l'élimination complète de l'air et son remplacement par un stérilisant, ce que les évents facilitent grâce à un échange gazeux contrôlé.
Egalisation de la pression : Les cycles de stérilisation créent des différences de pression que les évents doivent prendre en compte sans compromettre les barrières stériles ou l'intégrité de l'emballage.
Paramètres de performance critiques
Résistance à la température : Les évents stérilisables doivent conserver leur intégrité structurelle et leurs performances de filtration à des températures de stérilisation allant de 121°C à 150°C.
Compatibilité chimique : Les matériaux doivent résister à la dégradation causée par les produits chimiques de stérilisation, notamment la vapeur, l'oxyde d'éthylène, le peroxyde d'hydrogène et l'ozone.
Efficacité de la barrière microbienne : Après la stérilisation, les évents doivent assurer une ventilation fiable. barrière microbienne3 avec des pores d'une taille typique de 0,2-0,22 microns pour la rétention des bactéries.
Considérations relatives à la conformité réglementaire
Exigences de validation de la FDA : Les applications de dispositifs médicaux nécessitent des processus de stérilisation validés avec une performance documentée des évents tout au long des cycles de stérilisation.
Conformité aux normes ISO : Les évents stérilisables doivent être conformes ISO 116074 et les exigences de la norme ISO 17665 relative à la stérilisation à la vapeur pour les applications médicales.
Tests de biocompatibilité : Les applications de contact avec des dispositifs médicaux peuvent nécessiter des tests de biocompatibilité USP Class VI pour garantir la sécurité des patients.
Catégories d'application
Emballage des dispositifs médicaux : Emballage stérile pour les implants, les instruments chirurgicaux et les dispositifs médicaux jetables nécessitant un maintien de la stérilité jusqu'à leur utilisation.
Fabrication de produits pharmaceutiques : Équipement de traitement stérile, bioréacteurs et conteneurs pharmaceutiques nécessitant des processus de stérilisation validés.
Équipement de laboratoire : Contenants de laboratoire autoclavables, récipients de culture et équipements d'analyse nécessitant des conditions stériles pour obtenir des résultats précis.
Comment les différentes méthodes de stérilisation affectent-elles les matériaux des bouchons d'évent ?
Les différentes méthodes de stérilisation créent des défis uniques pour les matériaux des bouchons d'évent, nécessitant des propriétés de matériaux spécifiques et des considérations de conception pour une performance optimale.
La stérilisation à la vapeur soumet les matériaux à des températures élevées (121-134°C) et à des conditions de vapeur saturée qui peuvent entraîner une dégradation thermique, des changements dimensionnels et des dommages aux membranes. La stérilisation à l'ETO expose les matériaux à des produits chimiques réactifs à des températures plus basses (37-63°C) mais à des durées d'exposition plus longues qui peuvent entraîner une dégradation chimique et des dégagements gazeux. Chaque méthode nécessite une sélection spécifique des matériaux pour une performance fiable.
Effets de la stérilisation à la vapeur
Stress thermique : Les températures élevées entraînent une dilatation thermique, une fonte potentielle des composants thermoplastiques et une dégradation des matériaux sensibles à la température.
Réactions d'hydrolyse5: L'exposition à la vapeur peut entraîner une dégradation hydrolytique de certains polymères, en particulier les polyesters et certains polyamides.
Stabilité dimensionnelle : Des cycles thermiques répétés peuvent entraîner des modifications dimensionnelles qui affectent les performances d'étanchéité et l'efficacité de la filtration.
Les défis de la stérilisation ETO
Réactivité chimique : L'oxyde d'éthylène réagit avec les matériaux contenant des atomes d'hydrogène actifs, ce qui peut altérer les propriétés des matériaux et créer des résidus toxiques.
Exigences en matière de dégagement gazeux : Les produits stérilisés à l'ETO nécessitent des périodes d'aération prolongées pour éliminer l'ETO absorbé et les produits de réaction avant de pouvoir être utilisés en toute sécurité.
Caractéristiques de pénétration : L'ETO nécessite des conditions d'humidité et de température spécifiques pour une pénétration efficace, ce qui influe sur les exigences de conception des évents.
Effets du plasma de peroxyde d'hydrogène
Dégradation oxydative : Le plasma H2O2 crée des espèces hautement réactives qui peuvent dégrader les matériaux organiques par des réactions d'oxydation.
Compatibilité des matériaux : De nombreux élastomères et certains plastiques sont incompatibles avec la stérilisation au plasma H2O2 en raison de leur dégradation rapide.
Avantages à basse température : La stérilisation au plasma fonctionne à basse température (45-55°C), ce qui réduit le stress thermique sur les matériaux sensibles à la température.
Considérations sur les rayonnements gamma
Dommages causés par les radiations : Le rayonnement gamma de haute énergie peut provoquer la scission ou la réticulation de la chaîne de polymères, ce qui modifie considérablement les propriétés des matériaux.
Accumulation de doses : La stérilisation gamma répétée peut provoquer des dommages cumulatifs, ce qui limite le nombre de cycles de stérilisation que les matériaux peuvent supporter.
Besoins en antioxydants : Les formulations résistantes aux radiations nécessitent souvent des antioxydants pour prévenir la dégradation oxydative pendant et après l'irradiation.
J'ai récemment aidé Ahmed Al-Rashid, directeur des opérations d'une usine pharmaceutique à Dubaï, à résoudre les problèmes de validation de la stérilisation à l'ETO de ses systèmes d'aération de bioréacteurs. Leurs bouchons d'aération standard absorbaient l'ETO et nécessitaient des périodes d'aération prolongées de 14 jours qui perturbaient les programmes de production. En mettant en œuvre nos bouchons d'aération en PTFE compatibles avec l'ETO et présentant des caractéristiques d'absorption minimales, ils ont réduit le temps d'aération à 24 heures tout en maintenant une assurance de stérilité totale - ce qui a considérablement amélioré l'efficacité de la production ! 🚀
Quels sont les meilleurs matériaux pour la stérilisation en autoclave ?
La sélection de matériaux appropriés pour la stérilisation en autoclave nécessite de comprendre la stabilité thermique, la résistance à l'hydrolyse et les performances à long terme en cas d'exposition répétée à la vapeur.
Le PTFE (polytétrafluoroéthylène) offre des performances supérieures en autoclave avec des températures de service continues jusqu'à 260°C, une excellente inertie chimique et une résistance à l'hydrolyse. Le PVDF (polyfluorure de vinylidène) offre une bonne stabilité thermique jusqu'à 150 °C à un coût inférieur. Évitez le nylon, le polyéthylène standard et la plupart des élastomères qui se dégradent dans les conditions de l'autoclave, compromettant ainsi les performances de filtration et d'étanchéité.
Avantages des membranes PTFE
Résistance exceptionnelle à la température : Le PTFE conserve son intégrité structurelle et ses performances de filtration à des températures bien supérieures aux conditions typiques de l'autoclave (121-134°C).
Inertie chimique : Le PTFE résiste à la dégradation causée par la vapeur, les produits chimiques de nettoyage et les sous-produits de stérilisation, ce qui garantit des performances constantes à long terme.
Propriétés hydrophobes : La nature hydrophobe du PTFE empêche l'absorption d'eau et maintient la stabilité dimensionnelle tout au long des cycles de stérilisation.
Comparaison des performances des matériaux
| Matériau | Température maximale (°C) | Résistance à la vapeur | Résistance à l'hydrolyse | Facteur de coût |
|---|---|---|---|---|
| PTFE | 260 | Excellent | Excellent | Haut |
| PVDF | 150 | Bon | Bon | Moyen |
| PP (Polypropylène) | 135 | Juste | Juste | Faible |
| Nylon | 80-100 | Pauvre | Pauvre | Faible |
Choix du matériau du boîtier
Acier inoxydable 316L : Offre une excellente résistance à la corrosion, une stabilité thermique et une facilité de nettoyage pour les applications pharmaceutiques et médicales nécessitant des procédures de nettoyage validées.
PEEK (polyétheréthercétone) : Offre une stabilité thermique exceptionnelle (utilisation continue jusqu'à 250°C) avec une excellente résistance chimique pour les applications exigeantes en autoclave.
Polypropylène : Option rentable pour les applications à usage unique avec des performances adéquates pour les cycles d'autoclave standard à 121°C.
Considérations sur les composants d'étanchéité
Joints toriques en EPDM : Offre une bonne résistance à la vapeur et une bonne stabilité thermique pour des températures allant jusqu'à 150°C avec d'excellentes performances d'étanchéité.
Joints en silicone : Ils offrent une résistance supérieure à la température (jusqu'à 200°C) mais peuvent présenter des problèmes de compatibilité avec certains produits chimiques de nettoyage.
Joints toriques encapsulés en PTFE : Combinez la résistance chimique du PTFE avec les propriétés d'étanchéité de l'élastomère pour les applications exigeantes nécessitant les deux caractéristiques de performance.
Optimisation de la conception pour l'utilisation de l'autoclave
Expansion thermique Accommodation : La conception des évents doit tenir compte de la dilatation thermique différentielle entre les matériaux afin d'éviter une défaillance du joint lors des cycles de température.
Caractéristiques de drainage : Une conception adéquate de l'évacuation empêche l'accumulation de condensat qui pourrait compromettre les performances de filtration ou créer des risques de contamination.
Soutien à la validation : Les caractéristiques de conception doivent faciliter les tests de validation, y compris la décomposition de la pression, le défi microbien et la vérification de la performance thermique.
Quels sont les matériaux qui conviennent le mieux aux processus de stérilisation ETO ?
La stérilisation ETO présente des défis uniques en matière de matériaux, nécessitant une compatibilité chimique, une absorption minimale et des caractéristiques de dégazage rapide pour un traitement efficace.
Le PTFE et le PVDF offrent une excellente compatibilité avec l'ETO, avec une absorption chimique minimale et un dégazage rapide. Évitez les matériaux contenant des sites d'hydrogène actifs comme le nylon, le PVC et le caoutchouc naturel qui réagissent avec l'ETO en formant des composés toxiques. Les boîtiers en acier inoxydable offrent une résistance chimique optimale, tandis que les joints en silicone offrent une bonne compatibilité avec l'ETO avec des caractéristiques de dégazage acceptables pour la plupart des applications.
Compatibilité chimique ETO
Mécanismes de réaction : L'ETO réagit avec les matériaux contenant des groupes hydroxyle, amino, carboxyle et sulfhydryle, formant des dérivés de l'éthylène glycol et d'autres composés potentiellement toxiques.
Caractéristiques d'absorption : Les matériaux à forte absorption d'ETO nécessitent des périodes d'aération prolongées, ce qui augmente considérablement le temps et les coûts de traitement.
Cinétique de dégazage : Les matériaux à dégazage rapide permettent des cycles d'aération plus courts, améliorant l'efficacité du processus et réduisant les temps de stockage.
Classement des performances matérielles de l'ETO
Excellente compatibilité avec l'ETO :
- PTFE : absorption minimale, dégazage rapide, pas de réactivité chimique
- PVDF : Faible absorption, bon dégazage, excellente résistance chimique
- Acier inoxydable : Pas d'absorption, possibilité d'utilisation immédiate
Bonne compatibilité avec l'ETO :
- Polypropylène : Absorption modérée, dégazage acceptable
- Silicone : Faible réactivité, exigences modérées en matière de dégazage
Mauvaise compatibilité avec l'ETO :
- Nylon : Réactivité élevée, aération prolongée nécessaire
- PVC : dégradation chimique, formation de composés toxiques
- Caoutchouc naturel : absorption élevée, dégradation potentielle
Temps d'aération requis
| Matériau | Durée d'aération typique | Niveau d'absorption ETO | Taux de dégazage |
|---|---|---|---|
| PTFE | 8-24 heures | Minime | Rapide |
| PVDF | 24-48 heures | Faible | Bon |
| Polypropylène | 48-72 heures | Modéré | Modéré |
| Nylon | 7-14 jours | Haut | Lenteur |
Optimisation des paramètres du processus
Contrôle de la température : La stérilisation ETO fonctionne généralement entre 37 et 63°C, ce qui nécessite des matériaux qui conservent leurs performances dans cette plage de température.
Exigences en matière d'humidité : L'efficacité de l'ETO requiert une humidité relative de 40-80%, ce qui nécessite des matériaux qui fonctionnent de manière cohérente dans ces conditions d'humidité.
Gestion de la concentration de gaz : Les concentrations d'ETO de 450-1200 mg/L nécessitent des matériaux qui résistent aux attaques chimiques tout en permettant la pénétration de l'agent stérilisant.
Considérations relatives à la validation
Essais sur les résidus : Les produits stérilisés à l'ETO doivent être testés pour détecter les résidus d'ETO et les produits de réaction afin de garantir le respect des limites de sécurité.
Entretien de la biocompatibilité : Les matériaux doivent conserver leur biocompatibilité après l'exposition à l'ETO et l'aération, ce qui nécessite une sélection validée des matériaux.
Surveillance des processus : La stérilisation ETO nécessite une surveillance continue de la température, de l'humidité, de la pression et de la concentration de gaz tout au long du cycle.
Comment sélectionner et valider les bouchons d'évent stérilisables ?
La sélection et la validation appropriées des bouchons d'évent stérilisables garantissent des performances de stérilisation fiables, la conformité aux réglementations et un succès opérationnel à long terme.
La sélection nécessite de faire correspondre les propriétés du matériau à la méthode de stérilisation, de définir les exigences de performance et de prendre en compte les normes réglementaires. La validation implique des tests de performance thermique, des études de résistance microbienne, une évaluation de la compatibilité chimique et une évaluation de la stabilité à long terme. Documenter tous les essais conformément aux normes de la FDA et de l'ISO pour la soumission réglementaire et la conformité du système de qualité.
Cadre des critères de sélection
Méthode de stérilisation Compatibilité : Adapter les matériaux des évents aux méthodes de stérilisation spécifiques (vapeur, ETO, plasma H2O2, gamma) en fonction des exigences de température, de résistance aux produits chimiques et aux radiations.
Spécifications de performance : Définir les débits, les pressions nominales, l'efficacité de filtration et les propriétés de barrière microbienne requis en fonction des exigences de l'application.
Exigences réglementaires : Tenez compte de la classification des dispositifs par la FDA, de la conformité aux normes ISO et des exigences de biocompatibilité pour les applications prévues.
Paramètres d'évaluation de l'application
Environnement d'exploitation : Évaluer les plages de température, l'exposition aux produits chimiques, les conditions de pression et les risques de contamination tout au long du cycle de vie du produit.
Fréquence de stérilisation : Tenir compte de l'utilisation unique par rapport aux cycles de stérilisation multiples et des effets cumulatifs sur les performances et la fiabilité des matériaux.
Portée de la validation : Déterminer les exigences en matière d'essais sur la base de l'évaluation des risques, de la voie réglementaire et des exigences du système de qualité.
Protocole de test de validation
Essai de performance thermique :
- Cycle de température dans les conditions de stérilisation
- Mesure de la stabilité dimensionnelle
- Vérification de l'efficacité de la filtration après exposition thermique
Test de provocation microbienne :
- Défi bactérien avec des organismes de test appropriés
- Vérification du maintien de la stérilité
- Évaluation de l'intégrité de la barrière à long terme
Évaluation de la compatibilité chimique :
- Évaluation de la dégradation des matériaux
- Essais sur les substances extractibles et lessivables
- Vérification du maintien de la biocompatibilité
Exigences en matière de documentation
Spécifications des matériaux : Fiches techniques complètes des matériaux, y compris la composition chimique, les propriétés thermiques et les certifications réglementaires.
Protocoles d'essai : Protocoles de validation détaillés conformes aux directives de la FDA et aux normes ISO pour la validation de la stérilisation.
Données sur les performances : Résultats d'essais complets démontrant la performance dans les conditions de fonctionnement et les cycles de stérilisation spécifiés.
Intégration du système de qualité
Qualification du fournisseur : Établir des accords de qualité avec les fournisseurs, notamment en ce qui concerne la traçabilité des matériaux, le contrôle des modifications et les exigences en matière de documentation sur la qualité.
Inspection entrante : Élaborer des procédures d'inspection pour la vérification des dimensions critiques, des propriétés des matériaux et des caractéristiques de performance.
Validation des processus : Intégrer la performance des évents dans la validation globale du processus de stérilisation, y compris les tests du scénario le plus défavorable.
Considérations relatives à la gestion des risques
Analyse des modes de défaillance : Identifier les modes de défaillance potentiels, y compris la dégradation des matériaux, la défaillance des joints et la compromission de la filtration, avec les stratégies d'atténuation appropriées.
Contrôle des changements : Établir des procédures pour gérer les changements de matériaux, les changements de fournisseurs et les modifications de spécifications avec les exigences de revalidation appropriées.
Contrôle continu : Mettre en œuvre des programmes de contrôle continu afin de vérifier la continuité des performances et d'identifier les problèmes potentiels avant qu'ils n'affectent la qualité du produit.
Conclusion
Les bouchons d'évent stérilisables jouent un rôle essentiel en assurant une stérilisation efficace tout en maintenant des barrières stériles dans les applications des dispositifs médicaux et pharmaceutiques. Il est essentiel de comprendre les défis uniques des différentes méthodes de stérilisation et de sélectionner les matériaux appropriés pour garantir des performances fiables et la conformité aux réglementations.
Les bouchons d'évent à base de PTFE offrent des performances supérieures dans le cadre de plusieurs méthodes de stérilisation, offrant une excellente résistance à la température, une compatibilité chimique et une fiabilité à long terme. Une sélection et une validation appropriées garantissent une efficacité optimale de la stérilisation tout en minimisant le temps et les coûts de traitement.
Chez Bepto, notre gamme complète de bouchons d'évent stérilisables comprend des membranes en PTFE de qualité pharmaceutique, des performances thermiques validées et une documentation complète pour les soumissions réglementaires. Avec plus d'une décennie d'expérience dans les applications d'évent spécialisées et des capacités de fabrication certifiées ISO, nous fournissons les solutions fiables et rentables dont vous avez besoin pour les applications de stérilisation critiques. Faites-nous confiance pour assurer la validation de vos processus de stérilisation et la sécurité de vos produits ! 🔬
FAQ sur les bouchons d'évent stérilisables
Q : Le même bouchon d'évent peut-il être utilisé pour la stérilisation en autoclave et en ETO ?
A : Oui, les bouchons d'évent à membrane PTFE peuvent être stérilisés efficacement à la fois en autoclave et à l'ETO. Le PTFE offre une excellente résistance à la température pour les cycles en autoclave et une absorption minimale de l'ETO pour une aération rapide, ce qui le rend idéal pour les installations utilisant plusieurs méthodes de stérilisation.
Q : Combien de cycles de stérilisation un bouchon d'évent peut-il supporter ?
A : Les bouchons d'évent en PTFE de haute qualité résistent généralement à plus de 100 cycles d'autoclave ou à plus de 50 cycles d'ETO tout en conservant leurs performances de filtration. La durée de vie réelle dépend des paramètres de stérilisation, des procédures de manipulation et des critères d'acceptation des performances pour votre application spécifique.
Q : Quelle est la taille des pores requise pour la filtration stérile dans les applications médicales ?
A : Les applications médicales nécessitent généralement des pores de 0,2 ou 0,22 micron pour une rétention bactérienne fiable. Cette taille de pore fournit une assurance de stérilité validée tout en permettant un flux de gaz adéquat pour une stérilisation efficace et une égalisation de la pression.
Q : Les bouchons d'évent stérilisables nécessitent-ils des tests de validation particuliers ?
A : Oui, les bouchons d'évent stérilisables doivent faire l'objet d'essais de validation, notamment en ce qui concerne les performances thermiques, le défi microbien et les études de compatibilité des matériaux. Les tests doivent être conformes aux directives de la FDA et aux normes ISO, et la documentation doit étayer la validation du processus de stérilisation et les demandes d'homologation.
Q : Comment éviter la contamination des bouchons d'évent pendant la stérilisation ?
A : Prévenir la contamination par une installation correcte, des couvertures de protection pendant la manipulation, des paramètres de stérilisation validés et un stockage post-stérilisation approprié. Utilisez une technique stérile lors de l'installation et assurez-vous que les bouchons d'évent sont conçus pour votre méthode de stérilisation spécifique et les exigences de l'application.
-
Apprenez les principes scientifiques de la stérilisation par autoclave et comment la vapeur saturée sous pression est utilisée pour tuer efficacement les micro-organismes. ↩
-
Explorer le processus chimique de stérilisation à l'oxyde d'éthylène (ETO), une méthode à basse température utilisée pour stériliser les dispositifs médicaux sensibles à la chaleur et à l'humidité. ↩
-
Découvrez les méthodes utilisées pour tester et valider l'efficacité d'une barrière microbienne, en s'assurant qu'elle empêche la pénétration de micro-organismes et maintient la stérilité. ↩
-
Passez en revue les principales exigences de la norme ISO 11607, qui spécifie les matériaux et les essais pour les systèmes de barrière stérile pour les dispositifs médicaux. ↩
-
Comprendre la réaction chimique de l'hydrolyse et comment elle peut entraîner la dégradation de certains matériaux polymères lorsqu'ils sont exposés à l'eau ou à la vapeur à des températures élevées. ↩



