Vääränlainen kaapeliläpivientien valinta lääketieteellisissä ja puhdastilaympäristöissä aiheuttaa kontaminaatioriskiä, säännösten noudattamatta jättämistä ja laitehäiriöitä, jotka johtavat potilasturvallisuuden vaarantumiseen, kalliisiin laitoksen sulkemisiin ja FDA:n rikkomuksiin, kun taas riittämätön tiivistys, sopimattomat materiaalit ja huono puhdistettavuus johtavat bakteerien kasvuun, hiukkasmaiseen kontaminaatioon ja steriiliysrikkomuksiin, jotka vaarantavat kriittiset terveydenhuollon toiminnot. Monet laitosjohtajat kamppailevat sellaisten läpivientien valitsemisen kanssa, jotka täyttävät tiukat lääketieteelliset standardit ja säilyttävät samalla luotettavan sähköisen suorituskyvyn.
Kaapeliläpivientien valitseminen lääkinnällisiin laitteisiin ja puhdastiloihin edellyttää FDA:n määräysten ymmärtämistä, USP-luokka VI1 materiaalivaatimukset, IP68+-tiivistysstandardit ja puhdastilaluokitustarpeet. Lääketieteellisen luokan ruostumaton teräs tai erikoistunut polymeerirakenne tarjoaa bioyhteensopivuuden, kemikaalien kestävyyden ja sileät pinnat tehokasta puhdistusta ja sterilointia varten säilyttäen samalla sähköisen eheyden kriittisissä terveydenhuollon sovelluksissa. Onnistuminen riippuu sääntelyn noudattamisen ja toiminnan luotettavuuden tasapainottamisesta.
Työskenneltyäni sairaalainsinöörien kanssa Bostonin suurimmissa lääketieteellisissä keskuksissa, lääkevalmistajien kanssa Sveitsissä ja puhdastilojen kanssa Singaporessa olen oppinut, että lääketieteelliset kaapeliläpiviennit ovat välttämättömiä steriilien ympäristöjen ylläpitämisessä ja potilasturvallisuuden varmistamisessa. Anna minun jakaa kriittistä tietoa optimaalisten läpivientien valitsemiseksi lääketieteellisiin ja puhdastiloihin tarkoitettuihin sovelluksiisi.
Sisällysluettelo
- Mikä erottaa lääketieteelliset kaapeliläpiviennit tavallisista läpivientiläpivienneistä?
- Miten täytät FDA:n ja lääkinnällisten laitteiden määräykset?
- Mitä materiaaleja tarvitaan puhdastiloissa?
- Miten varmistetaan asianmukainen puhdistus- ja sterilointiyhteensopivuus?
- Mitkä ovat tärkeimmät valintaperusteet eri lääketieteellisissä sovelluksissa?
- Lääketieteellisiä kaapeliläpivientejä koskevat usein kysytyt kysymykset
Mikä erottaa lääketieteelliset kaapeliläpiviennit tavallisista läpivientiläpivienneistä?
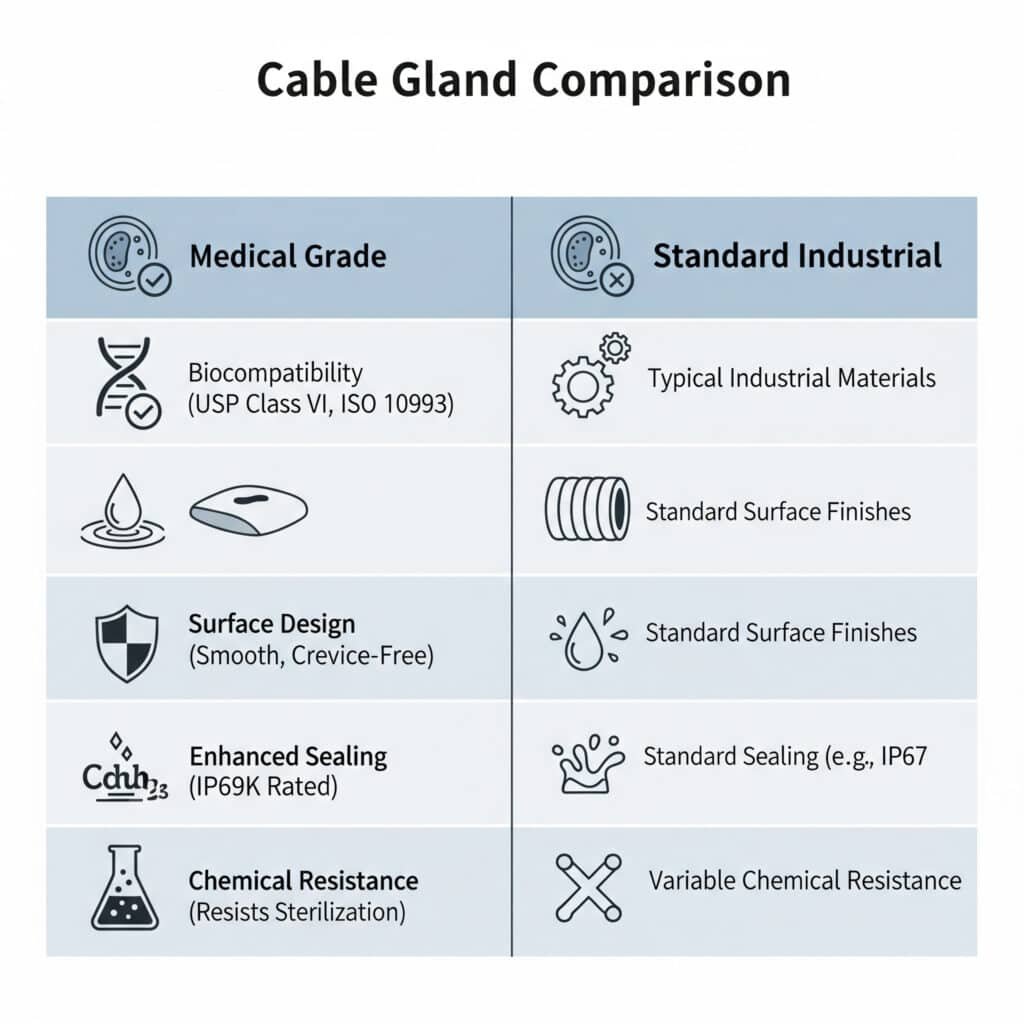
Lääketieteelliset kaapeliläpiviennit eroavat tavallisista läpivienneistä käyttämällä bioyhteensopivia materiaaleja, joissa on sileät puhdistettavat pinnat, jotka täyttävät FDA:n määräykset, jotka tarjoavat paremman tiivistyksen kontaminaation estämiseksi ja jotka kestävät kemiallisesti puhdistusaineita ja sterilointiprosesseja. Erikoisvalmisteiset mallit poistavat rakoja, joissa bakteerit voisivat asustaa, mutta säilyttävät samalla sähköisen suorituskyvyn kriittisissä terveydenhuoltoympäristöissä.
Näiden erojen ymmärtäminen on ratkaisevan tärkeää, koska lääketieteellisissä sovelluksissa on ainutlaatuisia turvallisuus- ja sääntelyvaatimuksia, joita tavanomaiset teollisuustulppaliitokset eivät pysty riittävästi täyttämään.
Biologista yhteensopivuutta koskevat vaatimukset
USP-luokan VI vaatimustenmukaisuus: Lääketieteellisissä kaapeliläpivienneissä on käytettävä materiaaleja, jotka läpäisevät Yhdysvaltojen farmakopean luokan VI biologisen testauksen biologisen yhteensopivuuden ja turvallisuuden varmistamiseksi lääkinnällisten laitteiden sovelluksissa.
ISO 10993 -standardit: Materiaalien on täytettävä ISO 109932 lääkinnällisten laitteiden biologiset arviointistandardit, joilla varmistetaan, ettei laitteella ole sytotoksisia, herkistäviä tai ärsyttäviä vaikutuksia ihmiskudokseen.
FDA 21 CFR 177 -hyväksyntä: Lääke- ja lääkintälaitesovelluksissa vaaditaan usein FDA:n määräysten mukaisia elintarvikekelpoisia materiaaleja, jotka ovat suorassa ja epäsuorassa elintarvikekontaktissa.
Bioyhteensopivat polymeerit: Erikoismateriaalit, kuten lääketieteellisen luokan PEEK, PTFE tai farmaseuttisen luokan nailon, tarjoavat bioyhteensopivuutta mekaanisista ominaisuuksista tinkimättä.
Puhdistettavuutta edistävä pinnan muotoilu
Sileä Pintakäsittely: Lääketieteellisissä rauhasissa on erittäin sileät pinnat, joiden Ra-arvot ovat yleensä alle 0,8 mikrometriä, mikä estää bakteerien tarttumisen ja mahdollistaa tehokkaan puhdistuksen.
Rakovapaa muotoilu: Poistetaan terävät kulmat, syvät kierteet ja monimutkaiset geometriat, jotka voivat sisältää bakteereja tai vastustaa puhdistus- ja sterilointiprosesseja.
Pyöristetyt reunat: Kaikissa ulkopinnoissa on pyöristetyt reunat ja sileät siirtymät, jotka helpottavat puhdistusta ja estävät puhdastilakäsineiden tai steriilien pakkausten vahingoittumisen.
Minimaalinen pinta-ala: Virtaviivainen rakenne minimoi saastumiselle altistuvan pinta-alan säilyttäen samalla tarvittavan mekaanisen ja sähköisen suorituskyvyn.
Parannettu tiivistysteho
IP68+ luokitukset: Ylivoimainen ympäristösuojaus, joka ylittää tavanomaisen IP68-luokan, ja saavuttaa usein IP69K-luokan korkean paineen ja korkean lämpötilan puhdistussovelluksissa.
Kontaminaatioesteet: Useat tiivistysvaiheet estävät hiukkasten, bakteerien ja puhdistuskemikaalien tunkeutumisen, mikä voisi vaarantaa steriilien ympäristöjen turvallisuuden.
Paineen kestävyys: Parannetut paineluokitukset kestävät aggressiivisia puhdistus- ja sterilointiprosesseja ilman tiivisteen rikkoutumista.
Pitkän aikavälin luotettavuus: Tiivistysmateriaalit säilyttävät eheytensä toistuvissa sterilointisykleissä ja altistumalla ankarille puhdistuskemikaaleille.
Kemiallinen kestävyys Ominaisuudet
Puhdistusaineiden yhteensopivuus: Kestää sairaalaluokan desinfiointiaineita, kvaternäärisiä ammoniumyhdisteitä, vetyperoksidia ja muita aggressiivisia puhdistuskemikaaleja.
Sterilointikestävyys: Materiaalit kestävät gammasäteilyä, etyleenioksidia, höyryautoklavointia ja muita sterilointimenetelmiä hajoamatta.
Farmaseuttiset kemikaalit: Kestää liuottimia, happoja, emäksiä ja lääkeaineseoksia, joita esiintyy yleisesti lääketieteellisissä valmistusympäristöissä.
Lämpötilavakaus: Säilytä ominaisuudet sterilointilämpötilajaksojen ja puhdastilojen lämpötilan säätövaatimusten avulla.
New Jerseyssä sijaitsevan suuren lääketehtaan laitosjohtaja David kohtasi toistuvia kontaminaatio-ongelmia steriileissä täyttölinjoissa, joissa tavalliset kaapeliläpiviennit sisälsivät bakteereja tiukoista puhdistusmenetelmistä huolimatta. Nykyisissä messinkiläpivienneissä oli monimutkaisia kierteitä ja pintakuvioita, joita ei voitu steriloida riittävästi, mikä johti erien hylkäämiseen ja FDA:n vaatimustenmukaisuuteen liittyviin ongelmiin. Määritimme lääketieteellisen luokan ruostumattomasta teräksestä valmistetut kaapeliläpiviennit, joissa oli sähkökiillotetut pinnat ja rakovapaat mallit, jotka täyttivät USP Class VI -vaatimukset. Päivitys poisti kontaminaatiolähteet, saavutti 99,9%:n puhdistustehokkuuden ja auttoi laitosta läpäisemään FDA:n tarkastukset samalla kun tuotteiden hylkäysprosentti väheni 85%:llä. 😊
Miten täytät FDA:n ja lääkinnällisten laitteiden määräykset?
FDA:n ja lääkinnällisten laitteiden säädösten noudattaminen edellyttää, että käytetään materiaaleja, joilla on asianmukaiset sertifikaatit, ylläpidetään yksityiskohtaista dokumentaatiota, noudatetaan Hyvät tuotantotavat (GMP)3, jäljitettävyyden varmistaminen ja 21 CFR:n osan 820 mukaisten laatujärjestelmien toteuttaminen; lääketieteelliset kaapeliläpiviennit edellyttävät FDA:n hyväksymiä materiaaleja, bioyhteensopivuustestejä ja valmistuksen valvontaa, joilla varmistetaan johdonmukainen laatu ja turvallisuus lääkinnällisten laitteiden sovelluksissa.
Lääketieteellisissä sovelluksissa säännösten noudattaminen on ehdoton edellytys, koska virheet voivat johtaa potilasvahinkoihin, tuotteiden takaisinvetoon ja vakaviin oikeudellisiin seurauksiin.
FDA:n materiaalivaatimukset
21 CFR osa 177: Lääkkeiden tai lääkinnällisten laitteiden kanssa kosketuksiin joutuvien materiaalien on täytettävä FDA:n elintarvikelisäaineita koskevat määräykset epäsuorassa elintarvikekontaktissa olevien aineiden osalta.
Master Access File (MAF): Toimittajien on ylläpidettävä FDA:n pääkäyttökansioita, joissa dokumentoidaan materiaaliturvallisuus, valmistusprosessit ja laadunvalvontamenettelyt.
Drug Master File (DMF): Lääkesovelluksia varten materiaalit saattavat vaatia Drug Master File -rekisteröintiä, jossa on yksityiskohtaiset koostumus- ja valmistustiedot.
Vaatimustenmukaisuustodistus: Toimittajien on toimitettava todistukset, jotka vahvistavat, että materiaalit täyttävät kaikki sovellettavat FDA:n määräykset ja vaatimukset.
Lääkinnällisten laitteiden laatustandardit
ISO 13485 -vaatimustenmukaisuus: Valmistuksen on noudatettava ISO 13485 -standardin mukaisia lääkinnällisten laitteiden laadunhallintajärjestelmiä suunnittelussa, tuotannossa ja markkinoille saattamisen jälkeisessä valvonnassa.
21 CFR osa 820 (QSR): Laatujärjestelmäasetuksen noudattaminen, jolla varmistetaan asianmukainen suunnittelun valvonta, asiakirjojen valvonta ja korjaavat/ennaltaehkäisevät toimet.
Riskienhallinta: ISO 14971 -standardin mukaiset lääkinnällisten laitteiden riskinhallintaprosessit, mukaan lukien riskianalyysi, arviointi ja valvontatoimenpiteet.
Suunnittelun valvonta: Muodolliset suunnittelunvalvontaprosessit, mukaan lukien suunnittelun suunnittelu, panos- ja lähtövaatimukset, tarkistukset, verifiointi ja validointi.

Dokumentointi ja jäljitettävyys
Materiaalitodistukset: Täydellinen materiaalin jäljitettävyys analyysitodistuksin, biokompatibiliteettitestien tuloksin ja säädösten noudattamista koskevin asiakirjoin.
Valmistusrekisterit: Yksityiskohtaiset valmistusasiakirjat, mukaan lukien prosessiparametrit, laadunvalvontatestit ja erien dokumentointi täydellistä jäljitettävyyttä varten.
Muutosten hallinta: Viralliset muutostenhallintamenettelyt, jotka koskevat kaikkia materiaalien, prosessien tai eritelmien muutoksia, jotka vaikuttavat määräystenmukaisuuteen.
Toimittajan pätevyys: Kattavat toimittajien pätevöintiohjelmat, joilla varmistetaan, että kaikki materiaalit ja komponentit täyttävät lääkinnällisten laitteiden vaatimukset.
Validointivaatimukset
Biologisen yhteensopivuuden testaus: USP-luokan VI testit, mukaan lukien systeemiset injektio-, intrakutaaniset ja implantointitestit biologisen turvallisuuden varmistamiseksi.
Puhdistuksen validointi: Dokumentoidut puhdistusmenetelmät, joiden validointitiedot osoittavat, että epäpuhtaudet on poistettu tehokkaasti ja että biokuorta on vähennetty.
Steriloinnin validointi: Sterilointiprosessien validointi, mukaan lukien annoskartoitus, steriiliyden varmistustasot ja materiaalien yhteensopivuustutkimukset.
Suorituskyvyn testaus: Sähköiset, mekaaniset ja ympäristötestaukset, joilla varmistetaan, että suorituskyky täyttää lääkinnällisten laitteiden vaatimukset koko tuotteen elinkaaren ajan.
Lainsäädännön toimittamisen tuki
510(k)-asiakirjat: Tekninen dokumentaatio, joka tukee FDA:n 510(k)-hakemuksia kaapeliläpivientiä sisältäville lääkinnällisille laitteille.
Tekniset tiedostot: Kattavat tekniset asiakirjat CE-merkintää varten lääkinnällisiä laitteita koskevan asetuksen (MDR) mukaisesti Euroopan markkinoilla.
Laatusopimukset: Toimittajien kanssa tehtävät viralliset laatusopimukset, joissa määritellään vastuualueet, eritelmät ja vaatimustenmukaisuusvaatimukset.
Tarkastustuki: Tuki FDA:n, ilmoitettujen laitosten ja asiakkaiden auditoinneille, mukaan lukien asiakirjojen tarkastaminen ja laitostarkastukset.
Mitä materiaaleja tarvitaan puhdastiloissa?
Puhdastilasovellukset edellyttävät materiaaleja, joilla on alhaiset kaasuuntumisominaisuudet, hiukkasten muodostumisen kestävyys, kemiallinen yhteensopivuus puhdistusaineiden kanssa, sileät ei-huokoiset pinnat ja sopiva johtavuus. Lääketieteellisen luokan ruostumaton teräs 316L, PEEK, PTFE ja erikoistuneet puhdastilahyväksytyt polymeerit tarjoavat optimaalisen suorituskyvyn ja täyttävät samalla seuraavat vaatimukset ISO 146444 puhdastilavaatimukset ja sähköisen eheyden säilyttäminen valvotuissa ympäristöissä.
Materiaalin valinta on ratkaisevan tärkeää, koska puhdastilat edellyttävät tiukkaa hiukkas- ja molekyylikontaminaation valvontaa, sillä se voi vaarantaa tuotteen laadun tai steriilit olosuhteet.
Ruostumatonta terästä koskevat vaatimukset
316L Medical Grade: Austeniittinen ruostumaton teräs, jossa on alhainen hiilipitoisuus ja joka tarjoaa erinomaisen korroosionkestävyyden ja bioyhteensopivuuden lääketieteellisiin sovelluksiin.
Sähkökiillotettu viimeistely: Sähkökiillotus poistaa pinnan epätarkkuudet, vähentää hiukkasten muodostumista ja luo sileät pinnat tehokasta puhdistusta varten.
Passivointikäsittely: Kemiallinen passivointi parantaa korroosionkestävyyttä ja poistaa raudan epäpuhtaudet, jotka voivat aiheuttaa värimuutoksia tai hiukkasten muodostumista.
Pinnan karheus: Alle 0,8 mikrometrin (32 mikrotuuman) Ra-arvot minimoivat bakteerien tarttumisen ja helpottavat puhdistus- ja sterilointiprosesseja.
Korkean suorituskyvyn polymeerit
PEEK (polyeetterieteriketoni): Erinomainen kemiallinen kestävyys, vähäinen kaasunmuodostus ja bioyhteensopivuus tekevät PEEK:stä ihanteellisen lääke- ja lääkinnällisten laitteiden sovelluksiin.
PTFE (polytetrafluorieteeni): Erinomainen kemiallinen inerttiys ja tarttumattomuus takaavat erinomaisen kestävyyden puhdistuskemikaaleja ja biologisia materiaaleja vastaan.
Lääketieteellisen luokan nailonit: Erityisesti muotoillut nailonit, joilla on USP Class VI -hyväksyntä, tarjoavat hyvät mekaaniset ominaisuudet ja bioyhteensopivuuden lääketieteellisiin sovelluksiin.
Puhdastilahyväksytty POM: Polyoksimetyleeni, jossa on alhainen hiukkasten muodostuminen ja hyvä mittatarkkuus tarkkuuspuhdastilakäyttöön.
Puhdastilaluokitus Yhteensopivuus
ISO-luokka 5 (luokka 100): Erittäin sileät pinnat, joissa hiukkasten muodostuminen on minimaalista puolijohteiden ja lääkkeiden valmistussovelluksissa.
ISO-luokka 6 (luokka 1000): Kohtalainen hiukkasten hallinta lääkinnällisten laitteiden valmistuksessa ja joissakin lääkeprosesseissa.
ISO-luokka 7 (luokka 10000): Puhdastilojen standardivaatimukset yleisiä farmaseuttisia ja lääkinnällisten laitteiden kokoonpanotoimintoja varten.
ISO-luokka 8 (luokka 100000): Pakkausten ja joidenkin lääkinnällisten laitteiden valmistusprosessien puhdastilavaatimukset.
Uloskaasujen ja saastumisen valvonta
Vähän kaasuja muodostavat materiaalit: Materiaalit, joiden haihtuvien orgaanisten yhdisteiden (VOC) päästöt ovat mahdollisimman vähäiset ja jotka voivat saastuttaa herkkiä prosesseja tai tuotteita.
Molekulaarinen saastuminen: Molekyylien epäpuhtauksien, kuten silikonien, pehmittimien ja muiden tuotteen laatuun mahdollisesti vaikuttavien orgaanisten yhdisteiden valvonta.
Ioninen saastuminen: Materiaalit, joiden ionipitoisuus on alhainen, elektronisten komponenttien ja farmaseuttisten tuotteiden saastumisen estämiseksi.
Uuttuvat aineet: Minimaalinen määrä uuttuvia aineita, jotka voivat käytön aikana huuhtoutua farmaseuttisiin tuotteisiin tai puhdistusliuoksiin.
Kemiallinen yhteensopivuusmatriisi
| Puhdistusaine | 316L SS | PEEK | PTFE | Lääketieteellinen Nylon |
|---|---|---|---|---|
| Isopropyylialkoholi | Erinomainen | Erinomainen | Erinomainen | Hyvä |
| Vetyperoksidi | Erinomainen | Erinomainen | Erinomainen | Fair |
| Kvaternaarinen ammonium | Erinomainen | Erinomainen | Erinomainen | Hyvä |
| Natriumhypokloriitti | Hyvä | Erinomainen | Erinomainen | Huono |
| Peretikkahappo | Hyvä | Erinomainen | Erinomainen | Huono |
Hassan, joka johtaa toimintoja Sveitsissä sijaitsevassa huippuluokan lääketehtaassa, tarvitsi kaapeliläpivientien päivittämistä ISO-luokan 5 puhdastilassa, jossa valmistetaan steriilejä ruiskeena käytettäviä lääkkeitä. Nykyiset läpiviennit tuottivat hiukkasia puhdistusjaksojen aikana, eivätkä ne kestäneet aggressiivisia sterilointiprotokollia, joita heidän uudet biologiset tuotteensa edellyttivät. Toimitimme sähkökiillotetut 316L-ruostumattomasta teräksestä valmistetut kaapeliläpiviennit, joiden hiukkastuotanto on validoidusti vähäistä ja jotka ovat täysin kemiallisesti yhteensopivia heidän puhdistus- ja sterilointiprosessiensa kanssa. Päivityksellä saavutettiin 90%-hiukkasmäärät alle ISO-luokan 5 raja-arvojen, poistettiin puhdistukseen liittyvät kontaminaatiotapahtumat ja tuettiin heidän uuden steriilin valmistuslinjansa onnistunutta validointia.
Miten varmistetaan asianmukainen puhdistus- ja sterilointiyhteensopivuus?
Asianmukaisen puhdistus- ja sterilointiyhteensopivuuden varmistaminen edellyttää sellaisten materiaalien valitsemista, jotka kestävät toistuvan altistumisen puhdistuskemikaaleille ja sterilointimenetelmille, pintojen suunnittelua täydellistä puhdistettavuutta varten, puhdistusmenetelmien validointia ja yksityiskohtaisen dokumentoinnin ylläpitoa. Lääketieteelliset kaapeliläpiviennit edellyttävät sileitä, rakoja sisältämättömiä pintoja, kemikaalinkestäviä materiaaleja ja validoituja puhdistusprotokollia, joilla saavutetaan vaaditut steriiliyden varmistustasot.
Puhdistuksen ja steriloinnin yhteensopivuus on olennaisen tärkeää, koska riittämätön dekontaminaatio voi johtaa tuotteiden kontaminaatioon, potilasturvallisuusriskeihin ja säännösten rikkomiseen.
Sterilointimenetelmän yhteensopivuus
Höyryautoklavointi: Materiaalien on kestettävä 121°C-134°C höyryautoklavointi5 sykliä ilman hajoamista, mittamuutoksia tai tiivisteen rikkoutumista.
Gammasäteily: Kestää 25-50 kGy:n gammasäteilyannoksia, joita käytetään yleisesti lääkinnällisten laitteiden steriloinnissa ilman materiaalin hajoamista.
Etyleenioksidi (EtO): Kemiallinen yhteensopivuus EtO-steriloinnin kanssa, mukaan lukien sterilointiaineen kestävyys ja asianmukaiset kaasunpoisto-ominaisuudet.
Vetyperoksidiplasma: Yhteensopivuus matalan lämpötilan plasmasterilointijärjestelmien kanssa, mukaan lukien materiaalin stabiilius ja täydellinen sterilointiaineen tunkeutuminen.
Puhdistuksen validointivaatimukset
Puhdistusmenetelmät: Dokumentoidut puhdistusmenettelyt, joissa määritellään tehokkaan puhdistamisen edellyttämät kemikaalit, pitoisuudet, kontaktiajat ja mekaaniset toimet.
Validointiprotokollat: Viralliset validointitutkimukset, joissa osoitetaan puhdistuksen tehokkuus käyttäen pahimman mahdollisen saastumisen skenaarioita ja analyyttisiä testejä.
Hyväksymiskriteerit: Määritellyt puhtauden hyväksymiskriteerit, mukaan lukien silmämääräinen tarkastus, hiukkasmäärät, biokuormitustasot ja kemiallisten jäämien raja-arvot.
Rutiiniseuranta: Jatkuvat seurantaohjelmat, joilla varmistetaan puhdistuksen jatkuva tehokkuus ja tunnistetaan mahdolliset suorituskyvyn heikkenemiset.
Pinnan suunnitteluun liittyvät näkökohdat
Viemäröintiominaisuudet: Suunnitteluominaisuudet, jotka edistävät puhdistusliuosten täydellistä valumista ja estävät epäpuhtauksia sisältävien lammikoiden muodostumisen.
Saavutettavuus: Kaikki pinnat on voitava puhdistaa lääketieteellisissä laitoksissa käytettävillä tavanomaisilla puhdistusvälineillä ja -menetelmillä.
Purkamisvaatimukset: Harkitse, onko tiivisteitä purettava puhdistusta varten vai riittääkö ehjä puhdistus.
Tiivisteen vaihto: Menettelyt tiivisteiden vaihtoa ja validointia varten, kun tiivisteiden osat on vaihdettava säännöllisesti puhdistuskemikaalialtistumisen vuoksi.
Dokumentointi ja vaatimustenmukaisuus
Puhdistusohjeet: Yksityiskohtaiset puhdistusohjeet, mukaan lukien vaiheittaiset menettelyt, kemikaaleja koskevat tiedot ja turvallisuusohjeet.
Käyttöturvallisuustiedot: Täydelliset materiaaliturvallisuustiedot, mukaan lukien kemiallinen yhteensopivuus, lämpötilarajat ja sterilointiyhteensopivuus.
Validointiraportit: Puhdistuksen validointiraportit, joissa osoitetaan tehokkuus ja vahvistetaan rutiininomaisen seurannan vaatimukset.
Koulutusmateriaalit: Koulutusmateriaali laitoksen henkilökunnalle lääkinnällisten kaapeliläpivientien asianmukaisesta puhdistuksesta, käsittelystä ja huoltomenetelmistä.
Laadunvalvonnan testaus
Biokuorman testaus: Säännöllinen testaus mikrobikontaminaation varmentamiseksi puhdistuksen tehokkuuden varmistamiseksi ja mahdollisten ongelma-alueiden tunnistamiseksi.
Endotoksiinin testaus: Testataan bakteerien endotoksiinit, jotka voivat aiheuttaa pyrogeenisia reaktioita lääke- ja lääkinnällisten laitteiden sovelluksissa.
Hiukkasten laskenta: Hiukkasmäärän testaus sen varmistamiseksi, että puhdastilavaatimukset täyttyvät puhdistus- ja huoltotoimien jälkeen.
Kemiallisten jäämien analysointi: Testataan, onko tuotteisiin jäänyt puhdistuskemikaalijäämiä, jotka voivat saastuttaa tuotteita tai vaikuttaa bioyhteensopivuuteen.
Mitkä ovat tärkeimmät valintaperusteet eri lääketieteellisissä sovelluksissa?
Keskeiset valintaperusteet vaihtelevat sovelluksittain, mutta niihin kuuluvat sääntelyn vaatimustenmukaisuusvaatimukset, biokompatibiliteettitasot, puhdastilaluokitukset, sterilointimenetelmät, kemiallinen altistuminen ja sähköisen suorituskyvyn tarpeet. Kirurgiset laitteet edellyttävät korkeinta biokompatibiliteettia, lääketeollisuus kemikaalien kestävyyttä ja diagnostiikkalaitteet keskittyvät sähköiseen eheyteen, kun taas kaikki sovellukset edellyttävät asianmukaisia sääntelyn mukaisia sertifiointeja ja yhteensopivuutta puhdistuksen kanssa.
Erilaisilla lääketieteellisillä sovelluksilla on ainutlaatuisia vaatimuksia, jotka on otettava huolellisesti huomioon kaapeliläpivientiä valittaessa, jotta voidaan varmistaa optimaalinen suorituskyky ja määräystenmukaisuus.
Kirurgiset ja potilaskontaktilaitteet
Suoraa kontaktia koskevat vaatimukset: USP-luokan VI bioyhteensopivuus, johon liittyy ylimääräinen sytotoksisuustesti materiaaleille, jotka ovat suorassa kosketuksessa potilaaseen kirurgisten toimenpiteiden aikana.
Sterilointitiheys: Kyky kestää toistuvia sterilointisyklejä ilman hajoamista, mikä edellyttää tyypillisesti satoja sterilointisyklejä kestäviä materiaaleja.
Sähköturvallisuus: Parannetut sähköturvallisuusvaatimukset, mukaan lukien alhainen vuotovirta ja luotettava eristys potilaskäyttöön kytketyille laitteille.
Luotettavuus hätätilanteessa: Kriittiset luotettavuusvaatimukset elämää ylläpitäville ja ensiapulaitteille, joiden vikaantuminen voi vaikuttaa suoraan potilasturvallisuuteen.
Lääketeollisuus
GMP:n noudattaminen: Hyvän tuotantotavan vaatimukset, mukaan lukien materiaalien jäljitettävyys, muutosten hallinta ja validointiasiakirjat.
Tuotteen kosketusturvallisuus: Materiaalit, jotka eivät saastuta lääkevalmisteita huuhtoutumisen, hiukkasten muodostumisen tai kemiallisen vuorovaikutuksen kautta.
Puhdistuksen validointi: Laajat puhdistuksen validointivaatimukset, joihin liittyy dokumentoituja menettelyjä ja hyväksymiskriteerejä lääkkeiden valmistusta varten.
Eräasiakirjat: Täydellinen erien dokumentointi ja jäljitettävyys lääkkeiden valmistuslaitteissa käytettävien materiaalien osalta.
Diagnostiikka- ja laboratoriolaitteet
Tarkkuusvaatimukset: Mittapysyvyys ja tarkkuus analyysilaitteissa, jotka vaativat johdonmukaista mekaanista ja sähköistä suorituskykyä.
Kemiallinen kestävyys: Kestää laboratoriokemikaaleja, reagensseja ja puhdistusliuottimia, joita käytetään yleisesti diagnostisissa sovelluksissa.
EMC Performance: Sähkömagneettista yhteensopivuutta koskevat vaatimukset herkille analyysi- ja diagnostiikkalaitteille.
Kalibrointivakaus: Mekaaninen vakaus, joka ei vaikuta laitteen kalibrointiin tai mittaustarkkuuteen ajan myötä.
Lääkinnällisten laitteiden valmistus
Prosessin validointi: Materiaalit ja komponentit, jotka tukevat lääkinnällisten laitteiden valmistuksen prosessien validointivaatimuksia.
Laatujärjestelmät: Integrointi ISO 13485 -laatujärjestelmiin, mukaan lukien toimittajien kelpuuttaminen ja saapuvien tuotteiden tarkastusmenettelyt.
Riskienhallinta: Materiaalit, jotka tukevat lääkinnällisten laitteiden riskinhallintavaatimuksia, mukaan lukien vikatilojen analyysi ja lieventämisstrategiat.
Sääntelytuki: Toimittajan tuki viranomaishakemuksille, mukaan lukien tekninen dokumentaatio ja viranomaisasiantuntemus.
Valintapäätösmatriisi
| Sovellustyyppi | Ensisijaiset kriteerit | Toissijaiset kriteerit | Kriittiset standardit |
|---|---|---|---|
| Kirurgiset laitteet | Biologinen yhteensopivuus | Sterilointi | USP luokka VI, ISO 10993 |
| Farmaseuttinen | Kemiallinen kestävyys | GMP-vaatimustenmukaisuus | FDA 21 CFR, cGMP |
| Diagnostiikka | Tarkkuus | EMC Suorituskyky | IEC 61326, ISO 15189 |
| Valmistus | Prosessin validointi | Laatujärjestelmät | ISO 13485, 21 CFR 820 |
Kustannus-hyötyanalyysi
Alkuperäiset kustannukset vs. elinkaari: Huomioi kokonaisomistuskustannukset, mukaan lukien huolto-, vaihto- ja vaatimustenmukaisuuskustannukset laitteiden käyttöiän aikana.
Sääntelyriski: Tasapainota olennaiset kustannukset ja säännösten noudattamiseen liittyvät riskit sekä säännösten noudattamatta jättämisestä mahdollisesti aiheutuvat kustannukset.
Suorituskykyvaatimukset: Varmistetaan, että valitut materiaalit täyttävät suorituskykyä koskevat vähimmäisvaatimukset ilman, että niitä eritellään liikaa, mikä lisää kustannuksia tarpeettomasti.
Toimittajan valmiudet: Arvioi toimittajien valmiudet jatkuvaan tukeen, dokumentointiin ja sääntelyn noudattamiseen liittyvään apuun.
Päätelmä
Kaapeliläpivientien valitseminen lääkinnällisiin laitteisiin ja puhdastiloihin edellyttää, että ymmärretään ainutlaatuiset sääntely-, materiaali- ja suorituskykyvaatimukset, jotka erottavat nämä sovellukset tavanomaisista teollisista käyttötarkoituksista. Onnistuminen riippuu bioyhteensopivuuden, puhdistettavuuden, säännöstenmukaisuuden ja sähköisen suorituskyvyn tasapainottamisesta.
Luotettavan lääketieteellisen kaapelitiivisteen suorituskyvyn avain on yhteistyö sellaisten toimittajien kanssa, jotka ymmärtävät lääketieteellisiä laitteita koskevat määräykset ja pystyvät tarjoamaan asianmukaiset materiaalit, dokumentoinnin ja jatkuvan tuen koko tuotteen elinkaaren ajan. Bepto on erikoistunut lääketieteellisiin kaapelitiivisteisiin, jotka täyttävät FDA:n vaatimukset ja kansainväliset lääkinnällisten laitteiden standardit, ja tarjoaa laadunvarmistuksen ja sääntelytuen, joita tarvitaan kriittisissä terveydenhuollon sovelluksissa.
Lääketieteellisiä kaapeliläpivientejä koskevat usein kysytyt kysymykset
K: Mitä sertifiointeja tarvitsen lääketieteellisiin kaapeliläpivientiin?
A: Lääketieteelliset kaapeliläpiviennit edellyttävät yleensä USP Class VI -biologisen yhteensopivuuden sertifiointia, FDA 21 CFR -vaatimustenmukaisuutta materiaalien osalta ja ISO 13485 -valmistuksen laatujärjestelmiä. Erityisvaatimukset riippuvat sovelluksestasi ja sääntelyviranomaisesta.
K: Voiko tavallisia ruostumattomasta teräksestä valmistettuja kaapeliläpivientejä käyttää lääketieteellisissä sovelluksissa?
A: Tavallinen ruostumaton teräs ei välttämättä täytä lääketieteellisiä vaatimuksia. Lääketieteellisissä sovelluksissa tarvitaan 316L-ruostumatonta terästä, jossa on sähkökiillotettu viimeistely, bioyhteensopivuustestaus ja asianmukainen dokumentaatio säännösten noudattamista varten.
K: Miten puhdistan ja steriloin lääketieteelliset kaapeliläpiviennit?
A: Noudata valmistajan validoituja puhdistusmenetelmiä käyttäen hyväksyttyjä puhdistusaineita ja sterilointimenetelmiä. Useimmat lääkinnälliset rauhaset tukevat höyryautoklavointia, gammasäteilyä tai kemiallista sterilointia asianmukaisen materiaalin yhteensopivuuden vallitessa.
K: Mitä eroa on puhdastilan ja lääketieteellisen luokan kaapeliläpivientien välillä?
A: Lääketieteellinen luokka sisältää bioyhteensopivuusvaatimukset ja FDA:n vaatimustenmukaisuuden, kun taas puhdastilaluokka keskittyy hiukkasten hallintaan ja kemikaalien kestävyyteen. Joissakin sovelluksissa vaaditaan sekä lääketieteellisiä että puhdastilaluokkia.
K: Kuinka usein lääkinnälliset kaapeliläpiviennit on vaihdettava?
A: Vaihtoväli riippuu sterilointisykleistä, kemiallisesta altistumisesta ja valmistajan suosituksista. Tarkasta tyypillisesti 100-200 sterilointisyklin välein ja vaihda kunnonarvioinnin ja validointivaatimusten perusteella.
-
Tutustu USP-luokan VI sertifiointiin vaadittaviin erityisiin biologisen reaktiivisuuden testeihin. ↩
-
Tutustu yleiskatsaukseen lääkinnällisten laitteiden biologista arviointia koskevasta ISO 10993 -standardisarjasta. ↩
-
Tutustu FDA:n virallisiin ohjeisiin ja määräyksiin nykyisistä hyvistä tuotantotavoista (cGMP). ↩
-
Tutustu yksityiskohtaiseen oppaaseen ISO 14644 -standardeista, jotka koskevat ilman puhtauden luokittelua puhdastiloissa. ↩
-
Ymmärtää höyrysteriloinnin periaatteet, mukaan lukien ajan, lämpötilan ja paineen merkitys. ↩



