Die unsachgemäße Auswahl von Kabelverschraubungen in medizinischen und Reinraumumgebungen führt zu Kontaminationsrisiken, zur Nichteinhaltung gesetzlicher Vorschriften und zu Gerätefehlfunktionen, die die Sicherheit der Patienten gefährden, zu kostspieligen Betriebsstilllegungen und zu Verstößen gegen die FDA führen, während eine unzureichende Abdichtung, ungeeignete Materialien und schlechte Reinigbarkeit zu Bakterienwachstum, Partikelkontamination und Sterilitätsverletzungen führen, die kritische Abläufe im Gesundheitswesen gefährden. Viele Einrichtungsleiter haben Schwierigkeiten, Stopfbuchsen auszuwählen, die den strengen medizinischen Normen entsprechen und gleichzeitig eine zuverlässige elektrische Leistung gewährleisten.
Die Auswahl von Kabelverschraubungen für medizinische Geräte und Reinräume erfordert die Kenntnis der FDA-Vorschriften, USP Klasse VI1 Die Konstruktion aus medizinischem Edelstahl oder speziellem Polymer bietet Biokompatibilität, chemische Beständigkeit und glatte Oberflächen für eine effektive Reinigung und Sterilisation bei gleichzeitiger Aufrechterhaltung der elektrischen Integrität in kritischen Gesundheitsanwendungen. Der Erfolg hängt vom Gleichgewicht zwischen der Einhaltung der Vorschriften und der Betriebssicherheit ab.
Durch meine Zusammenarbeit mit Krankenhausingenieuren in großen medizinischen Zentren in Boston, mit Pharmaherstellern in der Schweiz und mit Reinraumeinrichtungen in Singapur habe ich gelernt, dass Kabelverschraubungen in medizinischer Qualität für die Aufrechterhaltung steriler Umgebungen und die Gewährleistung der Patientensicherheit unerlässlich sind. Lassen Sie mich Ihnen das entscheidende Wissen für die Auswahl optimaler Verschraubungen für Ihre medizinischen und Reinraumanwendungen vermitteln.
Inhaltsübersicht
- Wodurch unterscheiden sich medizinische Kabelverschraubungen von Standardverschraubungen?
- Wie erfüllen Sie die FDA- und Medizinproduktevorschriften?
- Welche Materialien sind für Reinraumanwendungen erforderlich?
- Wie können Sie die Kompatibilität von Reinigung und Sterilisation sicherstellen?
- Was sind die wichtigsten Auswahlkriterien für verschiedene medizinische Anwendungen?
- FAQs über medizinische Kabelverschraubungen
Wodurch unterscheiden sich medizinische Kabelverschraubungen von Standardverschraubungen?
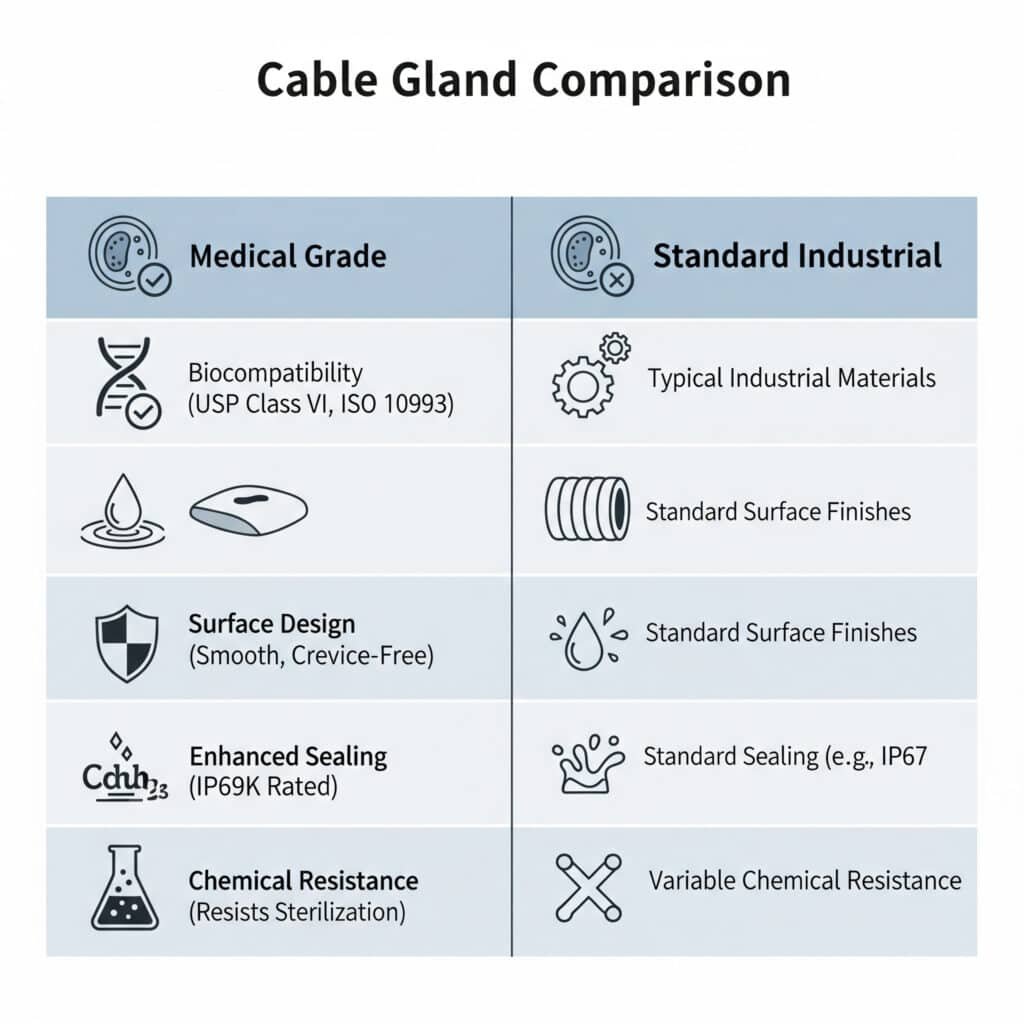
Medizinische Kabelverschraubungen unterscheiden sich von Standardverschraubungen durch die Verwendung biokompatibler Materialien, glatte, reinigbare Oberflächen, die Erfüllung der FDA-Vorschriften, eine verbesserte Abdichtung zur Verhinderung von Kontaminationen und chemische Beständigkeit gegen Reinigungsmittel und Sterilisationsverfahren sowie ein spezielles Design, das Spalten eliminiert, in denen sich Bakterien ansiedeln könnten, während die elektrische Leistung in kritischen Umgebungen im Gesundheitswesen erhalten bleibt.
Das Verständnis dieser Unterschiede ist von entscheidender Bedeutung, da medizinische Anwendungen besondere Sicherheits- und Regulierungsanforderungen stellen, die von Standard-Industrieverschraubungen nicht angemessen erfüllt werden können.
Anforderungen an die Biokompatibilität
Einhaltung der USP Klasse VI: Für medizinische Kabelverschraubungen müssen Materialien verwendet werden, die die biologischen Tests der Klasse VI der United States Pharmacopeia für Biokompatibilität und Sicherheit bei der Anwendung von Medizinprodukten bestehen.
ISO 10993 Normen: Die Materialien müssen folgende Anforderungen erfüllen ISO 109932 biologische Bewertungsstandards für Medizinprodukte, die sicherstellen, dass sie keine zytotoxischen, sensibilisierenden oder reizenden Auswirkungen auf menschliches Gewebe haben.
FDA 21 CFR 177-Zulassung: Für pharmazeutische und medizintechnische Anwendungen werden häufig lebensmitteltaugliche Materialien benötigt, die den FDA-Vorschriften für den direkten und indirekten Kontakt mit Lebensmitteln entsprechen.
Biokompatible Polymere: Spezielle Materialien wie medizinisches PEEK, PTFE oder pharmazeutische Nylons bieten Biokompatibilität ohne Beeinträchtigung der mechanischen Eigenschaften.
Oberflächendesign für Reinigungsfähigkeit
Glatte Oberfläche: Medizinische Drüsen verfügen über ultraglatte Oberflächen mit Ra-Werten von typischerweise unter 0,8 Mikrometern, um die Anhaftung von Bakterien zu verhindern und eine effektive Reinigung zu ermöglichen.
Spaltfreies Design: Beseitigung von scharfen Ecken, tiefen Gewinden und komplexen Geometrien, die Bakterien beherbergen oder Reinigungs- und Sterilisationsprozessen widerstehen könnten.
Abgerundete Kanten: Alle Außenflächen weisen abgerundete Kanten und glatte Übergänge auf, um die Reinigung zu erleichtern und Beschädigungen von Reinraumhandschuhen oder Sterilverpackungen zu vermeiden.
Minimaler Oberflächenbereich: Stromlinienförmige Designs minimieren die Oberfläche, die Verunreinigungen ausgesetzt ist, und erhalten gleichzeitig die erforderliche mechanische und elektrische Leistung.
Verbesserte Dichtungsleistung
IP68+ Bewertungen: Hervorragender Umweltschutz, der über den Standard IP68 hinausgeht und oft IP69K für Hochdruck- und Hochtemperatur-Reinigungsanwendungen erreicht.
Barrieren gegen Kontamination: Mehrere Dichtungsstufen verhindern das Eindringen von Partikeln, Bakterien und Reinigungschemikalien, die sterile Umgebungen beeinträchtigen könnten.
Druckbeständigkeit: Verbesserte Druckwerte, um aggressiven Reinigungsverfahren und Sterilisationsprozessen ohne Dichtungsversagen standzuhalten.
Langfristige Verlässlichkeit: Die Dichtungsmaterialien bleiben auch nach wiederholten Sterilisationszyklen und der Einwirkung von aggressiven Reinigungschemikalien intakt.
Chemische Beständigkeit Eigenschaften
Kompatibilität der Reinigungsmittel: Beständigkeit gegen Desinfektionsmittel in Krankenhausqualität, quaternäre Ammoniumverbindungen, Wasserstoffperoxid und andere aggressive Reinigungschemikalien.
Widerstandsfähigkeit gegen Sterilisation: Die Materialien widerstehen Gammastrahlung, Ethylenoxid, Dampfautoklavierung und anderen Sterilisationsmethoden ohne Beeinträchtigung.
Pharmazeutische Chemikalien: Beständigkeit gegen Lösungsmittel, Säuren, Basen und pharmazeutische Verbindungen, die in der medizinischen Fertigung häufig vorkommen.
Temperaturstabilität: Aufrechterhaltung der Eigenschaften durch Sterilisations-Temperaturzyklen und Anforderungen an die Reinraum-Temperaturregelung.
David, Betriebsleiter einer großen pharmazeutischen Produktionsanlage in New Jersey, hatte immer wieder mit Kontaminationsproblemen in den sterilen Abfüllanlagen zu kämpfen, wo die Standard-Kabelverschraubungen trotz strenger Reinigungsprotokolle Bakterien beherbergten. Die vorhandenen Messingverschraubungen wiesen komplexe Gewindemuster und Oberflächenbeschaffenheiten auf, die nicht ausreichend sterilisiert werden konnten, was zur Zurückweisung von Chargen und zu Problemen mit der FDA-Konformität führte. Wir spezifizierten Kabelverschraubungen aus medizinischem Edelstahl mit elektropolierten Oberflächen und spaltfreiem Design, die den Anforderungen der USP-Klasse VI entsprechen. Durch die Aufrüstung wurden Kontaminationsquellen beseitigt, eine Reinigungswirkung von 99,9% erreicht und die Anlage konnte die FDA-Inspektionen bestehen, während die Produktrückweisungsrate um 85% gesenkt wurde.
Wie erfüllen Sie die FDA- und Medizinproduktevorschriften?
Die Einhaltung der FDA-Bestimmungen und der Vorschriften für medizinische Geräte erfordert die Verwendung von Materialien mit den entsprechenden Zertifizierungen, eine detaillierte Dokumentation und die Einhaltung der Gute Herstellungspraktiken (GMP)3Für medizinische Kabelverschraubungen sind von der FDA zugelassene Materialien, Biokompatibilitätstests und Herstellungskontrollen erforderlich, die eine gleichbleibende Qualität und Sicherheit bei der Anwendung medizinischer Geräte gewährleisten.
Die Einhaltung gesetzlicher Vorschriften ist bei medizinischen Anwendungen nicht verhandelbar, da Fehler zu Patientenschäden, Produktrückrufen und schwerwiegenden rechtlichen Konsequenzen führen können.
FDA-Materialanforderungen
21 CFR Teil 177: Materialien, die mit Arzneimitteln oder Medizinprodukten in Berührung kommen, müssen die FDA-Bestimmungen für Lebensmittelzusatzstoffe für Stoffe mit indirektem Lebensmittelkontakt erfüllen.
Master Access File (MAF): Die Lieferanten müssen FDA Master Access Files führen, in denen Materialsicherheit, Herstellungsprozesse und Qualitätskontrollverfahren dokumentiert sind.
Drug Master File (DMF): Für pharmazeutische Anwendungen müssen die Materialien möglicherweise in einer Arzneimittelstammdatei (Drug Master File) mit detaillierten Angaben zur Zusammensetzung und Herstellung registriert werden.
Konformitätsbescheinigung: Die Lieferanten müssen Zertifikate vorlegen, die bestätigen, dass die Materialien alle geltenden FDA-Vorschriften und -Spezifikationen erfüllen.
Qualitätsstandards für Medizinprodukte
Einhaltung der ISO 13485: Die Herstellung muss nach dem Qualitätsmanagementsystem ISO 13485 für Medizinprodukte in den Bereichen Entwicklung, Produktion und Überwachung nach dem Inverkehrbringen erfolgen.
21 CFR Teil 820 (QSR): Einhaltung der Vorschriften des Qualitätssicherungssystems zur Gewährleistung ordnungsgemäßer Konstruktionskontrollen, Dokumentenkontrolle und Korrektur-/Vorbeugungsmaßnahmen.
Risikomanagement: ISO 14971 Risikomanagementverfahren für Medizinprodukte, einschließlich Risikoanalyse, -bewertung und -kontrollmaßnahmen.
Design-Kontrollen: Formale Entwurfskontrollprozesse, einschließlich Entwurfsplanung, Input/Output-Anforderungen, Überprüfungen, Verifizierung und Validierung.

Dokumentation und Rückverfolgbarkeit
Material-Zertifikate: Vollständige Materialrückverfolgbarkeit mit Analysezertifikaten, Biokompatibilitätstestergebnissen und Dokumentation der Einhaltung gesetzlicher Vorschriften.
Herstellungsaufzeichnungen: Detaillierte Herstellungsaufzeichnungen, einschließlich Prozessparameter, Qualitätskontrolltests und Chargendokumentation für eine vollständige Rückverfolgbarkeit.
Kontrolle ändern: Formelle Änderungskontrollverfahren für alle Änderungen an Materialien, Prozessen oder Spezifikationen, die sich auf die Einhaltung von Vorschriften auswirken.
Lieferantenqualifizierung: Umfassende Qualifizierungsprogramme für Zulieferer, die sicherstellen, dass alle Materialien und Komponenten die Anforderungen an Medizinprodukte erfüllen.
Anforderungen an die Validierung
Biokompatibilitätstests: USP-Klasse-VI-Tests, einschließlich systemischer Injektions-, Intrakutan- und Implantationstests zur Überprüfung der biologischen Sicherheit.
Validierung der Reinigung: Dokumentierte Reinigungsverfahren mit Validierungsdaten, die die effektive Entfernung von Verunreinigungen und die Reduzierung der biologischen Belastung belegen.
Validierung der Sterilisation: Validierung von Sterilisationsprozessen, einschließlich Dosiszuordnung, Sterilitätssicherungsniveaus und Materialkompatibilitätsstudien.
Leistungstests: Elektrische, mechanische und umwelttechnische Tests, um zu überprüfen, ob die Leistung während des gesamten Produktlebenszyklus den Anforderungen an medizinische Geräte entspricht.
Unterstützung bei Zulassungsanträgen
510(k)-Dokumentation: Technische Dokumentation zur Unterstützung von FDA 510(k) Anträgen für medizinische Geräte mit Kabelverschraubungen.
Technische Dateien: Umfassende technische Unterlagen für die CE-Kennzeichnung gemäß der Medizinprodukteverordnung (MDR) auf den europäischen Märkten.
Qualitätsvereinbarungen: Formelle Qualitätsvereinbarungen mit Lieferanten, in denen Verantwortlichkeiten, Spezifikationen und Konformitätsanforderungen festgelegt sind.
Audit-Unterstützung: Unterstützung bei Audits der FDA, der benannten Stelle und von Kunden, einschließlich Überprüfung der Dokumentation und Inspektionen der Einrichtungen.
Welche Materialien sind für Reinraumanwendungen erforderlich?
Reinraumanwendungen erfordern Materialien mit geringen Ausgasungseigenschaften, Beständigkeit gegen Partikelbildung, chemischer Kompatibilität mit Reinigungsmitteln, glatten, nicht porösen Oberflächen und angemessenen Leitfähigkeitsniveaus. Medizinischer Edelstahl 316L, PEEK, PTFE und spezielle, für Reinräume zugelassene Polymere bieten optimale Leistung und erfüllen gleichzeitig die Anforderungen von ISO 146444 Reinraumstandards und Aufrechterhaltung der elektrischen Integrität in kontrollierten Umgebungen.
Die Auswahl des Materials ist von entscheidender Bedeutung, da in Reinräumen eine strenge Kontrolle der Partikel- und Molekülkontamination erforderlich ist, die die Produktqualität oder die sterilen Bedingungen beeinträchtigen könnte.
Anforderungen an nichtrostenden Stahl
316L Medizinische Qualität: Austenitischer rostfreier Stahl mit niedrigem Kohlenstoffgehalt, der eine hervorragende Korrosionsbeständigkeit und Biokompatibilität für medizinische Anwendungen bietet.
Elektropolierte Oberfläche: Durch das Elektropolieren werden Oberflächenmängel beseitigt, die Partikelbildung reduziert und glatte Oberflächen für eine effektive Reinigung geschaffen.
Passivierungsbehandlung: Die chemische Passivierung verbessert die Korrosionsbeständigkeit und entfernt Eisenverunreinigungen, die zu Verfärbungen oder Partikelbildung führen können.
Oberflächenrauhigkeit: Ra-Werte unter 0,8 Mikrometern (32 Mikrozoll) minimieren das Anhaften von Bakterien und erleichtern Reinigungs- und Sterilisationsprozesse.
Hochleistungs-Polymere
PEEK (Polyetheretherketon): Aufgrund seiner hervorragenden chemischen Beständigkeit, geringen Ausgasung und Biokompatibilität ist PEEK ideal für pharmazeutische und medizintechnische Anwendungen.
PTFE (Polytetrafluorethylen): Hervorragende chemische Inertheit und Antihafteigenschaften sorgen für ausgezeichnete Beständigkeit gegen Reinigungschemikalien und biologische Materialien.
Nylons in medizinischer Qualität: Speziell formulierte Nylons mit USP Class VI-Zulassung bieten gute mechanische Eigenschaften mit Biokompatibilität für medizinische Anwendungen.
Reinraumzugelassenes POM: Polyoxymethylen mit geringer Partikelbildung und guter Formbeständigkeit für Präzisionsreinraumanwendungen.
Kompatibilität der Reinraumklassifizierung
ISO-Klasse 5 (Klasse 100): Ultraglatte Oberflächen mit minimaler Partikelbildung für Anwendungen in der Halbleiter- und Arzneimittelherstellung.
ISO-Klasse 6 (Klasse 1000): Mäßige Partikelkontrolle für die Herstellung medizinischer Geräte und einige pharmazeutische Prozesse.
ISO-Klasse 7 (Klasse 10000): Standard-Reinraumanforderungen für allgemeine pharmazeutische und medizintechnische Montagearbeiten.
ISO-Klasse 8 (Klasse 100000): Grundlegende Reinraumanforderungen für Verpackungen und einige Herstellungsverfahren für medizinische Geräte.
Ausgasung und Kontaminationskontrolle
Gering ausgasende Materialien: Materialien mit minimalen Emissionen flüchtiger organischer Verbindungen (VOC), die empfindliche Prozesse oder Produkte kontaminieren könnten.
Molekulare Kontamination: Kontrolle von molekularen Verunreinigungen, einschließlich Silikonen, Weichmachern und anderen organischen Verbindungen, die die Produktqualität beeinträchtigen könnten.
Ionische Kontamination: Materialien mit niedrigem Ionengehalt, um eine Kontamination von elektronischen Bauteilen und pharmazeutischen Produkten zu verhindern.
Extrahierbare Stoffe: Minimale extrahierbare Stoffe, die bei der Verwendung in pharmazeutische Produkte oder Reinigungslösungen übergehen könnten.
Matrix der chemischen Verträglichkeit
| Reinigungsmittel | EDELSTAHL 316L | PEEK | PTFE | Medizinisches Nylon |
|---|---|---|---|---|
| Isopropylalkohol | Ausgezeichnet | Ausgezeichnet | Ausgezeichnet | Gut |
| Wasserstoffsuperoxyd | Ausgezeichnet | Ausgezeichnet | Ausgezeichnet | Messe |
| Quaternäres Ammonium | Ausgezeichnet | Ausgezeichnet | Ausgezeichnet | Gut |
| Natriumhypochlorit | Gut | Ausgezeichnet | Ausgezeichnet | Schlecht |
| Peressigsäure | Gut | Ausgezeichnet | Ausgezeichnet | Schlecht |
Hassan, der den Betrieb einer hochmodernen pharmazeutischen Anlage in der Schweiz leitet, musste die Kabelverschraubungen in ihrem Reinraum der ISO-Klasse 5 für die Herstellung steriler Injektionsmittel aufrüsten. Die vorhandenen Verschraubungen erzeugten während der Reinigungszyklen Partikel und hielten den aggressiven Sterilisationsprotokollen, die für ihre neuen biologischen Produkte erforderlich sind, nicht stand. Wir lieferten elektropolierte Kabelverschraubungen aus 316L-Edelstahl mit nachweislich geringer Partikelbildung und vollständiger chemischer Kompatibilität mit den Reinigungs- und Sterilisationsverfahren des Unternehmens. Durch die Aufrüstung wurde eine Partikelanzahl von 90% unter den Grenzwerten der ISO-Klasse 5 erreicht, reinigungsbedingte Kontaminationsereignisse wurden vermieden und die erfolgreiche Validierung der neuen sterilen Fertigungslinie unterstützt.
Wie können Sie die Kompatibilität von Reinigung und Sterilisation sicherstellen?
Um die Kompatibilität mit Reinigungs- und Sterilisationsverfahren zu gewährleisten, müssen Materialien ausgewählt werden, die einer wiederholten Einwirkung von Reinigungschemikalien und Sterilisationsverfahren standhalten, die Oberflächen müssen so gestaltet sein, dass sie vollständig gereinigt werden können, die Reinigungsverfahren müssen validiert werden und es muss eine ausführliche Dokumentation geführt werden. Medizinische Kabelverschraubungen erfordern glatte, spaltfreie Oberflächen, chemikalienbeständige Materialien und validierte Reinigungsprotokolle, die das erforderliche Sterilitätsniveau gewährleisten.
Die Kompatibilität von Reinigung und Sterilisation ist von entscheidender Bedeutung, da eine unzureichende Dekontamination zu Produktkontaminationen, Risiken für die Patientensicherheit und Verstößen gegen gesetzliche Vorschriften führen kann.
Kompatibilität der Sterilisationsmethode
Dampf-Autoklavieren: Die Materialien müssen 121°C-134°C standhalten. Dampf-Autoklavieren5 Zyklen, ohne dass es zu Beeinträchtigungen, Maßveränderungen oder Dichtungsversagen kommt.
Gammastrahlung: Beständigkeit gegenüber Gammastrahlungsdosen von 25-50 kGy, die üblicherweise für die Sterilisation von Medizinprodukten verwendet werden, ohne dass das Material beschädigt wird.
Ethylenoxid (EtO): Chemische Kompatibilität mit der EtO-Sterilisation, einschließlich Beständigkeit gegen das Sterilisationsmittel und geeignete Entgasungseigenschaften.
Wasserstoffperoxid-Plasma: Kompatibilität mit Niedertemperatur-Plasma-Sterilisationssystemen, einschließlich Materialstabilität und vollständiger Durchdringung des Sterilisiermittels.
Anforderungen an die Reinigungsvalidierung
Reinigungsverfahren: Dokumentierte Reinigungsverfahren mit Angabe der Chemikalien, Konzentrationen, Einwirkzeiten und mechanischen Maßnahmen, die für eine wirksame Dekontamination erforderlich sind.
Validierungsprotokolle: Formale Validierungsstudien, die die Wirksamkeit der Reinigung anhand von Worst-Case-Kontaminationsszenarien und analytischen Tests nachweisen.
Kriterien für die Akzeptanz: Definierte Akzeptanzkriterien für die Sauberkeit, einschließlich visueller Inspektion, Partikelzählung, Bioburden-Grenzwerte und Grenzwerte für chemische Rückstände.
Routinemäßige Überwachung: Laufende Überwachungsprogramme zur Überprüfung der kontinuierlichen Wirksamkeit der Reinigung und zur Feststellung von Leistungseinbußen.
Überlegungen zur Oberflächengestaltung
Entwässerungsmerkmale: Konstruktionsmerkmale, die ein vollständiges Abfließen der Reinigungslösungen fördern und Ansammlungen verhindern, in denen sich Verunreinigungen ansammeln könnten.
Zugänglichkeit: Alle Oberflächen müssen für die Reinigung mit den in medizinischen Einrichtungen üblichen Reinigungsgeräten und -verfahren zugänglich sein.
Anforderungen an die Demontage: Überlegen Sie, ob die Stopfbuchsen zur Reinigung demontiert werden müssen oder ob eine intakte Reinigung für die Anwendung ausreicht.
Austausch der Dichtung: Verfahren für den Austausch von Dichtungen und die Validierung, wenn Dichtungskomponenten aufgrund der Einwirkung von Reinigungschemikalien regelmäßig ausgetauscht werden müssen.
Dokumentation und Einhaltung der Vorschriften
Anweisungen zur Reinigung: Detaillierte Reinigungsanweisungen mit Schritt-für-Schritt-Verfahren, chemischen Spezifikationen und Sicherheitsvorkehrungen.
Daten zur Materialsicherheit: Vollständige Informationen zur Materialsicherheit, einschließlich chemischer Verträglichkeit, Temperaturgrenzen und Sterilisationsverträglichkeit.
Validierungsberichte: Reinigungsvalidierungsberichte zum Nachweis der Wirksamkeit und zur Festlegung von Routineüberwachungsanforderungen.
Schulungsunterlagen: Schulungsmaterial für das Personal von Einrichtungen zur ordnungsgemäßen Reinigung, Handhabung und Wartung von medizinischen Kabelverschraubungen.
Prüfung der Qualitätskontrolle
Bioburden-Tests: Regelmäßige Tests auf mikrobielle Verunreinigung, um die Wirksamkeit der Reinigung zu überprüfen und potenzielle Problembereiche zu identifizieren.
Endotoxin-Tests: Prüfung auf bakterielle Endotoxine, die bei pharmazeutischen und medizintechnischen Anwendungen pyrogene Reaktionen hervorrufen können.
Partikelzählung: Partikelzählungstests zur Überprüfung, ob die Reinraumanforderungen nach Reinigungs- und Wartungsarbeiten eingehalten werden.
Analyse chemischer Rückstände: Prüfung auf Rückstände von Reinigungschemikalien, die Produkte kontaminieren oder die Biokompatibilität beeinträchtigen könnten.
Was sind die wichtigsten Auswahlkriterien für verschiedene medizinische Anwendungen?
Die wichtigsten Auswahlkriterien variieren je nach Anwendung, umfassen jedoch Anforderungen an die Einhaltung gesetzlicher Vorschriften, Biokompatibilitätsstufen, Reinraumklassifizierungen, Sterilisationsmethoden, chemische Belastung und elektrische Leistungsanforderungen, wobei für chirurgische Geräte höchste Biokompatibilität, für die pharmazeutische Herstellung chemische Beständigkeit und für diagnostische Geräte elektrische Integrität erforderlich sind, während für alle Anwendungen entsprechende gesetzliche Zertifizierungen und Reinigungsverträglichkeit erforderlich sind.
Verschiedene medizinische Anwendungen haben einzigartige Anforderungen, die bei der Auswahl der Kabelverschraubungen sorgfältig berücksichtigt werden müssen, um eine optimale Leistung und die Einhaltung der gesetzlichen Vorschriften zu gewährleisten.
Chirurgische Geräte und Geräte mit Patientenkontakt
Anforderungen für direkten Kontakt: Biokompatibilität der USP-Klasse VI mit zusätzlichen Zytotoxizitätstests für Materialien, die bei chirurgischen Eingriffen in direktem Patientenkontakt stehen.
Häufigkeit der Sterilisation: Die Fähigkeit, häufigen Sterilisationszyklen ohne Beeinträchtigung standzuhalten, erfordert in der Regel Materialien, die über Hunderte von Sterilisationszyklen hinweg stabil sind.
Elektrische Sicherheit: Erhöhte Anforderungen an die elektrische Sicherheit, einschließlich geringer Ableitströme und zuverlässiger Isolierung für Geräte, die an Patienten angeschlossen sind.
Verlässlichkeit im Notfall: Kritische Zuverlässigkeitsanforderungen für lebenserhaltende und notfallmedizinische Geräte, deren Ausfall die Sicherheit der Patienten direkt beeinträchtigen könnte.
Pharmazeutische Herstellung
GMP-Einhaltung: Anforderungen an die gute Herstellungspraxis, einschließlich Materialrückverfolgbarkeit, Änderungskontrolle und Validierungsdokumentation.
Sicherheit bei Produktkontakt: Materialien, die pharmazeutische Produkte nicht durch Auslaugung, Partikelbildung oder chemische Wechselwirkung verunreinigen.
Validierung der Reinigung: Umfassende Anforderungen an die Reinigungsvalidierung mit dokumentierten Verfahren und Akzeptanzkriterien für die pharmazeutische Herstellung.
Batch-Dokumentation: Vollständige Chargendokumentation und Rückverfolgbarkeit für Materialien, die in pharmazeutischen Produktionsanlagen verwendet werden.
Diagnostik- und Laborgeräte
Anforderungen an die Präzision: Maßhaltigkeit und Präzision für analytische Instrumente, die eine gleichbleibende mechanische und elektrische Leistung erfordern.
Chemische Beständigkeit: Beständigkeit gegen Laborchemikalien, Reagenzien und Reinigungsmittel, die üblicherweise bei diagnostischen Anwendungen verwendet werden.
EMC-Leistung: Anforderungen an die elektromagnetische Verträglichkeit von empfindlichen Analyse- und Diagnosegeräten.
Stabilität der Kalibrierung: Mechanische Stabilität, die die Kalibrierung des Instruments oder die Messgenauigkeit im Laufe der Zeit nicht beeinträchtigt.
Herstellung medizinischer Geräte
Prozess-Validierung: Materialien und Komponenten, die die Anforderungen an die Prozessvalidierung bei der Herstellung von Medizinprodukten unterstützen.
Qualitätssysteme: Integration in ISO 13485-Qualitätssysteme, einschließlich Lieferantenqualifizierung und Eingangskontrollverfahren.
Risikomanagement: Materialien zur Unterstützung der Anforderungen an das Risikomanagement von Medizinprodukten, einschließlich Fehlermöglichkeitsanalysen und Strategien zur Risikominderung.
Regulatorische Unterstützung: Unterstützung der Zulieferer bei der Einreichung von Zulassungsanträgen, einschließlich technischer Dokumentation und Fachwissen über Rechtsvorschriften.
Matrix für Auswahlentscheidungen
| Art der Anwendung | Primäre Kriterien | Sekundäre Kriterien | Kritische Standards |
|---|---|---|---|
| Chirurgische Ausrüstung | Biokompatibilität | Sterilisation | USP Klasse VI, ISO 10993 |
| Pharmazeutische | Chemische Beständigkeit | GMP-Einhaltung | FDA 21 CFR, cGMP |
| Diagnostik | Präzision | EMC-Leistung | IEC 61326, ISO 15189 |
| Herstellung | Prozess-Validierung | Qualitätssysteme | ISO 13485, 21 CFR 820 |
Kosten-Nutzen-Analyse
Anschaffungskosten vs. Lebenszyklus: Berücksichtigen Sie die Gesamtbetriebskosten einschließlich der Kosten für Wartung, Austausch und Einhaltung der Vorschriften über die gesamte Lebensdauer der Geräte.
Regulatorisches Risiko: Abwägen der materiellen Kosten gegen die Risiken der Einhaltung von Vorschriften und die potenziellen Kosten einer Nichteinhaltung.
Leistungsanforderungen: Stellen Sie sicher, dass die ausgewählten Materialien die Mindestanforderungen an die Leistung erfüllen, ohne dass eine Überspezifikation die Kosten unnötig in die Höhe treibt.
Fähigkeiten der Lieferanten: Bewertung der Fähigkeiten von Zulieferern im Hinblick auf laufenden Support, Dokumentation und Unterstützung bei der Einhaltung von Vorschriften.
Schlussfolgerung
Die Auswahl von Kabelverschraubungen für medizinische Geräte und Reinräume erfordert ein Verständnis der besonderen gesetzlichen Vorschriften, Material- und Leistungsanforderungen, die diese Anwendungen von Standardanwendungen in der Industrie unterscheiden. Der Erfolg hängt vom Gleichgewicht zwischen Biokompatibilität, Reinigbarkeit, Einhaltung von Vorschriften und elektrischer Leistung ab.
Der Schlüssel zu einer zuverlässigen Leistung medizinischer Kabelverschraubungen liegt in der Zusammenarbeit mit Lieferanten, die sich mit den Vorschriften für Medizinprodukte auskennen und geeignete Materialien, Dokumentation und kontinuierliche Unterstützung während des gesamten Produktlebenszyklus anbieten können. Wir bei Bepto haben uns auf medizinische Kabelverschraubungen spezialisiert, die den Anforderungen der FDA und den internationalen Normen für Medizinprodukte entsprechen, und bieten die Qualitätssicherung und regulatorische Unterstützung, die für kritische Anwendungen im Gesundheitswesen erforderlich sind.
FAQs über medizinische Kabelverschraubungen
F: Welche Zertifizierungen benötige ich für medizinische Kabelverschraubungen?
A: Medizinische Kabelverschraubungen erfordern in der Regel eine Biokompatibilitätszertifizierung nach USP Klasse VI, die Einhaltung von FDA 21 CFR für die Materialien und Qualitätssysteme nach ISO 13485 für die Herstellung. Die spezifischen Anforderungen hängen von Ihrer Anwendung und der zuständigen Behörde ab.
F: Können normale Kabelverschraubungen aus Edelstahl in medizinischen Anwendungen verwendet werden?
A: Normaler rostfreier Stahl erfüllt möglicherweise nicht die medizinischen Anforderungen. Medizinische Anwendungen erfordern Edelstahl 316L in medizinischer Qualität mit elektropolierter Oberfläche, Biokompatibilitätstests und ordnungsgemäßer Dokumentation für die Einhaltung von Vorschriften.
F: Wie reinige und sterilisiere ich medizinische Kabelverschraubungen?
A: Befolgen Sie die validierten Reinigungsverfahren des Herstellers mit zugelassenen Reinigungsmitteln und Sterilisationsmethoden. Die meisten medizinischen Drüsen können mit Dampfautoklavierung, Gammastrahlung oder chemischer Sterilisation bei entsprechender Materialverträglichkeit behandelt werden.
F: Was ist der Unterschied zwischen Kabelverschraubungen für Reinräume und für medizinische Zwecke?
A: Die medizinische Qualität umfasst Biokompatibilitätsanforderungen und FDA-Konformität, während die Reinraumqualität auf Partikelkontrolle und Chemikalienbeständigkeit ausgerichtet ist. Einige Anwendungen erfordern sowohl medizinische als auch Reinraum-Spezifikationen.
F: Wie oft sollten medizinische Kabelverschraubungen ausgetauscht werden?
A: Die Häufigkeit des Austauschs hängt von den Sterilisationszyklen, der chemischen Belastung und den Empfehlungen des Herstellers ab. In der Regel wird nach 100-200 Sterilisationszyklen eine Inspektion durchgeführt und je nach Zustandsbewertung und Validierungsanforderungen ersetzt.
-
Erfahren Sie mehr über die spezifischen biologischen Reaktivitätstests, die für die Zertifizierung nach USP Klasse VI erforderlich sind. ↩
-
Verschaffen Sie sich einen Überblick über die Normenreihe ISO 10993 für die biologische Bewertung von Medizinprodukten. ↩
-
Lesen Sie die offiziellen FDA-Richtlinien und -Vorschriften für die aktuelle gute Herstellungspraxis (cGMP). ↩
-
Entdecken Sie einen detaillierten Leitfaden zu den ISO 14644-Normen für die Klassifizierung der Luftreinheit in Reinräumen. ↩
-
die Prinzipien der Dampfsterilisation zu verstehen, einschließlich der Rolle von Zeit, Temperatur und Druck. ↩



