Forkert valg af kabelforskruninger i medicinske miljøer og renrum medfører risiko for kontaminering, manglende overholdelse af lovgivningen og funktionsfejl i udstyret, hvilket resulterer i fare for patientsikkerheden, dyre nedlukninger af anlæg og overtrædelser af FDA, mens utilstrækkelig tætning, uhensigtsmæssige materialer og dårlig rengøringsevne fører til bakterievækst, partikelforurening og sterilitetsbrud, der kompromitterer kritiske operationer i sundhedsvæsenet. Mange institutionsledere kæmper med at vælge kirtler, der opfylder strenge medicinske standarder og samtidig opretholder en pålidelig elektrisk ydeevne.
Valg af kabelforskruninger til medicinsk udstyr og renrum kræver forståelse af FDA's regler, USP klasse VI1 materialekrav, IP68+ forseglingsstandarder og behov for renrumsklassificering med konstruktion i rustfrit stål af medicinsk kvalitet eller specialiseret polymer, der giver biokompatibilitet, kemisk modstandsdygtighed og glatte overflader til effektiv rengøring og sterilisering, samtidig med at den elektriske integritet bevares i kritiske sundhedsapplikationer. Succes afhænger af balancen mellem overholdelse af lovgivningen og driftssikkerhed.
Efter at have arbejdet med hospitalsingeniører på store medicinske centre i Boston, farmaceutiske producenter i Schweiz og renrumsfaciliteter i hele Singapore har jeg lært, at kabelforskruninger af medicinsk kvalitet er afgørende for at opretholde sterile miljøer og sikre patientsikkerheden. Lad mig dele den kritiske viden om valg af optimale forskruninger til dine medicinske og renrumsapplikationer.
Indholdsfortegnelse
- Hvad adskiller medicinske kabelforskruninger fra standardforskruninger?
- Hvordan opfylder du FDA's regler for medicinsk udstyr?
- Hvilke materialer er nødvendige til renrumsapplikationer?
- Hvordan sikrer du korrekt rengøring og steriliseringskompatibilitet?
- Hvad er de vigtigste udvælgelseskriterier for forskellige medicinske anvendelser?
- Ofte stillede spørgsmål om medicinske kabelforskruninger
Hvad adskiller medicinske kabelforskruninger fra standardforskruninger?
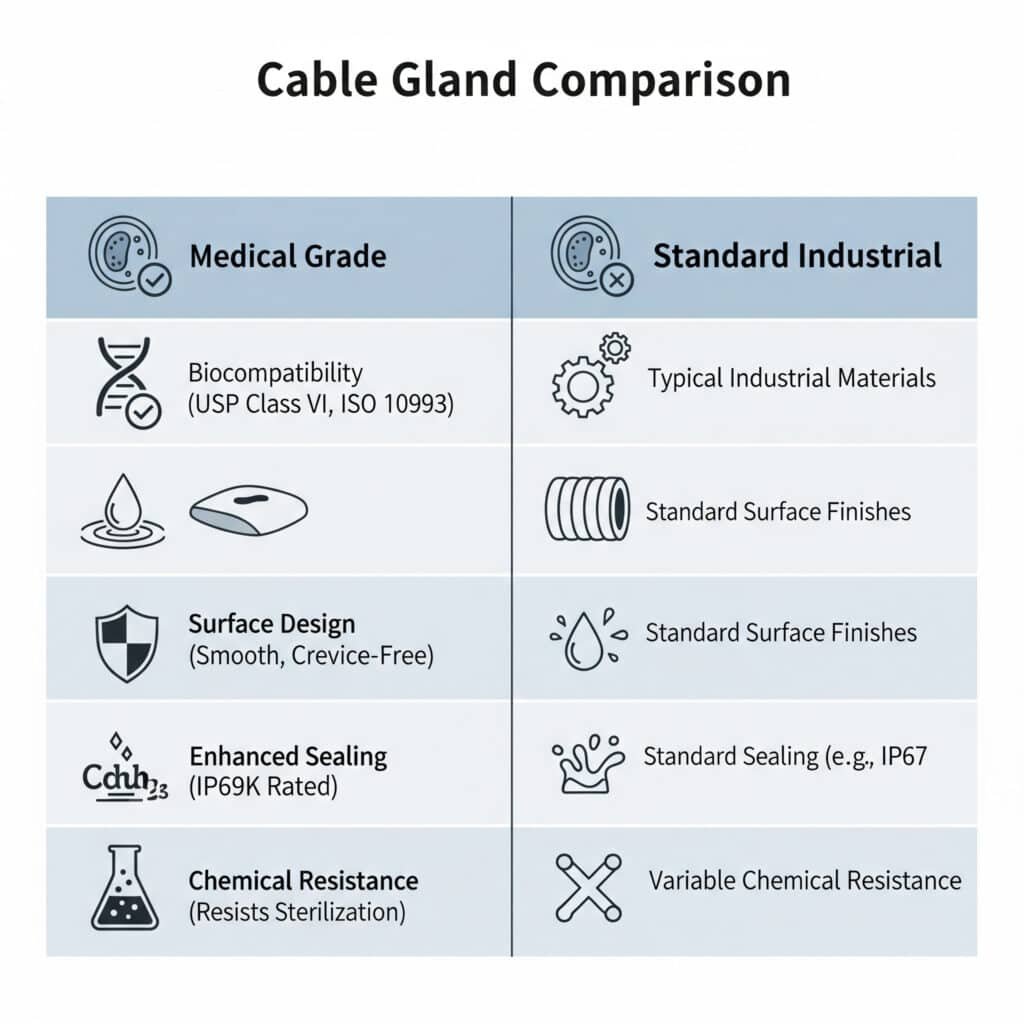
Medicinske kabelforskruninger adskiller sig fra standardforskruninger ved at bruge biokompatible materialer, have glatte overflader, der kan rengøres, opfylde FDA-reglerne, give forbedret forsegling til forebyggelse af kontaminering og tilbyde kemisk modstandsdygtighed over for rengøringsmidler og steriliseringsprocesser med specialdesign, der eliminerer sprækker, hvor bakterier kan husere, samtidig med at den elektriske ydeevne opretholdes i kritiske sundhedsmiljøer.
Det er afgørende at forstå disse forskelle, fordi medicinske anvendelser har unikke sikkerheds- og lovkrav, som almindelige industrielle forskruninger ikke kan opfylde.
Krav til biokompatibilitet
Overensstemmelse med USP klasse VI: Medicinske kabelforskruninger skal bruge materialer, der består United States Pharmacopeia Class VI biologisk test for biokompatibilitet og sikkerhed i medicinsk udstyr.
ISO 10993 standarder: Materialer skal opfylde ISO 109932 biologiske evalueringsstandarder for medicinsk udstyr, der sikrer, at der ikke er cytotoksiske, sensibiliserende eller irriterende virkninger på menneskeligt væv.
FDA 21 CFR 177 Godkendelse: Fødevaregodkendte materialer, der opfylder FDA's regler for direkte og indirekte fødevarekontakt, er ofte påkrævet til farmaceutisk og medicinsk udstyr.
Biokompatible polymerer: Specialiserede materialer som PEEK af medicinsk kvalitet, PTFE eller nyloner af farmaceutisk kvalitet giver biokompatibilitet uden at gå på kompromis med de mekaniske egenskaber.
Overfladedesign for rengøringsvenlighed
Glat overfladefinish: Medicinske kirtler har ultraglatte overflader med Ra-værdier på typisk under 0,8 mikrometer for at forhindre bakterieadhæsion og muliggøre effektiv rengøring.
Sprækkefrit design: Eliminering af skarpe hjørner, dybe gevind og komplekse geometrier, der kan huse bakterier eller modstå rengørings- og steriliseringsprocesser.
Afrundede kanter: Alle udvendige overflader har afrundede kanter og glatte overgange for at lette rengøringen og forhindre skader på renrumshandsker eller steril emballage.
Minimalt overfladeareal: Strømlinede designs minimerer det overfladeareal, der udsættes for forurening, samtidig med at den nødvendige mekaniske og elektriske ydeevne opretholdes.
Forbedret forseglingsevne
IP68+-klassificering: Overlegen miljøbeskyttelse ud over standard IP68, der ofte opnår IP69K til højtryks- og højtemperaturrengøring.
Forureningsbarrierer: Flere forseglingstrin forhindrer indtrængning af partikler, bakterier og rengøringskemikalier, der kan kompromittere sterile miljøer.
Modstandsdygtighed over for tryk: Forbedrede trykværdier for at modstå aggressive rengøringsprocedurer og steriliseringsprocesser uden tætningsfejl.
Pålidelighed på lang sigt: Forseglingsmaterialer bevarer deres integritet gennem gentagne steriliseringscyklusser og udsættelse for skrappe rengøringskemikalier.
Egenskaber for kemisk resistens
Kompatibilitet med rengøringsmidler: Modstandsdygtig over for desinfektionsmidler af hospitalskvalitet, kvaternære ammoniumforbindelser, hydrogenperoxid og andre aggressive rengøringskemikalier.
Modstandsdygtighed over for sterilisering: Materialerne tåler gammastråling, ethylenoxid, dampautoklavering og andre steriliseringsmetoder uden at blive nedbrudt.
Farmaceutiske kemikalier: Modstandsdygtighed over for opløsningsmidler, syrer, baser og farmaceutiske forbindelser, der ofte findes i medicinske produktionsmiljøer.
Temperaturstabilitet: Oprethold egenskaber gennem steriliseringstemperaturcyklusser og krav til temperaturkontrol i renrum.
David, der er facility manager på en større farmaceutisk fabrik i New Jersey, stod over for tilbagevendende forureningsproblemer i deres sterile påfyldningslinjer, hvor standard kabelforskruninger husede bakterier på trods af strenge rengøringsprotokoller. De eksisterende messingforskruninger havde komplekse gevindmønstre og overfladefinish, som ikke kunne steriliseres tilstrækkeligt, hvilket førte til afvisning af partier og problemer med at overholde FDA's regler. Vi specificerede kabelforskruninger i rustfrit stål af medicinsk kvalitet med elektropolerede overflader og sprækkefrit design, der opfyldte USP Class VI-kravene. Opgraderingen eliminerede forureningskilder, opnåede 99,9% rengøringseffektivitet og hjalp anlægget med at bestå FDA-inspektioner, samtidig med at antallet af afviste produkter blev reduceret med 85%. 😊
Hvordan opfylder du FDA's regler for medicinsk udstyr?
For at overholde FDA's og det medicinske udstyrs regler skal man bruge materialer med korrekte certificeringer, vedligeholde detaljeret dokumentation og følge God fremstillingspraksis (GMP)3Det kræver FDA-godkendte materialer, biokompatibilitetstest og produktionskontrol, der sikrer ensartet kvalitet og sikkerhed i forbindelse med medicinsk udstyr, og som er i overensstemmelse med 21 CFR Part 820.
Overholdelse af lovgivningen er ikke til forhandling i medicinske applikationer, fordi fejl kan resultere i patientskader, produkttilbagekaldelser og alvorlige juridiske konsekvenser.
FDA's krav til materialer
21 CFR del 177: Materialer i kontakt med lægemidler eller medicinsk udstyr skal opfylde FDA's regler for fødevaretilsætningsstoffer for indirekte fødevarekontaktstoffer.
Master Access File (MAF): Leverandører skal vedligeholde FDA Master Access Files, der dokumenterer materialesikkerhed, fremstillingsprocesser og kvalitetskontrolprocedurer.
Drug Master File (DMF): Til farmaceutiske anvendelser kan materialer kræve Drug Master File-registrering med detaljerede oplysninger om sammensætning og fremstilling.
Certifikat for overensstemmelse: Leverandører skal fremlægge certifikater, der bekræfter, at materialerne opfylder alle gældende FDA-regler og -specifikationer.
Kvalitetsstandarder for medicinsk udstyr
Overholdelse af ISO 13485: Produktionen skal følge ISO 13485-kvalitetsstyringssystemer for medicinsk udstyr til design, produktion og overvågning efter markedsføring.
21 CFR del 820 (QSR): Overholdelse af kvalitetssystemforordningen, der sikrer korrekt designkontrol, dokumentkontrol og korrigerende/forebyggende handlinger.
Risikostyring: ISO 14971 risikostyringsprocesser for medicinsk udstyr, herunder risikoanalyse, evaluering og kontrolforanstaltninger.
Designkontrol: Formelle designkontrolprocesser, herunder designplanlægning, input/output-krav, gennemgang, verifikation og validering.

Dokumentation og sporbarhed
Materialecertifikater: Komplet materialesporbarhed med analysecertifikater, resultater af biokompatibilitetstest og dokumentation for overholdelse af lovgivningen.
Produktionsoptegnelser: Detaljerede produktionsjournaler, herunder procesparametre, kvalitetskontroltest og batchdokumentation for fuld sporbarhed.
Kontrol af ændringer: Formelle procedurer for ændringskontrol for alle ændringer af materialer, processer eller specifikationer, der påvirker overholdelse af lovgivningen.
Kvalificering af leverandører: Omfattende leverandørkvalificeringsprogrammer, der sikrer, at alle materialer og komponenter opfylder kravene til medicinsk udstyr.
Krav til validering
Test af biokompatibilitet: USP klasse VI-test, herunder systemisk injektion, intrakutan og implantationstest for at verificere biologisk sikkerhed.
Validering af rengøring: Dokumenterede rengøringsprocedurer med valideringsdata, der beviser effektiv fjernelse af forurenende stoffer og reduktion af bioburden.
Validering af sterilisering: Validering af steriliseringsprocesser, herunder kortlægning af doser, sikringsniveauer for sterilitet og undersøgelser af materialekompatibilitet.
Test af ydeevne: Elektrisk, mekanisk og miljømæssig testning for at verificere, at ydeevnen opfylder kravene til medicinsk udstyr i hele produktets livscyklus.
Støtte til regulatorisk indsendelse
510(k)-dokumentation: Teknisk dokumentation, der understøtter FDA 510(k)-ansøgninger for medicinsk udstyr med kabelforskruninger.
Tekniske filer: Omfattende tekniske filer til CE-mærkning i henhold til forordningen om medicinsk udstyr (MDR) på de europæiske markeder.
Kvalitetsaftaler: Formelle kvalitetsaftaler med leverandører, der definerer ansvar, specifikationer og krav til overholdelse.
Støtte til revision: Støtte til FDA, bemyndigede organer og kundeaudits, herunder gennemgang af dokumentation og facilitetsinspektioner.
Hvilke materialer er nødvendige til renrumsapplikationer?
Renrumsapplikationer kræver materialer med lave afgasningsegenskaber, modstandsdygtighed over for partikeldannelse, kemisk kompatibilitet med rengøringsmidler, glatte ikke-porøse overflader og passende ledningsevneniveauer, hvor rustfrit stål 316L af medicinsk kvalitet, PEEK, PTFE og specialiserede renrumsgodkendte polymerer giver optimal ydeevne og samtidig opfylder kravene. ISO 146444 renrumsstandarder og opretholdelse af elektrisk integritet i kontrollerede miljøer.
Materialevalg er afgørende, fordi renrum kræver streng kontrol med partikel- og molekylær kontaminering, der kan kompromittere produktkvaliteten eller de sterile forhold.
Krav til rustfrit stål
316L medicinsk kvalitet: Austenitisk rustfrit stål med lavt kulstofindhold, der giver overlegen korrosionsbestandighed og biokompatibilitet til medicinske anvendelser.
Elektropoleret finish: Elektropolering fjerner ujævnheder i overfladen, reducerer partikeldannelsen og skaber glatte overflader til effektiv rengøring.
Passiveringsbehandling: Kemisk passivering forbedrer korrosionsbestandigheden og fjerner jernforurening, der kan forårsage misfarvning eller partikeldannelse.
Overfladens ruhed: Ra-værdier under 0,8 mikrometer (32 mikrotommer) minimerer bakteriel vedhæftning og letter rengørings- og steriliseringsprocesser.
Højtydende polymerer
PEEK (polyetheretherketon): Fremragende kemisk modstandsdygtighed, lav afgasning og biokompatibilitet gør PEEK ideel til farmaceutisk og medicinsk udstyr.
PTFE (polytetrafluorethylen): Overlegen kemisk inerti og non-stick-egenskaber giver fremragende modstandsdygtighed over for rengøringskemikalier og biologiske materialer.
Nylons af medicinsk kvalitet: Specielt formulerede nyloner med USP Class VI-godkendelse giver gode mekaniske egenskaber med biokompatibilitet til medicinske anvendelser.
Renrumsgodkendt POM: Polyoxymethylen med lav partikeldannelse og god dimensionsstabilitet til præcisionsrenrumsopgaver.
Kompatibilitet med renrumsklassificering
ISO-klasse 5 (klasse 100): Ultraglatte overflader med minimal partikeldannelse til halvleder- og lægemiddelproduktion.
ISO-klasse 6 (klasse 1000): Moderat partikelkontrol til fremstilling af medicinsk udstyr og visse farmaceutiske processer.
ISO-klasse 7 (klasse 10000): Standard renrumskrav til generelle farmaceutiske og medicinske samleprocesser.
ISO-klasse 8 (klasse 100000): Grundlæggende renrumskrav til emballage og visse fremstillingsprocesser for medicinsk udstyr.
Kontrol af afgasning og forurening
Materialer med lav afgasning: Materialer med minimal udledning af flygtige organiske forbindelser (VOC), der kan forurene følsomme processer eller produkter.
Molekylær forurening: Kontrol af molekylære forureninger, herunder silikoner, blødgørere og andre organiske forbindelser, der kan påvirke produktkvaliteten.
Ionisk forurening: Materialer med lavt ionindhold for at forhindre kontaminering af elektroniske komponenter og farmaceutiske produkter.
Ekstraherbare stoffer: Minimalt med ekstraherbare stoffer, der kan udvaskes til farmaceutiske produkter eller rengøringsmidler under brug.
Matrix for kemisk kompatibilitet
| Rengøringsmiddel | 316L SS | PEEK | PTFE | Medicinsk nylon |
|---|---|---|---|---|
| Isopropylalkohol | Fremragende | Fremragende | Fremragende | God |
| Hydrogenperoxid | Fremragende | Fremragende | Fremragende | Fair |
| Kvaternært ammonium | Fremragende | Fremragende | Fremragende | God |
| Natriumhypoklorit | God | Fremragende | Fremragende | Dårlig |
| Pereddikesyre | God | Fremragende | Fremragende | Dårlig |
Hassan, som er driftsleder på et topmoderne farmaceutisk anlæg i Schweiz, havde brug for at opgradere kabelforskruninger i deres ISO klasse 5-renrum til fremstilling af sterile injektionsvæsker. De eksisterende kabelforskruninger genererede partikler under rengøringscyklusser og kunne ikke modstå de aggressive steriliseringsprotokoller, der kræves til deres nye biologiske produkter. Vi leverede elektropolerede kabelforskruninger i rustfrit stål 316L med valideret lav partikelgenerering og fuldstændig kemisk kompatibilitet med deres rengørings- og steriliseringsprocesser. Opgraderingen opnåede partikelantal 90% under ISO klasse 5-grænserne, eliminerede rengøringsrelaterede kontamineringshændelser og understøttede en vellykket validering af deres nye sterile produktionslinje.
Hvordan sikrer du korrekt rengøring og steriliseringskompatibilitet?
For at sikre korrekt rengørings- og steriliseringskompatibilitet skal man vælge materialer, der kan modstå gentagen eksponering for rengøringskemikalier og steriliseringsmetoder, designe overflader til fuldstændig rengøring, validere rengøringsprocedurer og vedligeholde detaljeret dokumentation, hvor medicinske kabelforskruninger kræver glatte overflader uden sprækker, kemikalieresistente materialer og validerede rengøringsprotokoller, der opnår de krævede sterilitetssikringsniveauer.
Kompatibilitet med rengøring og sterilisering er afgørende, fordi utilstrækkelig dekontaminering kan føre til produktkontaminering, patientsikkerhedsrisici og overtrædelser af lovgivningen.
Steriliseringsmetodens kompatibilitet
Autoklavering med damp: Materialer skal kunne modstå 121°C-134°C Autoklavering med damp5 cyklusser uden nedbrydning, dimensionsændringer eller tætningsfejl.
Gammastråling: Modstandsdygtighed over for gammastrålingsdoser på 25-50 kGy, som ofte bruges til sterilisering af medicinsk udstyr, uden at materialet nedbrydes.
Ethylenoxid (EtO): Kemisk kompatibilitet med EtO-sterilisering, herunder modstandsdygtighed over for steriliseringsmidlet og korrekte afgasningsegenskaber.
Hydrogenperoxid-plasma: Kompatibilitet med lavtemperaturplasmasteriliseringssystemer, herunder materialestabilitet og fuldstændig indtrængning af steriliseringsmiddel.
Krav til validering af rengøring
Rengøringsprocedurer: Dokumenterede rengøringsprocedurer med angivelse af kemikalier, koncentrationer, kontakttider og mekaniske handlinger, der er nødvendige for effektiv dekontaminering.
Valideringsprotokoller: Formelle valideringsundersøgelser, der viser rengøringseffektivitet ved hjælp af worst case-forureningsscenarier og analytiske test.
Acceptkriterier: Definerede acceptkriterier for renlighed, herunder visuel inspektion, partikeltælling, bioburden-niveauer og grænser for kemiske rester.
Rutinemæssig overvågning: Løbende overvågningsprogrammer for at verificere den fortsatte rengøringseffektivitet og identificere enhver forringelse af ydeevnen.
Overvejelser om overfladedesign
Afvandingsfunktioner: Designfunktioner, der fremmer fuldstændig dræning af rengøringsmidler og forhindrer ansamlinger, der kan rumme forurenende stoffer.
Tilgængelighed: Alle overflader skal være tilgængelige for rengøring med standard rengøringsredskaber og -procedurer, der anvendes i medicinske faciliteter.
Krav til adskillelse: Overvej, om kirtlerne skal skilles ad for at blive rengjort, eller om intakt rengøring er tilstrækkelig til opgaven.
Udskiftning af pakning: Procedurer for udskiftning af pakninger og validering, når tætningskomponenter kræver periodisk udskiftning på grund af eksponering for rengøringskemikalier.
Dokumentation og overholdelse
Instruktioner for rengøring: Detaljerede rengøringsinstruktioner, herunder trinvise procedurer, kemiske specifikationer og sikkerhedsforanstaltninger.
Materialesikkerhedsdata: Komplet information om materialesikkerhed, herunder kemisk kompatibilitet, temperaturgrænser og steriliseringskompatibilitet.
Valideringsrapporter: Rengøringsvalideringsrapporter, der viser effektivitet og fastlægger krav til rutinemæssig overvågning.
Træningsmaterialer: Uddannelsesmateriale til personale på institutioner om korrekt rengøring, håndtering og vedligeholdelsesprocedurer for medicinske kabelforskruninger.
Test af kvalitetskontrol
Test af biologisk belastning: Regelmæssig testning for mikrobiel kontaminering for at verificere rengøringseffektiviteten og identificere potentielle problemområder.
Test af endotoksin: Test for bakterielle endotoksiner, der kan forårsage pyrogene reaktioner i farmaceutiske og medicinske applikationer.
Partikeltælling: Test af partikelantal for at verificere, at renrumskravene overholdes efter rengørings- og vedligeholdelsesaktiviteter.
Analyse af kemiske rester: Test for rester af rengøringskemikalier, der kan forurene produkter eller påvirke biokompatibiliteten.
Hvad er de vigtigste udvælgelseskriterier for forskellige medicinske anvendelser?
De vigtigste udvælgelseskriterier varierer fra applikation til applikation, men omfatter krav til overholdelse af lovgivning, biokompatibilitetsniveauer, renrumsklassifikationer, steriliseringsmetoder, kemisk eksponering og behov for elektrisk ydeevne, hvor kirurgisk udstyr kræver den højeste biokompatibilitet, farmaceutisk produktion kræver kemisk modstandsdygtighed og diagnostisk udstyr fokuserer på elektrisk integritet, mens alle applikationer kræver passende lovgivningsmæssige certificeringer og rengøringskompatibilitet.
Forskellige medicinske anvendelser har unikke krav, som skal overvejes nøje ved valg af kabelforskruninger for at sikre optimal ydeevne og overholdelse af lovgivningen.
Kirurgisk udstyr og udstyr til patientkontakt
Krav til direkte kontakt: USP klasse VI biokompatibilitet med yderligere cytotoksicitetstest for materialer i direkte patientkontakt under kirurgiske indgreb.
Steriliseringsfrekvens: Evne til at modstå hyppige steriliseringscyklusser uden nedbrydning, hvilket typisk kræver materialer, der er stabile gennem hundredvis af steriliseringscyklusser.
Elektrisk sikkerhed: Forbedrede krav til elektrisk sikkerhed, herunder lav lækstrøm og pålidelig isolering af patienttilsluttet udstyr.
Pålidelighed i nødsituationer: Kritiske pålidelighedskrav til livsopretholdende og akutmedicinsk udstyr, hvor fejl direkte kan påvirke patientsikkerheden.
Farmaceutisk produktion
Overholdelse af GMP: Krav til god fremstillingspraksis, herunder materialesporbarhed, ændringskontrol og valideringsdokumentation.
Sikkerhed ved produktkontakt: Materialer, der ikke forurener farmaceutiske produkter gennem udvaskning, partikeldannelse eller kemisk interaktion.
Validering af rengøring: Omfattende krav til rengøringsvalidering med dokumenterede procedurer og acceptkriterier for farmaceutisk produktion.
Batch-dokumentation: Komplet batchdokumentation og sporbarhed for materialer, der bruges i farmaceutisk produktionsudstyr.
Diagnose- og laboratorieudstyr
Krav til præcision: Dimensionsstabilitet og præcision til analyseinstrumenter, der kræver ensartet mekanisk og elektrisk ydeevne.
Kemisk modstandsdygtighed: Modstandsdygtighed over for laboratoriekemikalier, reagenser og rengøringsmidler, der ofte bruges i diagnostiske anvendelser.
EMC Performance: Krav til elektromagnetisk kompatibilitet for følsomme analyseinstrumenter og diagnostisk udstyr.
Kalibreringens stabilitet: Mekanisk stabilitet, der ikke påvirker instrumentets kalibrering eller målenøjagtighed over tid.
Fremstilling af medicinsk udstyr
Procesvalidering: Materialer og komponenter, der understøtter kravene til procesvalidering ved fremstilling af medicinsk udstyr.
Kvalitetssystemer: Integration med ISO 13485-kvalitetssystemer, herunder leverandørkvalificering og procedurer for indgående inspektion.
Risikostyring: Materialer, der understøtter kravene til risikostyring af medicinsk udstyr, herunder analyse af fejltilstande og strategier for afhjælpning.
Regulatorisk støtte: Leverandørstøtte til regulatoriske indsendelser, herunder teknisk dokumentation og regulatorisk ekspertise.
Beslutningsmatrix for udvælgelse
| Applikationstype | Primære kriterier | Sekundære kriterier | Kritiske standarder |
|---|---|---|---|
| Kirurgisk udstyr | Biokompatibilitet | Sterilisering | USP klasse VI, ISO 10993 |
| Farmaceutisk | Kemisk modstandsdygtighed | Overholdelse af GMP | FDA 21 CFR, cGMP |
| Diagnostisk | Præcision | EMC's ydeevne | IEC 61326, ISO 15189 |
| Produktion | Validering af processer | Kvalitetssystemer | ISO 13485, 21 CFR 820 |
Cost-benefit-analyse
Indledende omkostninger vs. livscyklus: Overvej de samlede ejeromkostninger, herunder omkostninger til vedligeholdelse, udskiftning og overholdelse af regler i hele udstyrets levetid.
Regulatorisk risiko: Afvej de materielle omkostninger i forhold til risici ved overholdelse af lovgivningen og potentielle omkostninger ved manglende overholdelse.
Krav til ydeevne: Sørg for, at de valgte materialer opfylder minimumskravene til ydeevne uden at overspecificere, hvilket øger omkostningerne unødigt.
Leverandørens evner: Evaluer leverandørernes muligheder for løbende support, dokumentation og hjælp til overholdelse af lovgivningen.
Konklusion
Valg af kabelforskruninger til medicinsk udstyr og renrum kræver forståelse af de unikke krav til lovgivning, materialer og ydeevne, der adskiller disse anvendelser fra almindelige industrielle anvendelser. Succes afhænger af balancen mellem biokompatibilitet, rengøringsvenlighed, overholdelse af regler og elektrisk ydeevne.
Nøglen til pålidelige medicinske kabelforskruninger ligger i at arbejde med leverandører, der forstår reglerne for medicinsk udstyr og kan levere passende materialer, dokumentation og løbende support i hele produktets livscyklus. Hos Bepto har vi specialiseret os i kabelforskruninger af medicinsk kvalitet, der opfylder FDA-krav og internationale standarder for medicinsk udstyr, og som giver den kvalitetssikring og lovgivningsmæssige støtte, der er nødvendig for kritiske sundhedsapplikationer.
Ofte stillede spørgsmål om medicinske kabelforskruninger
Q: Hvilke certificeringer skal jeg bruge til medicinske kabelforskruninger?
A: Medicinske kabelforskruninger kræver typisk USP Class VI-biokompatibilitetscertificering, FDA 21 CFR-overholdelse for materialer og ISO 13485-kvalitetssystemer til fremstilling. Specifikke krav afhænger af din anvendelse og lovgivningsmæssige jurisdiktion.
Spørgsmål: Kan almindelige kabelforskruninger i rustfrit stål bruges til medicinske formål?
A: Almindeligt rustfrit stål opfylder måske ikke de medicinske krav. Medicinske anvendelser kræver 316L rustfrit stål af medicinsk kvalitet med elektropoleret finish, test af biokompatibilitet og korrekt dokumentation for overholdelse af lovgivningen.
Q: Hvordan rengør og steriliserer jeg medicinske kabelforskruninger?
A: Følg producentens validerede rengøringsprocedurer med godkendte rengøringsmidler og steriliseringsmetoder. De fleste medicinske kirtler understøtter dampautoklavering, gammastråling eller kemisk sterilisering med korrekt materialekompatibilitet.
Q: Hvad er forskellen på kabelforskruninger til renrum og medicinsk brug?
A: Medicinsk kvalitet omfatter krav til biokompatibilitet og FDA-overholdelse, mens renrumskvalitet fokuserer på partikelkontrol og kemisk resistens. Nogle anvendelser kræver både medicinske og renrumsspecifikationer.
Q: Hvor ofte skal medicinske kabelforskruninger udskiftes?
A: Udskiftningsfrekvensen afhænger af steriliseringscyklusser, kemisk eksponering og producentens anbefalinger. Inspicér typisk efter hver 100-200 steriliseringscyklusser, og udskift på baggrund af tilstandsvurdering og valideringskrav.
-
Få mere at vide om de specifikke biologiske reaktivitetstest, der kræves for USP Class VI-certificering. ↩
-
Få et overblik over ISO 10993-serien af standarder for biologisk evaluering af medicinsk udstyr. ↩
-
Gennemgå de officielle FDA-retningslinjer og -regler for Current Good Manufacturing Practices (cGMP). ↩
-
Udforsk en detaljeret guide til ISO 14644-standarderne for klassificering af luftens renhed i renrum. ↩
-
Forstå principperne for dampsterilisering, herunder betydningen af tid, temperatur og tryk. ↩



