Selhání sterilizace zdravotnických prostředků stojí výrobce ročně miliony, přičemž 15-20% selhání je připisováno nedostatečnému odvětrávání, které brání správnému pronikání sterilizačního prostředku. Standardní odvzdušňovací zátky selhávají pod autokláv1 teploty 121-134 °C nebo degradují při vystavení působení sterilizace ethylenoxidem (ETO)2 chemikálií, což ohrožuje zajištění sterility a dodržování předpisů.
Sterilizovatelné ventilační zátky umožňují účinnou sterilizaci tím, že umožňují průnik páry nebo plynu ETO a zároveň zachovávají sterilní bariéry po sterilizaci. Ventilační otvory s PTFE membránou odolávají teplotám v autoklávu až do 150 °C a jsou odolné vůči chemické degradaci ETO, což zajišťuje spolehlivé udržení sterility zdravotnických prostředků, farmaceutického vybavení a laboratorních přístrojů vyžadujících validované sterilizační procesy.
V loňském roce jsem spolupracoval s Dr. Sarah Mitchellovou, ředitelkou kvality předního výrobce zdravotnických prostředků v Bostonu, který se potýkal se selháním validace sterilizace obalů svých implantabilních prostředků. Jejich standardní nylonové ventilační zátky se během cyklů v autoklávu tavily a bránily správnému průniku páry. Po přechodu na naše sterilizovatelné ventilační zátky z PTFE farmaceutické kvality s ověřenou teplotní odolností dosáhli sterilizační účinnosti 100% v 1 000 validačních cyklech - zajistili tak shodu s předpisy FDA a bezpečnost pacientů! 🏥
Obsah
- Co jsou sterilizovatelné ventilační zátky a proč jsou důležité?
- Jak ovlivňují různé metody sterilizace materiály ventilačních zátek?
- Které materiály jsou nejlepší pro sterilizaci v autoklávu?
- Jaké materiály se nejlépe hodí pro sterilizační procesy ETO?
- Jak vybrat a ověřit sterilizovatelné ventilační zátky?
- Časté dotazy týkající se sterilizovatelných ventilačních zátek
Co jsou sterilizovatelné ventilační zátky a proč jsou důležité?
Pochopení úlohy sterilizovatelných ventilačních zátek ve výrobě zdravotnických prostředků a léčiv je nezbytné pro zachování sterility a shody s předpisy.
Sterilizovatelné ventilační zátky jsou specializované prodyšné ventilační otvory navržené tak, aby odolávaly sterilizačním procesům a zároveň umožňovaly průnik sterilizačních prostředků a zachování sterilních bariér. Umožňují vytlačování vzduchu během sterilizace, zabraňují vzniku podtlaku během chlazení a udržují sterilní podmínky po sterilizaci. Mezi kritické aplikace patří obaly na zdravotnické prostředky, farmaceutické nádoby, laboratorní zařízení a zařízení pro sterilní zpracování.
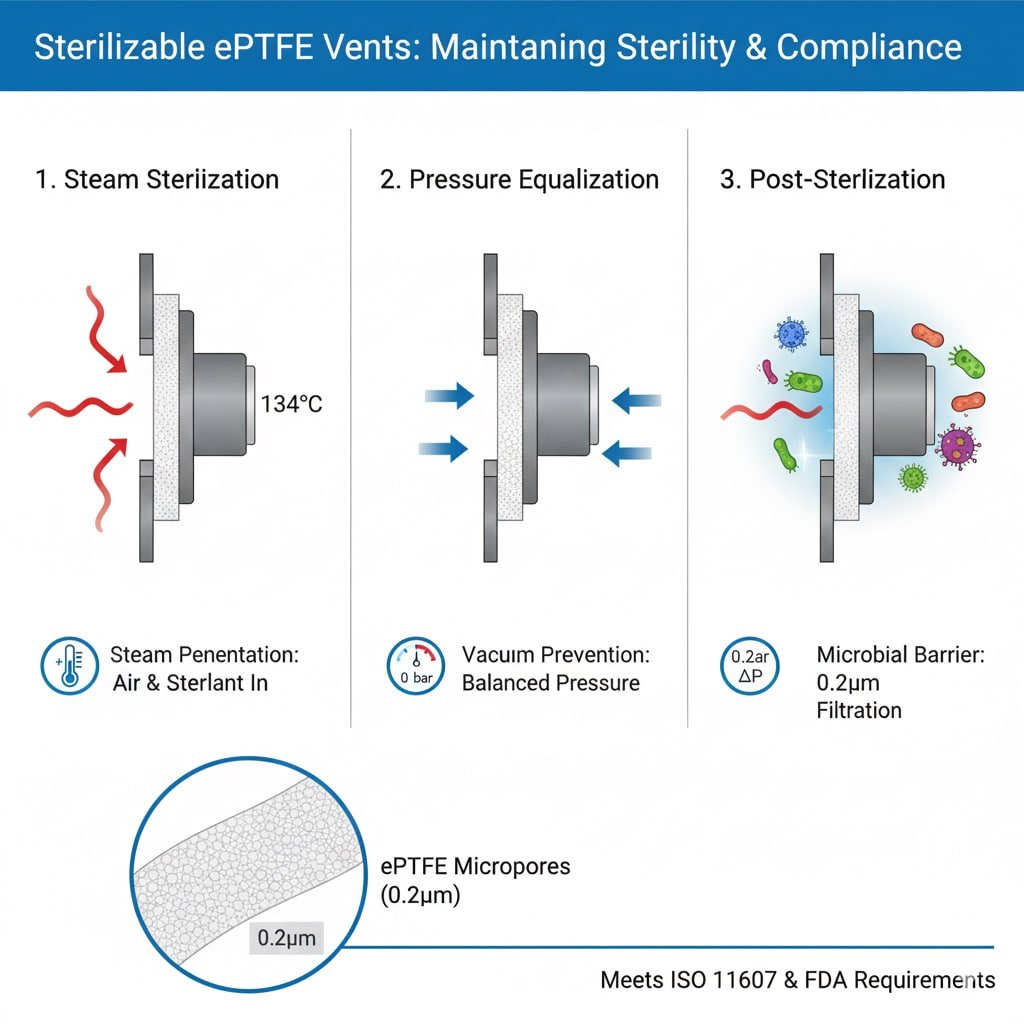
Požadavky na sterilizační proces
Pronikání páry: Sterilizace v autoklávu vyžaduje, aby pára pronikla do obalu a dostala se do kontaktu se všemi povrchy, což vyžaduje větrací otvory, které umožňují proudění plynu a zároveň zachovávají mikrobiální bariéry.
Výtlak vzduchu: Účinná sterilizace vyžaduje úplné odstranění vzduchu a jeho nahrazení sterilizačním prostředkem, což ventily umožňují prostřednictvím řízené výměny plynů.
Vyrovnání tlaku: Sterilizační cykly vytvářejí tlakové rozdíly, kterým se musí přizpůsobit ventilační otvory, aniž by došlo k narušení sterilních bariér nebo integrity balení.
Kritické parametry výkonu
Teplotní odolnost: Sterilizovatelné průduchy si musí zachovat strukturální integritu a filtrační výkon při sterilizačních teplotách od 121 °C do 150 °C.
Chemická kompatibilita: Materiály musí být odolné proti degradaci sterilizačními chemikáliemi včetně páry, ethylenoxidu, peroxidu vodíku a ozonu.
Účinnost mikrobiální bariéry: Po sterilizaci musí větrací otvory spolehlivě zajistit mikrobiální bariéra3 s velikostí pórů obvykle 0,2-0,22 mikronu pro zadržování bakterií.
Úvahy o dodržování právních předpisů
Požadavky FDA na validaci: Aplikace pro zdravotnické prostředky vyžadují validované sterilizační procesy s dokumentovaným výkonem ventilace v průběhu sterilizačních cyklů.
Dodržování norem ISO: Sterilizovatelné větrací otvory musí splňovat ISO 116074 normy pro balení a požadavky na parní sterilizaci podle normy ISO 17665 pro lékařské aplikace.
Testování biokompatibility: Aplikace pro kontakt se zdravotnickými prostředky mohou vyžadovat testování biokompatibility třídy VI podle USP pro zajištění bezpečnosti pacienta.
Kategorie aplikací
Obaly pro zdravotnické prostředky: Sterilní obaly pro implantáty, chirurgické nástroje a jednorázové zdravotnické prostředky vyžadující zachování sterility až do použití.
Farmaceutická výroba: Sterilní zpracovatelská zařízení, bioreaktory a farmaceutické nádoby vyžadující validované sterilizační procesy.
Laboratorní vybavení: Autoklávovatelné laboratorní nádoby, kultivační nádoby a analytické vybavení vyžadující sterilní podmínky pro přesné výsledky.
Jak ovlivňují různé metody sterilizace materiály ventilačních zátek?
Různé metody sterilizace vytvářejí pro materiály ventilačních zátek jedinečné výzvy, které vyžadují specifické vlastnosti materiálu a konstrukční hlediska pro optimální výkon.
Při parní sterilizaci jsou materiály vystaveny vysokým teplotám (121-134 °C) a podmínkám nasycené páry, které mohou způsobit tepelnou degradaci, rozměrové změny a poškození membrán. ETO sterilizace vystavuje materiály reaktivním chemikáliím při nižších teplotách (37-63 °C), ale delší době expozice, která může způsobit chemickou degradaci a odplynění. Každá metoda vyžaduje specifický výběr materiálu pro spolehlivý výkon.
Účinky parní sterilizace
Tepelné namáhání: Vysoké teploty způsobují tepelnou roztažnost, možné tavení termoplastických součástí a degradaci materiálů citlivých na teplotu.
Hydrolýzní reakce5: Působení páry může způsobit hydrolytickou degradaci některých polymerů, zejména polyesterů a některých polyamidů.
Rozměrová stabilita: Opakované tepelné cykly mohou způsobit rozměrové změny, které ovlivňují těsnicí vlastnosti a účinnost filtrace.
Problémy při sterilizaci ETO
Chemická reaktivita: Etyloxid reaguje s materiály obsahujícími atomy aktivního vodíku, čímž může dojít ke změně vlastností materiálu a vzniku toxických zbytků.
Požadavky na zplodiny: Výrobky sterilizované ETO vyžadují před bezpečným použitím prodlouženou dobu provzdušňování, aby se odstranil absorbovaný ETO a reakční produkty.
Charakteristiky průniku: ETO vyžaduje pro účinnou penetraci specifické vlhkostní a teplotní podmínky, což ovlivňuje požadavky na konstrukci ventilace.
Účinky plazmy peroxidu vodíku
Oxidační degradace: Plazma H2O2 vytváří vysoce reaktivní formy, které mohou rozkládat organické materiály oxidačními reakcemi.
Kompatibilita materiálů: Mnohé elastomery a některé plasty jsou neslučitelné se sterilizací plazmou H2O2 z důvodu rychlé degradace.
Výhody při nízkých teplotách: Plazmová sterilizace probíhá při nízkých teplotách (45-55 °C), což snižuje tepelné namáhání materiálů citlivých na teplotu.
Úvahy o záření gama
Poškození zářením: Vysokoenergetické záření gama může způsobit štěpení nebo zesíťování polymerních řetězců, což výrazně mění vlastnosti materiálu.
Akumulace dávky: Opakovaná sterilizace gama zářením může způsobit kumulativní poškození, což omezuje počet sterilizačních cyklů, které mohou materiály vydržet.
Požadavky na antioxidanty: Přípravky odolné vůči záření často vyžadují antioxidanty, aby se zabránilo oxidační degradaci během ozařování a po něm.
Nedávno jsem pomohl Ahmedu Al-Rashidovi, vedoucímu provozu ve farmaceutickém závodě v Dubaji, vyřešit problémy s validací ETO sterilizace u jejich systémů odvětrávání bioreaktorů. Jejich standardní odvzdušňovací zátky absorbovaly ETO a vyžadovaly prodloužené 14denní periody provzdušňování, které narušovaly výrobní harmonogramy. Zavedením našich odvzdušňovacích zátek z PTFE kompatibilních s ETO s minimálními absorpčními vlastnostmi zkrátili dobu provzdušňování na 24 hodin při zachování plného zajištění sterility - což výrazně zlepšilo efektivitu výroby! 🚀
Které materiály jsou nejlepší pro sterilizaci v autoklávu?
Výběr vhodných materiálů pro sterilizaci v autoklávu vyžaduje znalost tepelné stability, odolnosti vůči hydrolýze a dlouhodobé výkonnosti při opakovaném vystavení páře.
PTFE (polytetrafluorethylen) nabízí vynikající výkon v autoklávu s trvalou provozní teplotou až 260 °C, vynikající chemickou inertnost a odolnost proti hydrolýze. PVDF (polyvinylidenfluorid) poskytuje dobrou tepelnou stabilitu do 150 °C při nižších nákladech. Vyhněte se nylonu, standardnímu polyethylenu a většině elastomerů, které v podmínkách autoklávu degradují a zhoršují filtrační a těsnicí vlastnosti.
Výhody PTFE membrán
Výjimečná teplotní odolnost: PTFE si zachovává strukturální integritu a filtrační výkon při teplotách výrazně vyšších, než jsou běžné podmínky autoklávování (121-134 °C).
Chemická inertnost: PTFE je odolný proti degradaci párou, čisticími chemikáliemi a vedlejšími produkty sterilizace, což zajišťuje dlouhodobou stabilitu.
Hydrofobní vlastnosti: Hydrofobní povaha PTFE zabraňuje absorpci vody a udržuje rozměrovou stabilitu během sterilizačních cyklů.
Srovnání výkonnosti materiálů
| Materiál | Maximální teplota (°C) | Odolnost proti páře | Odolnost proti hydrolýze | Nákladový faktor |
|---|---|---|---|---|
| PTFE | 260 | Vynikající | Vynikající | Vysoká |
| PVDF | 150 | Dobrý | Dobrý | Střední |
| PP (polypropylen) | 135 | Spravedlivé | Spravedlivé | Nízká |
| Nylon | 80-100 | Špatný | Špatný | Nízká |
Výběr materiálu pouzdra
Nerezová ocel 316L: Poskytuje vynikající odolnost proti korozi, tepelnou stabilitu a čistitelnost pro farmaceutické a lékařské aplikace vyžadující ověřené čisticí postupy.
PEEK (polyetheretherketon): Nabízí vynikající tepelnou stabilitu (nepřetržité použití do 250 °C) s vynikající chemickou odolností pro náročné aplikace v autoklávu.
Polypropylen: Cenově výhodná varianta pro aplikace na jedno použití s dostatečným výkonem pro standardní autoklávovací cykly při 121 °C.
Úvahy o těsnicí součásti
O-kroužky EPDM: Poskytují dobrou odolnost proti vodní páře a tepelnou stabilitu při teplotách do 150 °C s vynikající těsnicí schopností.
Silikonová těsnění: Nabízejí vyšší teplotní odolnost (až 200 °C), ale mohou mít problémy s kompatibilitou s některými čisticími prostředky.
O-kroužky zapouzdřené PTFE: Kombinace chemické odolnosti PTFE s těsnicími vlastnostmi elastomeru pro náročné aplikace vyžadující obě výkonnostní charakteristiky.
Optimalizace konstrukce pro použití v autoklávu
Tepelná roztažnost Ubytování: Konstrukce odvzdušnění musí zohledňovat rozdílnou tepelnou roztažnost materiálů, aby se zabránilo selhání těsnění při teplotních cyklech.
Odvodňovací prvky: Správná konstrukce odvodnění zabraňuje hromadění kondenzátu, které by mohlo ohrozit výkon filtrace nebo způsobit riziko kontaminace.
Podpora validace: Konstrukční prvky by měly usnadnit validační zkoušky včetně testování rozpadu tlaku, mikrobiální zkoušky a ověření tepelného výkonu.
Jaké materiály se nejlépe hodí pro sterilizační procesy ETO?
ETO sterilizace představuje jedinečnou výzvu pro materiály vyžadující chemickou kompatibilitu, minimální absorpci a rychlé odplynění pro efektivní zpracování.
PTFE a PVDF nabízejí vynikající kompatibilitu s ETO s minimální absorpcí chemikálií a rychlým odplyněním. Vyhněte se materiálům s aktivními vodíkovými místy, jako je nylon, PVC a přírodní kaučuk, které reagují s ETO za vzniku toxických sloučenin. Pouzdra z nerezové oceli poskytují optimální chemickou odolnost, zatímco silikonová těsnění nabízejí dobrou kompatibilitu s ETO s přijatelnými charakteristikami odplyňování pro většinu aplikací.
Chemická kompatibilita ETO
Reakční mechanismy: ETO reaguje s materiály obsahujícími hydroxylové, aminové, karboxylové a sulfhydrylové skupiny za vzniku derivátů ethylenglykolu a dalších potenciálně toxických sloučenin.
Absorpční vlastnosti: Materiály s vysokou absorpcí ETO vyžadují delší dobu provzdušňování, což výrazně prodlužuje dobu zpracování a zvyšuje náklady.
Kinetika vypouštění plynů: Rychle odplyňující materiály umožňují kratší provzdušňovací cykly, což zvyšuje efektivitu procesu a zkracuje dobu skladování.
Hodnocení výkonnosti materiálu ETO
Vynikající kompatibilita s ETO:
- PTFE: Minimální absorpce, rychlé odplynění, žádná chemická reaktivita.
- PVDF: Nízká absorpce, dobré odplyňování, vynikající chemická odolnost.
- Nerezová ocel: Nerezová ocel: bez absorpce, možnost okamžitého použití
Dobrá kompatibilita s ETO:
- Polypropylen: Mírná absorpce, přijatelná plynatost.
- Silikon: Nízká reaktivita, mírné požadavky na odplyňování
Špatná kompatibilita s ETO:
- Nylon: Vysoká reaktivita, nutná delší aerace
- PVC: Chemická degradace, tvorba toxických sloučenin
- Přírodní kaučuk: vysoká absorpce, potenciální degradace
Požadavky na dobu provzdušňování
| Materiál | Typická doba provzdušňování | Úroveň absorpce ETO | Míra vypouštění plynů |
|---|---|---|---|
| PTFE | 8-24 hodin | Minimální | Rapid |
| PVDF | 24-48 hodin | Nízká | Dobrý |
| Polypropylen | 48-72 hodin | Mírná | Mírná |
| Nylon | 7-14 dní | Vysoká | Pomalý |
Optimalizace parametrů procesu
Regulace teploty: ETO sterilizace obvykle probíhá při teplotách 37-63 °C, což vyžaduje materiály, které si zachovávají výkonnost v celém tomto teplotním rozsahu.
Požadavky na vlhkost: Účinnost ETO vyžaduje relativní vlhkost 40-80%, což vyžaduje materiály, které za těchto vlhkostních podmínek trvale fungují.
Řízení koncentrace plynu: Koncentrace ETO 450-1200 mg/l vyžadují materiály, které jsou odolné vůči chemickému napadení a zároveň umožňují průnik sterilizačního prostředku.
Úvahy o validaci
Testování reziduí: Výrobky sterilizované ETO vyžadují testování na rezidua ETO a reakční produkty, aby se zajistilo dodržování bezpečnostních limitů.
Údržba biokompatibility: Materiály si musí zachovat biokompatibilitu po expozici ETO a provzdušňování, což vyžaduje validovaný výběr materiálu.
Monitorování procesů: ETO sterilizace vyžaduje nepřetržité monitorování teploty, vlhkosti, tlaku a koncentrace plynu v průběhu celého cyklu.
Jak vybrat a ověřit sterilizovatelné ventilační zátky?
Správný výběr a validace sterilizovatelných ventilačních zátek zajišťuje spolehlivý sterilizační výkon, shodu s předpisy a dlouhodobý provozní úspěch.
Výběr vyžaduje přizpůsobení vlastností materiálu metodě sterilizace, definování požadavků na výkon a zohlednění regulačních norem. Validace zahrnuje testování tepelného výkonu, mikrobiální studie, hodnocení chemické kompatibility a hodnocení dlouhodobé stability. Zdokumentujte veškeré testování podle norem FDA a ISO pro účely předložení regulačním orgánům a shody se systémem kvality.
Rámec výběrových kritérií
Kompatibilita sterilizačních metod: Přizpůsobte ventilační materiály konkrétním metodám sterilizace (pára, ETO, H2O2 plazma, gama) na základě požadavků na teplotu, chemickou odolnost a odolnost vůči záření.
Specifikace výkonu: Definujte požadované průtoky, jmenovité tlaky, filtrační účinnost a mikrobiální bariéry na základě požadavků aplikace.
Regulační požadavky: Zvažte klasifikaci zařízení podle FDA, shodu s normami ISO a požadavky na biokompatibilitu pro zamýšlené použití.
Parametry hodnocení aplikace
Provozní prostředí: Zhodnoťte teplotní rozsahy, vystavení chemickým látkám, tlakové podmínky a rizika kontaminace v průběhu celého životního cyklu výrobku.
Frekvence sterilizace: Zvažte jednorázové použití oproti vícenásobným sterilizačním cyklům a kumulativní účinky na výkonnost a spolehlivost materiálu.
Rozsah validace: Určete požadavky na testování na základě posouzení rizik, regulační cesty a požadavků na systém kvality.
Protokol o validačním testování
Zkoušky tepelného výkonu:
- Teplotní cyklování při sterilizačních podmínkách
- Měření rozměrové stability
- Ověření účinnosti filtrace po tepelné expozici
Testování mikrobiální výzvy:
- Bakteriální výzva s vhodnými testovacími organismy
- Ověřování udržování sterility
- Dlouhodobé hodnocení integrity bariér
Posouzení chemické kompatibility:
- Hodnocení degradace materiálu
- Testování extrahovatelných a vyluhovatelných látek
- Ověřování údržby biokompatibility
Požadavky na dokumentaci
Specifikace materiálu: Kompletní materiálové listy včetně chemického složení, tepelných vlastností a regulačních certifikátů.
Testovací protokoly: Podrobné validační protokoly podle pokynů FDA a norem ISO pro validaci sterilizace.
Údaje o výkonu: Komplexní výsledky testů prokazující výkonnost za stanovených provozních podmínek a sterilizačních cyklů.
Integrace systému kvality
Kvalifikace dodavatele: Vypracování dohod o kvalitě s dodavateli, včetně požadavků na sledovatelnost materiálu, řízení změn a dokumentaci kvality.
Příchozí kontrola: Vypracování kontrolních postupů pro ověřování kritických rozměrů, vlastností materiálu a výkonnostních charakteristik.
Validace procesu: Začlenit výkonnost ventilace do celkové validace sterilizačního procesu včetně testování nejhoršího scénáře.
Úvahy o řízení rizik
Analýza způsobů selhání: Identifikujte potenciální způsoby selhání, včetně degradace materiálu, selhání těsnění a ohrožení filtrace, s vhodnými strategiemi zmírnění.
Řízení změn: Zavedení postupů pro řízení změn materiálu, změn dodavatele a změn specifikací s příslušnými požadavky na revalidaci.
Průběžné monitorování: Zavedení průběžných monitorovacích programů k ověření trvalého výkonu a identifikaci potenciálních problémů dříve, než ovlivní kvalitu výrobku.
Závěr
Sterilizovatelné ventilační zátky hrají klíčovou roli při zajišťování účinné sterilizace při zachování sterilních bariér ve zdravotnických prostředcích a farmaceutických aplikacích. Pochopení jedinečných problémů různých sterilizačních metod a výběr vhodných materiálů je zásadní pro spolehlivý výkon a dodržování předpisů.
Odvzdušňovací zátky na bázi PTFE mají vynikající výkon při různých metodách sterilizace, poskytují vynikající teplotní odolnost, chemickou kompatibilitu a dlouhodobou spolehlivost. Správný výběr a validace zajišťují optimální účinnost sterilizace a zároveň minimalizují dobu zpracování a náklady.
Naše ucelená řada sterilizovatelných ventilačních zátek Bepto zahrnuje membrány z PTFE farmaceutické kvality, validované teplotní parametry a kompletní dokumentační balíčky pro předložení regulačním orgánům. Díky více než desetiletým zkušenostem se specializovanými ventilačními aplikacemi a výrobním kapacitám s certifikací ISO poskytujeme spolehlivá a nákladově efektivní řešení, která potřebujete pro kritické sterilizační aplikace. Důvěřujte nám, že vaše sterilizační procesy budou validované a vaše výrobky bezpečné! 🔬
Časté dotazy týkající se sterilizovatelných ventilačních zátek
Otázka: Lze použít stejnou odvzdušňovací zátku pro sterilizaci v autoklávu i ETO?
A: Ano, membránové ventilační zátky z PTFE lze účinně sterilizovat v autoklávu i v ETO. PTFE nabízí vynikající teplotní odolnost pro autoklávové cykly a minimální absorpci ETO pro rychlé odvzdušnění, takže je ideální pro zařízení používající více metod sterilizace.
Otázka: Kolik sterilizačních cyklů vydrží ventilační zátka?
A: Vysoce kvalitní PTFE ventilační zátky obvykle vydrží více než 100 cyklů v autoklávu nebo více než 50 cyklů ETO při zachování filtračního výkonu. Skutečná životnost cyklu závisí na parametrech sterilizace, manipulačních postupech a kritériích přijatelnosti výkonu pro konkrétní aplikaci.
Otázka: Jaká velikost pórů je vyžadována pro sterilní filtraci v lékařských aplikacích?
A: Zdravotnické aplikace obvykle vyžadují velikost pórů 0,2 nebo 0,22 mikronu pro spolehlivé zadržení bakterií. Tato velikost pórů zajišťuje ověřenou sterilitu a zároveň umožňuje dostatečný průtok plynu pro účinnou sterilizaci a vyrovnání tlaku.
Otázka: Vyžadují sterilizovatelné ventilační zátky speciální validační testy?
A: Ano, sterilizovatelné ventilační zátky vyžadují validační testování, včetně testů tepelné výkonnosti, mikrobiální odolnosti a kompatibility materiálů. Testování se musí řídit pokyny FDA a normami ISO, přičemž je třeba doložit dokumentaci podporující validaci vašeho sterilizačního procesu a předložit ji regulačním orgánům.
Otázka: Jak zabráníte kontaminaci ventilační zátky během sterilizace?
A: Zabraňte kontaminaci správnou instalací, ochrannými kryty při manipulaci, ověřenými parametry sterilizace a vhodným skladováním po sterilizaci. Při instalaci používejte sterilní techniku a zajistěte, aby byly ventilační zátky navrženy pro konkrétní metodu sterilizace a požadavky na použití.
-
Seznamte se s vědeckými principy sterilizace v autoklávu a s tím, jak se nasycená pára pod tlakem používá k účinné likvidaci mikroorganismů. ↩
-
Prozkoumejte chemický proces sterilizace ethylenoxidem (ETO), nízkoteplotní metodu používanou ke sterilizaci zdravotnických prostředků citlivých na teplo a vlhkost. ↩
-
Seznamte se s metodami používanými k testování a ověřování účinnosti mikrobiální bariéry, které zajišťují, že bariéra zabraňuje vniknutí mikroorganismů a udržuje sterilitu. ↩
-
Přečtěte si klíčové požadavky normy ISO 11607, která specifikuje materiály a zkoušky sterilních bariérových systémů pro zdravotnické prostředky. ↩
-
Porozumět chemické reakci hydrolýzy a tomu, jak může způsobit degradaci některých polymerních materiálů, jsou-li vystaveny působení vody nebo páry při vysokých teplotách. ↩



