Nesprávný výběr kabelových vývodek v lékařském prostředí a v čistých prostorách způsobuje rizika kontaminace, nedodržení předpisů a poruchy zařízení, které mají za následek ohrožení bezpečnosti pacientů, nákladné odstávky zařízení a porušení předpisů FDA, zatímco nedostatečné utěsnění, nevhodné materiály a špatná čistitelnost vedou k růstu bakterií, kontaminaci částicemi a porušení sterility, které ohrožují kritické zdravotnické operace. Mnoho manažerů zařízení se potýká s výběrem vývodek, které splňují přísné lékařské normy a zároveň zachovávají spolehlivý elektrický výkon.
Výběr kabelových vývodek pro zdravotnické vybavení a čisté prostory vyžaduje znalost předpisů FDA, USP třída VI1 požadavky na materiál, normy těsnění IP68+ a požadavky na klasifikaci čistých prostor, přičemž konstrukce z lékařské nerezové oceli nebo specializovaného polymeru zajišťuje biokompatibilitu, chemickou odolnost a hladký povrch pro účinné čištění a sterilizaci při zachování elektrické integrity v kritických zdravotnických aplikacích. Úspěch závisí na rovnováze mezi dodržováním právních předpisů a provozní spolehlivostí.
Po spolupráci s nemocničními inženýry ve velkých lékařských centrech v Bostonu, farmaceutickými výrobci ve Švýcarsku a zařízeními s čistými prostory v Singapuru jsem zjistil, že kabelové vývodky pro lékařské účely jsou nezbytné pro zachování sterilního prostředí a zajištění bezpečnosti pacientů. Dovolte mi podělit se s vámi o důležité poznatky pro výběr optimálních vývodek pro vaše lékařské aplikace a aplikace v čistých prostorách.
Obsah
- Čím se liší lékařské kabelové vývodky od standardních vývodek?
- Jak splnit předpisy FDA a předpisy pro zdravotnické prostředky?
- Jaké materiály jsou nutné pro aplikace v čistých prostorách?
- Jak zajistíte správné čištění a sterilizační kompatibilitu?
- Jaká jsou klíčová kritéria výběru pro různé lékařské aplikace?
- Časté dotazy týkající se lékařských kabelových vývodek
Čím se liší lékařské kabelové vývodky od standardních vývodek?
Zdravotnické kabelové vývodky se od standardních vývodek liší použitím biokompatibilních materiálů, hladkým čistitelným povrchem, splněním předpisů FDA, zvýšenou těsností pro prevenci kontaminace, chemickou odolností vůči čisticím prostředkům a sterilizačním procesům a specializovaným provedením, které eliminuje štěrbiny, v nichž by se mohly uchytit bakterie, při zachování elektrického výkonu v kritických zdravotnických prostředích.
Pochopení těchto rozdílů je zásadní, protože lékařské aplikace mají jedinečné bezpečnostní a regulační požadavky, které standardní průmyslové vývodky nemohou dostatečně splnit.
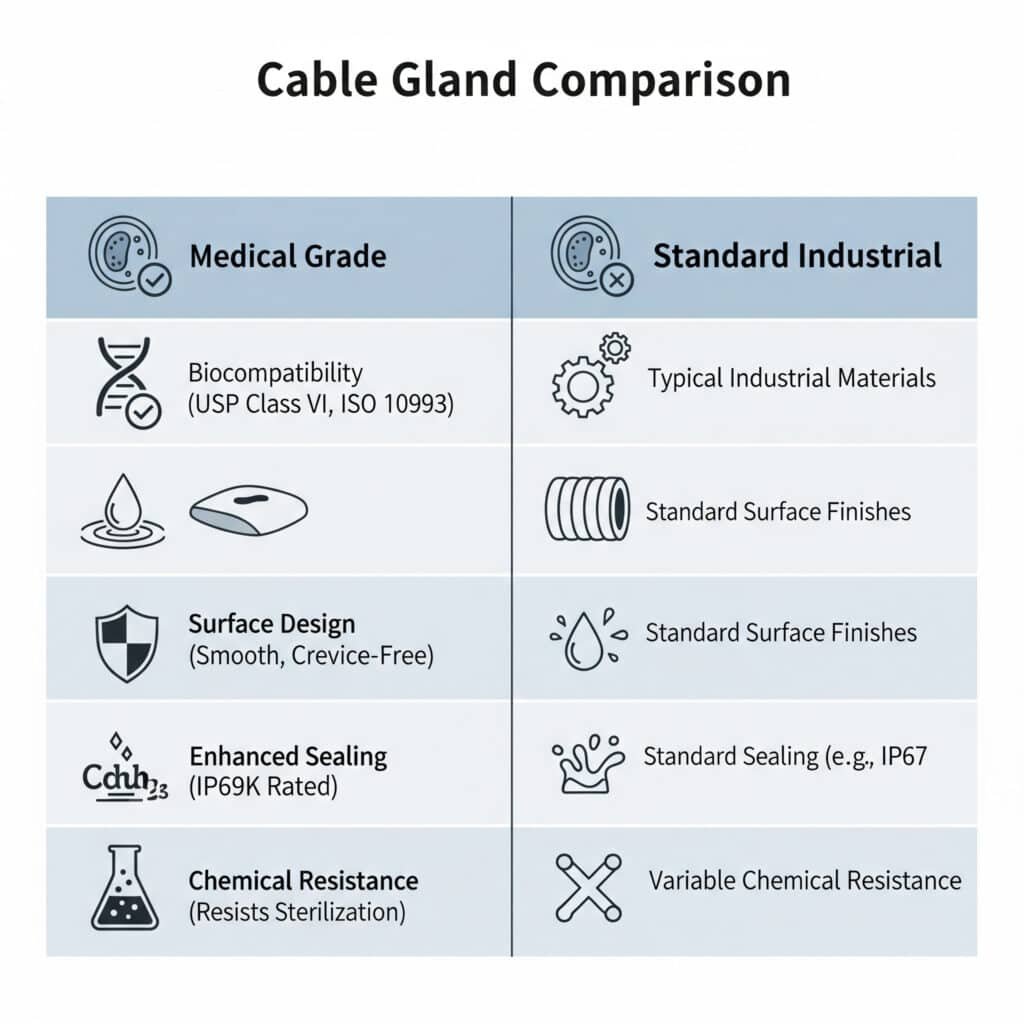
Požadavky na biokompatibilitu
Shoda s USP třídy VI: Zdravotnické kabelové vývodky musí používat materiály, které prošly biologickým testováním třídy VI podle amerického lékopisu pro biokompatibilitu a bezpečnost při použití ve zdravotnických prostředcích.
Normy ISO 10993: Materiály musí splňovat ISO 109932 normy biologického hodnocení zdravotnických prostředků, které zajišťují, že nemají cytotoxické, senzibilizující nebo dráždivé účinky na lidskou tkáň.
Schválení FDA 21 CFR 177: Pro farmaceutické aplikace a aplikace zdravotnických prostředků jsou často vyžadovány materiály potravinářské kvality, které splňují předpisy FDA pro přímý a nepřímý styk s potravinami.
Biokompatibilní polymery: Specializované materiály, jako je PEEK, PTFE nebo nylon farmaceutické kvality, zajišťují biokompatibilitu bez zhoršení mechanických vlastností.
Konstrukce povrchu pro čistitelnost
Hladká povrchová úprava: Zdravotnické vývodky mají velmi hladký povrch s hodnotami Ra obvykle pod 0,8 mikrometru, který zabraňuje ulpívání bakterií a umožňuje účinné čištění.
Design bez trhlin: Eliminace ostrých rohů, hlubokých závitů a složitých geometrických tvarů, které by mohly být zdrojem bakterií nebo odolávat čisticím a sterilizačním procesům.
Zaoblené hrany: Všechny vnější povrchy mají zaoblené hrany a hladké přechody, které usnadňují čištění a zabraňují poškození rukavic pro čisté prostory nebo sterilních obalů.
Minimální plocha: Zjednodušená konstrukce minimalizuje plochu vystavenou kontaminaci při zachování potřebného mechanického a elektrického výkonu.
Vylepšený těsnicí výkon
Hodnocení IP68+: Vyšší ochrana před vlivy prostředí než standardní IP68, často dosahující IP69K pro vysokotlaké čisticí aplikace při vysokých teplotách.
Kontaminační bariéry: Více těsnicích stupňů zabraňuje vniknutí částic, bakterií a čisticích chemikálií, které by mohly ohrozit sterilní prostředí.
Odolnost proti tlaku: Vyšší tlakové třídy, které odolávají agresivním čisticím postupům a sterilizačním procesům, aniž by došlo k selhání těsnění.
Dlouhodobá spolehlivost: Těsnicí materiály si zachovávají celistvost i při opakovaných sterilizačních cyklech a působení drsných čisticích chemikálií.
Vlastnosti chemické odolnosti
Kompatibilita s čisticími prostředky: Odolnost vůči nemocničním dezinfekčním prostředkům, kvartérním amoniovým sloučeninám, peroxidu vodíku a dalším agresivním čisticím chemikáliím.
Odolnost vůči sterilizaci: Materiály odolávají gama záření, ethylenoxidu, parní autoklávování a dalším metodám sterilizace bez degradace.
Farmaceutické chemikálie: Odolnost vůči rozpouštědlům, kyselinám, zásadám a farmaceutickým sloučeninám, které se běžně vyskytují v prostředí lékařské výroby.
Teplotní stabilita: Zachování vlastností při sterilizačních teplotních cyklech a požadavcích na kontrolu teploty v čistých prostorách.
David, manažer zařízení ve velkém farmaceutickém závodě v New Jersey, čelil opakovaným problémům s kontaminací sterilních plnicích linek, kde se navzdory přísným čisticím protokolům ve standardních kabelových vývodkách vyskytovaly bakterie. Stávající mosazné vývodky měly složité vzory závitů a povrchové úpravy, které nebylo možné adekvátně sterilizovat, což vedlo k vyřazování šarží a obavám o shodu s předpisy FDA. Specifikovali jsme kabelové vývodky z lékařské nerezové oceli s elektrolyticky leštěným povrchem a bez trhlin, které splňovaly požadavky USP třídy VI. Modernizace odstranila zdroje kontaminace, dosáhla účinnosti čištění 99,9% a pomohla zařízení projít kontrolami FDA při současném snížení počtu vyřazených výrobků o 85% 😊.
Jak splnit předpisy FDA a předpisy pro zdravotnické prostředky?
Dodržování předpisů FDA a zdravotnických prostředků vyžaduje používání materiálů s příslušnými certifikacemi, vedení podrobné dokumentace, dodržování předpisů FDA a zdravotnických prostředků. Správná výrobní praxe (GMP)3, zajištění sledovatelnosti a zavedení systémů kvality, které jsou v souladu s 21 CFR Part 820, přičemž lékařské kabelové vývodky vyžadují materiály schválené FDA, testování biokompatibility a výrobní kontroly, které zajišťují konzistentní kvalitu a bezpečnost při použití ve zdravotnických prostředcích.
Dodržování předpisů je v lékařských aplikacích neoddiskutovatelné, protože selhání může mít za následek poškození pacienta, stažení výrobku z trhu a závažné právní důsledky.
Požadavky na materiály FDA
21 CFR část 177: Materiály, které přicházejí do styku s léčivy nebo zdravotnickými prostředky, musí splňovat předpisy FDA týkající se potravinářských přísad pro látky přicházející do nepřímého styku s potravinami.
Hlavní přístupový soubor (MAF): Dodavatelé musí vést hlavní přístupové soubory FDA dokumentující bezpečnost materiálu, výrobní procesy a postupy kontroly kvality.
Základní soubor údajů o léčivém přípravku (DMF): U farmaceutických aplikací mohou materiály vyžadovat registraci základního souboru léčiv s podrobnými informacemi o složení a výrobě.
Osvědčení o shodě: Dodavatelé musí předložit certifikáty potvrzující, že materiály splňují všechny platné předpisy a specifikace FDA.
Normy kvality zdravotnických prostředků
Shoda s normou ISO 13485: Při výrobě musí být dodržovány systémy řízení kvality zdravotnických prostředků podle normy ISO 13485 pro návrh, výrobu a dohled po uvedení na trh.
21 CFR část 820 (QSR): Dodržování předpisů o systému jakosti zajišťující správné kontroly návrhu, kontrolu dokumentů a nápravná/preventivní opatření.
Řízení rizik: Procesy řízení rizik pro zdravotnické prostředky podle normy ISO 14971, včetně analýzy, hodnocení a kontrolních opatření.
Kontrola designu: Formální procesy kontroly návrhu včetně plánování návrhu, vstupních/výstupních požadavků, revizí, ověřování a validace.

Dokumentace a sledovatelnost
Certifikáty materiálu: Úplná sledovatelnost materiálu s certifikáty analýzy, výsledky testů biokompatibility a dokumentací o souladu s předpisy.
Výrobní záznamy: Podrobné výrobní záznamy včetně parametrů procesu, testů kontroly kvality a dokumentace šarží pro úplnou sledovatelnost.
Řízení změn: Formální postupy řízení změn pro všechny úpravy materiálů, procesů nebo specifikací, které mají vliv na dodržování předpisů.
Kvalifikace dodavatele: Komplexní programy kvalifikace dodavatelů zajišťující, že všechny materiály a součásti splňují požadavky na zdravotnické prostředky.
Požadavky na validaci
Testování biokompatibility: Testování USP třídy VI včetně systémových injekčních, intrakutánních a implantačních testů k ověření biologické bezpečnosti.
Validace čištění: Zdokumentované postupy čištění s validačními údaji prokazujícími účinné odstranění kontaminantů a snížení biologické zátěže.
Ověřování sterilizace: Validace sterilizačních procesů včetně mapování dávek, úrovní zajištění sterility a studií kompatibility materiálů.
Testování výkonu: Elektrické, mechanické a environmentální zkoušky k ověření, zda výkon splňuje požadavky na zdravotnické prostředky po celou dobu životnosti výrobku.
Podpora při předkládání regulačních žádostí
Dokumentace 510(k): Technická dokumentace podporující podání FDA 510(k) pro zdravotnické prostředky obsahující kabelové vývodky.
Technické soubory: Komplexní technická dokumentace pro označení CE podle nařízení o zdravotnických prostředcích (MDR) na evropských trzích.
Dohody o kvalitě: Formální dohody o kvalitě s dodavateli definující odpovědnosti, specifikace a požadavky na shodu.
Podpora auditu: Podpora při auditech FDA, notifikovaných osob a zákazníků, včetně kontroly dokumentace a inspekcí zařízení.
Jaké materiály jsou nutné pro aplikace v čistých prostorách?
Aplikace v čistých prostorech vyžadují materiály s nízkou úrovní odplyňování, odolností proti tvorbě částic, chemickou kompatibilitou s čisticími prostředky, hladkými neporézními povrchy a vhodnou úrovní vodivosti, přičemž nerezová ocel 316L, PEEK, PTFE a specializované polymery schválené pro čisté prostory poskytují optimální výkon a zároveň splňují požadavky na ISO 146444 normy pro čisté prostory a zachování elektrické integrity v kontrolovaných prostředích.
Výběr materiálu je velmi důležitý, protože čisté prostory vyžadují přísnou kontrolu kontaminace částicemi a molekulární kontaminace, která by mohla ohrozit kvalitu výrobku nebo sterilní podmínky.
Požadavky na nerezovou ocel
Lékařská třída 316L: Austenitická nerezová ocel s nízkým obsahem uhlíku zajišťující vynikající odolnost proti korozi a biokompatibilitu pro lékařské aplikace.
Elektricky leštěná povrchová úprava: Elektrolytické leštění odstraňuje nedokonalosti povrchu, snižuje tvorbu částic a vytváří hladký povrch pro účinné čištění.
Pasivační ošetření: Chemická pasivace zvyšuje odolnost proti korozi a odstraňuje znečištění železem, které by mohlo způsobit změnu barvy nebo tvorbu částic.
Drsnost povrchu: Hodnoty Ra nižší než 0,8 mikrometru (32 mikroinchů) minimalizují přilnavost bakterií a usnadňují procesy čištění a sterilizace.
Vysoce výkonné polymery
PEEK (polyetheretherketon): Díky vynikající chemické odolnosti, nízkému odplyňování a biokompatibilitě je PEEK ideální pro použití ve farmaceutickém průmyslu a zdravotnických zařízeních.
PTFE (polytetrafluorethylen): Vynikající chemická inertnost a nepřilnavost zajišťují vynikající odolnost vůči čisticím chemikáliím a biologickým materiálům.
Lékařské nylony: Nylony se speciálním složením a schválením USP Class VI nabízejí dobré mechanické vlastnosti a biokompatibilitu pro lékařské aplikace.
POM schválený pro čisté prostory: Polyoxymethylen s nízkou tvorbou částic a dobrou rozměrovou stabilitou pro přesné aplikace v čistých prostorách.
Kompatibilita s klasifikací čistých prostor
Třída ISO 5 (třída 100): Ultrahladké povrchy s minimální tvorbou částic pro aplikace v polovodičové a farmaceutické výrobě.
Třída ISO 6 (třída 1000): Mírná kontrola částic pro výrobu zdravotnických prostředků a některé farmaceutické procesy.
Třída ISO 7 (třída 10000): Standardní požadavky na čisté prostory pro všeobecné farmaceutické operace a montáže zdravotnických prostředků.
Třída ISO 8 (třída 100000): Základní požadavky na čisté prostory pro balení a některé výrobní procesy zdravotnických prostředků.
Kontrola výparů a kontaminace
Materiály s nízkým obsahem plynů: Materiály s minimálními emisemi těkavých organických látek (VOC), které by mohly kontaminovat citlivé procesy nebo výrobky.
Molekulární kontaminace: Kontrola molekulárních kontaminantů včetně silikonů, změkčovadel a dalších organických sloučenin, které by mohly ovlivnit kvalitu výrobku.
Iontová kontaminace: Materiály s nízkým obsahem iontů, které zabraňují kontaminaci elektronických součástek a farmaceutických výrobků.
Extrahovatelné látky: Minimální množství extrahovatelných látek, které by se mohly během používání vyluhovat do farmaceutických výrobků nebo čisticích roztoků.
Matice chemické kompatibility
| Čisticí prostředek | 316L SS | PEEK | PTFE | Lékařský nylon |
|---|---|---|---|---|
| Izopropylalkohol | Vynikající | Vynikající | Vynikající | Dobrý |
| Peroxid vodíku | Vynikající | Vynikající | Vynikající | Spravedlivé |
| Čtvrtohorní amonium | Vynikající | Vynikající | Vynikající | Dobrý |
| Chlornan sodný | Dobrý | Vynikající | Vynikající | Špatný |
| Kyselina peroctová | Dobrý | Vynikající | Vynikající | Špatný |
Hassan, který řídí provoz v nejmodernějším farmaceutickém závodě ve Švýcarsku, potřeboval modernizovat kabelové vývodky v čistém prostoru třídy 5 ISO pro výrobu sterilních injekcí. Stávající vývodky vytvářely při čisticích cyklech částice a nevydržely agresivní sterilizační protokoly vyžadované pro jejich nové biologické produkty. Dodali jsme elektrolyticky leštěné kabelové vývodky z nerezové oceli 316L s ověřenou nízkou tvorbou částic a naprostou chemickou kompatibilitou s jejich čisticími a sterilizačními procesy. Modernizace dosáhla počtu částic 90% pod limity ISO třídy 5, eliminovala případy kontaminace související s čištěním a podpořila úspěšnou validaci jejich nové sterilní výrobní linky.
Jak zajistíte správné čištění a sterilizační kompatibilitu?
Zajištění správného čištění a kompatibility se sterilizací vyžaduje výběr materiálů, které odolávají opakovanému vystavení čisticím chemikáliím a sterilizačním metodám, navrhování povrchů pro úplnou čistitelnost, ověřování čisticích postupů a vedení podrobné dokumentace, přičemž lékařské kabelové vývodky vyžadují hladké povrchy bez trhlin, materiály odolné vůči chemikáliím a ověřené čisticí protokoly, které dosahují požadované úrovně zajištění sterility.
Kompatibilita čištění a sterilizace je zásadní, protože nedostatečná dekontaminace může vést ke kontaminaci výrobků, ohrožení bezpečnosti pacientů a porušení předpisů.
Kompatibilita sterilizačních metod
Parní autoklávování: Materiály musí odolávat teplotám 121-134 °C parní autoklávování5 cyklů, aniž by došlo k degradaci, změně rozměrů nebo selhání těsnění.
Záření gama: Odolnost vůči dávkám gama záření 25-50 kGy běžně používaným pro sterilizaci zdravotnických prostředků bez degradace materiálu.
Oxid ethylnatý (EtO): Chemická kompatibilita se sterilizací EtO včetně odolnosti vůči sterilizačnímu činidlu a správných odplyňovacích vlastností.
Plazma s peroxidem vodíku: Kompatibilita s nízkoteplotními plazmovými sterilizačními systémy včetně stability materiálu a úplné penetrace sterilizačního prostředku.
Požadavky na validaci čištění
Postupy čištění: zdokumentované postupy čištění s uvedením chemických látek, koncentrací, doby kontaktu a mechanického působení, které jsou nezbytné pro účinnou dekontaminaci.
Validační protokoly: Formální validační studie prokazující účinnost čištění pomocí nejhorších scénářů kontaminace a analytických testů.
Kritéria přijatelnosti: Definovaná kritéria přijatelnosti pro čistotu, včetně vizuální kontroly, počtu částic, úrovně biologické zátěže a limitů chemických reziduí.
Rutinní monitorování: Průběžné monitorovací programy k ověření trvalé účinnosti čištění a zjištění případného zhoršení výkonu.
Úvahy o návrhu povrchu
Odvodňovací prvky: Konstrukční prvky, které podporují úplný odtok čisticích roztoků a zabraňují hromadění nečistot.
Přístupnost: Všechny povrchy musí být přístupné pro čištění standardními čisticími nástroji a postupy používanými ve zdravotnických zařízeních.
Požadavky na demontáž: Zvažte, zda je nutné vývodky pro čištění demontovat, nebo zda pro danou aplikaci postačí čištění vcelku.
Výměna těsnění: Postupy pro výměnu těsnění a validaci, pokud těsnicí součásti vyžadují pravidelnou výměnu z důvodu vystavení čisticí chemikálii.
Dokumentace a dodržování předpisů
Pokyny k čištění: Podrobné pokyny k čištění včetně postupů krok za krokem, specifikací chemikálií a bezpečnostních opatření.
Bezpečnostní údaje o materiálu: Kompletní informace o bezpečnosti materiálu včetně chemické kompatibility, teplotních limitů a kompatibility při sterilizaci.
Validační zprávy: Validační zprávy o čištění prokazující účinnost a stanovení požadavků na běžné monitorování.
Školící materiály: Školící materiály pro personál zařízení o správném čištění, manipulaci a údržbě zdravotnických kabelových vývodek.
Testování kontroly kvality
Testování biologické zátěže: Pravidelné testování mikrobiální kontaminace pro ověření účinnosti čištění a identifikaci potenciálních problémových oblastí.
Testování endotoxinů: Testování na přítomnost bakteriálních endotoxinů, které by mohly způsobit pyrogenní reakce ve farmaceutickém průmyslu a zdravotnických prostředcích.
Počítání částic: Testování počtu částic k ověření, zda jsou po čištění a údržbě dodrženy požadavky na čisté prostory.
Analýza chemických zbytků: Testování na zbytky čisticích chemikálií, které by mohly kontaminovat výrobky nebo ovlivnit biokompatibilitu.
Jaká jsou klíčová kritéria výběru pro různé lékařské aplikace?
Klíčová kritéria výběru se liší v závislosti na aplikaci, ale zahrnují požadavky na shodu s předpisy, úrovně biokompatibility, klasifikace čistých prostor, metody sterilizace, vystavení chemickým látkám a požadavky na elektrický výkon, přičemž chirurgická zařízení vyžadují nejvyšší biokompatibilitu, farmaceutická výroba vyžaduje chemickou odolnost a diagnostická zařízení se zaměřují na elektrickou integritu, zatímco všechny aplikace vyžadují příslušné certifikace podle předpisů a kompatibilitu s čištěním.
Různé lékařské aplikace mají jedinečné požadavky, které je třeba při výběru kabelových vývodek pečlivě zvážit, aby byl zajištěn optimální výkon a shoda s předpisy.
Chirurgické vybavení a vybavení pro kontakt s pacientem
Požadavky na přímý kontakt: Biokompatibilita třídy VI podle USP s dodatečným testováním cytotoxicity pro materiály, které přicházejí do přímého kontaktu s pacientem během chirurgických zákroků.
Frekvence sterilizace: Schopnost odolávat častým sterilizačním cyklům bez degradace, což obvykle vyžaduje materiály stabilní po stovky sterilizačních cyklů.
Elektrická bezpečnost: Zvýšené požadavky na elektrickou bezpečnost včetně nízkého unikajícího proudu a spolehlivé izolace pro zařízení připojená k pacientovi.
Nouzová spolehlivost: Kritické požadavky na spolehlivost u zařízení pro podporu života a zdravotnického vybavení pro urgentní případy, jejichž selhání by mohlo mít přímý dopad na bezpečnost pacientů.
Farmaceutická výroba
Dodržování GMP: Požadavky na správnou výrobní praxi včetně sledovatelnosti materiálu, řízení změn a validační dokumentace.
Bezpečnost při kontaktu s výrobkem: Materiály, které nekontaminují farmaceutické výrobky vyluhováním, tvorbou částic nebo chemickou interakcí.
Validace čištění: Rozsáhlé požadavky na validaci čištění s dokumentovanými postupy a kritérii přijatelnosti pro farmaceutickou výrobu.
Dávková dokumentace: Kompletní dokumentace šarží a sledovatelnost materiálů používaných ve farmaceutických výrobních zařízeních.
Diagnostické a laboratorní vybavení
Požadavky na přesnost: Rozměrová stabilita a přesnost pro analytické přístroje vyžadující konzistentní mechanický a elektrický výkon.
Chemická odolnost: Odolnost vůči laboratorním chemikáliím, činidlům a čisticím rozpouštědlům běžně používaným v diagnostických aplikacích.
Výkon EMC: Požadavky na elektromagnetickou kompatibilitu citlivých analytických přístrojů a diagnostických zařízení.
Stabilita kalibrace: Mechanická stabilita, která v průběhu času neovlivní kalibraci přístroje ani přesnost měření.
Výroba zdravotnických prostředků
Validace procesu: Materiály a součásti, které podporují požadavky na validaci procesů při výrobě zdravotnických prostředků.
Systémy kvality: Integrace se systémy kvality ISO 13485 včetně postupů kvalifikace dodavatelů a vstupní kontroly.
Řízení rizik: Materiály, které podporují požadavky na řízení rizik zdravotnických prostředků, včetně analýzy způsobů selhání a strategií zmírnění.
Regulační podpora: Dodavatelská podpora při předkládání regulačních žádostí včetně technické dokumentace a regulačních odborných znalostí.
Matice pro rozhodování o výběru
| Typ aplikace | Primární kritéria | Sekundární kritéria | Kritické normy |
|---|---|---|---|
| Chirurgické vybavení | Biokompatibilita | Sterilizace | USP třída VI, ISO 10993 |
| Farmaceutické | Chemická odolnost | Dodržování zásad GMP | FDA 21 CFR, cGMP |
| Diagnostika | Přesnost | Výkon EMC | IEC 61326, ISO 15189 |
| Výroba | Ověřování procesů | Systémy kvality | ISO 13485, 21 CFR 820 |
Analýza nákladů a přínosů
Počáteční náklady vs. životní cyklus: Zvažte celkové náklady na vlastnictví včetně nákladů na údržbu, výměnu a dodržování předpisů po celou dobu životnosti zařízení.
Regulační riziko: Vyvážit materiální náklady a rizika dodržování předpisů a potenciální náklady v případě nedodržení předpisů.
Požadavky na výkon: Zajistěte, aby vybrané materiály splňovaly minimální požadavky na výkon bez nadměrných specifikací, které zbytečně zvyšují náklady.
Schopnosti dodavatele: Zhodnoťte schopnosti dodavatelů v oblasti průběžné podpory, dokumentace a pomoci při dodržování předpisů.
Závěr
Výběr kabelových vývodek pro zdravotnická zařízení a čisté prostory vyžaduje pochopení jedinečných regulačních, materiálových a výkonnostních požadavků, které tyto aplikace odlišují od standardního průmyslového použití. Úspěch závisí na vyvážení biokompatibility, čistitelnosti, souladu s předpisy a elektrického výkonu.
Klíčem ke spolehlivému fungování lékařských kabelových vývodek je spolupráce s dodavateli, kteří rozumějí předpisům pro zdravotnické prostředky a mohou poskytnout vhodné materiály, dokumentaci a průběžnou podporu po celou dobu životnosti výrobku. Ve společnosti Bepto se specializujeme na kabelové vývodky pro lékařské účely, které splňují požadavky FDA a mezinárodní normy pro zdravotnické prostředky, a poskytujeme záruku kvality a regulační podporu potřebnou pro kritické aplikace ve zdravotnictví.
Časté dotazy týkající se lékařských kabelových vývodek
Otázka: Jaká osvědčení potřebuji pro lékařské kabelové vývodky?
A: Zdravotnické kabelové vývodky obvykle vyžadují certifikaci biokompatibility USP třídy VI, shodu s FDA 21 CFR pro materiály a výrobní systémy kvality ISO 13485. Konkrétní požadavky závisí na aplikaci a regulační pravomoci.
Otázka: Mohou být běžné kabelové vývodky z nerezové oceli použity ve zdravotnictví?
A: Běžná nerezová ocel nemusí splňovat lékařské požadavky. Zdravotnické aplikace vyžadují nerezovou ocel 316L pro lékařské účely s elektrolyticky leštěnou povrchovou úpravou, testování biokompatibility a řádnou dokumentaci pro dodržení předpisů.
Otázka: Jak čistit a sterilizovat lékařské kabelové vývodky?
A: Dodržujte výrobcem schválené postupy čištění za použití schválených čisticích prostředků a sterilizačních metod. Většina lékařských vývodek podporuje sterilizaci v parním autoklávu, gama záření nebo chemickou sterilizaci při správné kompatibilitě materiálu.
Otázka: Jaký je rozdíl mezi kabelovými vývodkami pro čisté prostory a pro lékařské účely?
A: Lékařská třída zahrnuje požadavky na biokompatibilitu a shodu s FDA, zatímco třída pro čisté prostory se zaměřuje na kontrolu částic a chemickou odolnost. Některé aplikace vyžadují jak lékařské specifikace, tak specifikace pro čisté prostory.
Otázka: Jak často by se měly vyměňovat lékařské kabelové vývodky?
A: Četnost výměny závisí na sterilizačních cyklech, působení chemikálií a doporučeních výrobce. Obvykle se provádí kontrola po každých 100-200 sterilizačních cyklech a výměna na základě posouzení stavu a požadavků na validaci.
-
Seznamte se s konkrétními testy biologické reaktivity, které jsou vyžadovány pro certifikaci USP třídy VI. ↩
-
Získejte přístup k přehledu norem řady ISO 10993 pro biologické hodnocení zdravotnických prostředků. ↩
-
Projděte si oficiální pokyny a předpisy FDA pro současnou správnou výrobní praxi (cGMP). ↩
-
Prozkoumejte podrobného průvodce normami ISO 14644 pro klasifikaci čistoty vzduchu v čistých prostorech. ↩
-
Porozumět principům parní sterilizace, včetně úlohy času, teploty a tlaku. ↩



