Неправилният избор на кабелни уплътнения в медицински и чисти помещения води до рискове от замърсяване, неспазване на нормативната уредба и неизправности в оборудването, които застрашават безопасността на пациентите, водят до скъпоструващи спирания на съоръженията и нарушения на изискванията на FDA, а неадекватното уплътняване, неподходящите материали и лошата почистваща способност водят до бактериален растеж, замърсяване с частици и нарушаване на стерилността, което компрометира критичните операции в здравеопазването. Много мениджъри на обекти се борят с избора на салници, които отговарят на строгите медицински стандарти, като същевременно поддържат надеждна електрическа работа.
Изборът на кабелни втулки за медицинско оборудване и чисти помещения изисква разбиране на разпоредбите на FDA, USP клас VI1 изискванията за материали, стандартите за уплътняване IP68+ и нуждите за класификация на чисти помещения, като конструкцията от медицинска неръждаема стомана или специализиран полимер осигурява биосъвместимост, химическа устойчивост и гладки повърхности за ефективно почистване и стерилизация, като същевременно запазва електрическата цялост в критични приложения в здравеопазването. Успехът зависи от постигането на баланс между спазването на нормативните изисквания и експлоатационната надеждност.
След като работих с инженери от болници в големи медицински центрове в Бостън, фармацевтични производители в Швейцария и съоръжения за чисти помещения в Сингапур, научих, че кабелните уплътнения от медицински клас са от съществено значение за поддържането на стерилна среда и осигуряването на безопасността на пациентите. Позволете ми да споделя важните знания за избора на оптимални кабелни втулки за вашите медицински приложения и приложения за чисти помещения.
Съдържание
- С какво медицинските кабелни уплътнения се различават от стандартните уплътнения?
- Как да спазвате правилата на FDA и на медицинските изделия?
- Какви материали са необходими за приложения в чисти помещения?
- Как да гарантирате правилната съвместимост при почистване и стерилизация?
- Какви са основните критерии за избор на различни медицински приложения?
- Често задавани въпроси за медицинските кабелни втулки
С какво медицинските кабелни уплътнения се различават от стандартните уплътнения?
Медицинските кабелни втулки се различават от стандартните втулки чрез използване на биосъвместими материали, гладки почистващи се повърхности, отговарящи на изискванията на FDA, осигуряващи подобрено уплътняване за предотвратяване на замърсяване и химическа устойчивост на почистващи препарати и процеси на стерилизация, със специализирани конструкции, които премахват пукнатините, в които могат да се задържат бактерии, като същевременно поддържат електрическите характеристики в критични за здравеопазването среди.
Разбирането на тези разлики е от решаващо значение, тъй като медицинските приложения имат уникални изисквания за безопасност и регулаторни изисквания, на които стандартните индустриални салници не могат да отговорят адекватно.
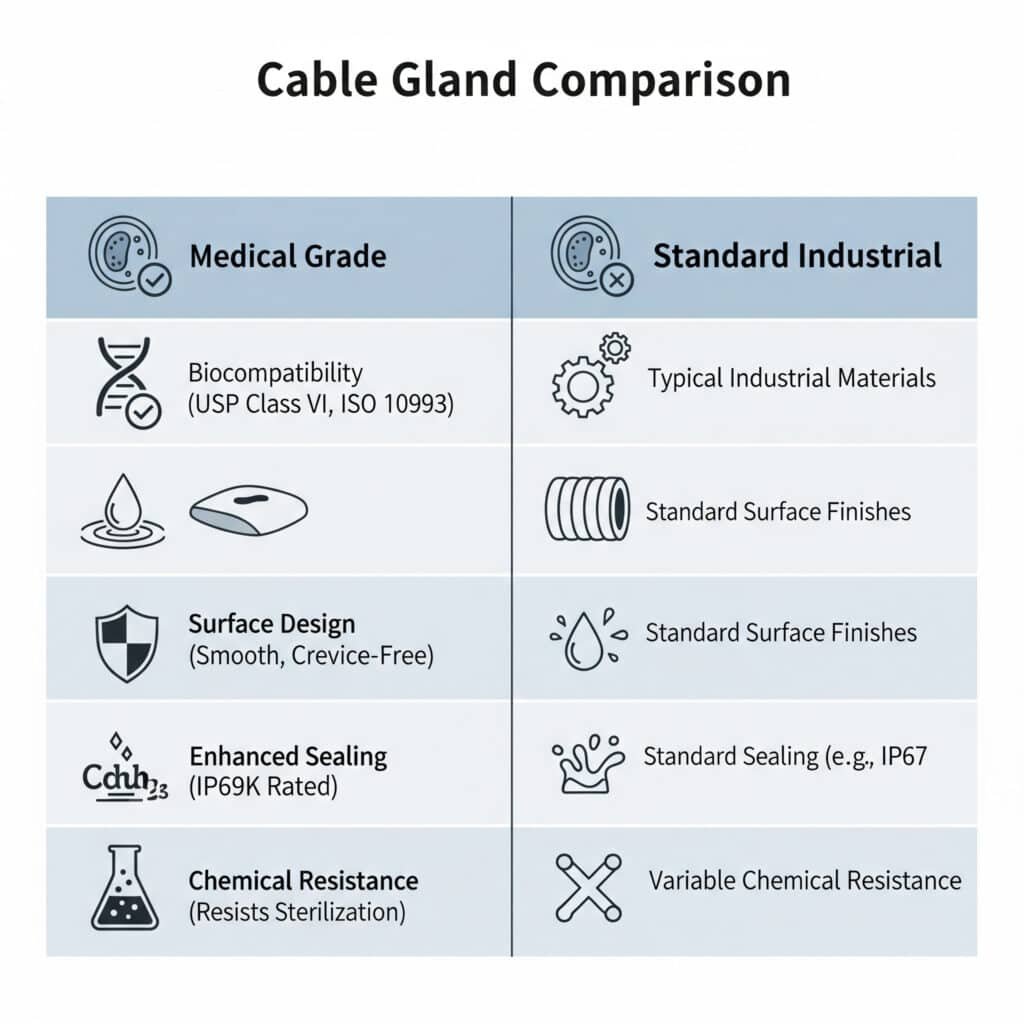
Изисквания за биосъвместимост
Съответствие с клас VI на USP: В медицинските кабелни жлези трябва да се използват материали, които преминават биологично изпитване по фармакопеята на САЩ, клас VI, за биосъвместимост и безопасност при приложенията на медицински изделия.
Стандарти ISO 10993: Материалите трябва да отговарят на ISO 109932 стандартите за биологична оценка на медицинските изделия, които гарантират, че няма цитотоксични, сенсибилизиращи или дразнещи ефекти върху човешката тъкан.
Одобрение на FDA 21 CFR 177: Материалите за хранително-вкусовата промишленост, отговарящи на изискванията на FDA за директен и индиректен контакт с храни, често се изискват за приложения във фармацевтиката и медицинските изделия.
Биосъвместими полимери: Специализирани материали като медицински PEEK, PTFE или фармацевтични найлони осигуряват биосъвместимост, без да се нарушават механичните свойства.
Дизайн на повърхността за почистване
Гладко покритие на повърхността: Медицинските жлези се отличават с изключително гладки повърхности със стойности на Ra обикновено под 0,8 микрометра, за да се предотврати залепването на бактерии и да се осигури ефективно почистване.
Дизайн без пукнатини: Елиминиране на острите ъгли, дълбоките нишки и сложните геометрични форми, които могат да задържат бактерии или да се противопоставят на процесите на почистване и стерилизация.
Заоблени ръбове: Всички външни повърхности са със заоблени ръбове и гладки преходи, за да се улесни почистването и да се предотврати повреждането на ръкавици за чисти помещения или стерилни опаковки.
Минимална площ на повърхността: Обтекаемите конструкции намаляват до минимум площта на повърхността, изложена на замърсяване, като същевременно поддържат необходимите механични и електрически характеристики.
Подобрена ефективност на уплътняването
Класификация IP68+: Превъзходна защита на околната среда отвъд стандартното ниво IP68, като често се постига IP69K за приложения за почистване при високо налягане и висока температура.
Бариери за замърсяване: Многобройните етапи на уплътняване предотвратяват проникването на частици, бактерии и почистващи химикали, които биха могли да застрашат стерилната среда.
Устойчивост на налягане: Повишени стойности на налягането, за да издържат на агресивни процедури за почистване и стерилизация без повреда на уплътнението.
Дългосрочна надеждност: Материалите за уплътняване запазват целостта си при многократни цикли на стерилизация и излагане на въздействието на агресивни почистващи химикали.
Свойства на химическа устойчивост
Съвместимост с почистващи препарати: Устойчивост на болнични дезинфектанти, четвъртични амониеви съединения, водороден пероксид и други агресивни почистващи химикали.
Устойчивост на стерилизация: Материалите издържат на гама-лъчение, етиленов оксид, автоклавиране с пара и други методи за стерилизация, без да се разрушават.
Фармацевтични химикали: Устойчивост на разтворители, киселини, основи и фармацевтични съединения, често срещани в медицинската производствена среда.
Температурна стабилност: Поддържане на свойствата чрез температурни цикли на стерилизация и изисквания за контрол на температурата в чисти помещения.
Дейвид, мениджър на съоръжения в голям фармацевтичен завод в Ню Джърси, се сблъсква с повтарящи се проблеми със замърсяването на стерилните линии за пълнене, където стандартните кабелни канали са задържали бактерии въпреки строгите протоколи за почистване. Съществуващите месингови уплътнители имаха сложни модели на резба и повърхностни покрития, които не можеха да бъдат адекватно стерилизирани, което водеше до отхвърляне на партиди и проблеми със съответствието с изискванията на FDA. Определихме кабелни втулки от медицинска неръждаема стомана с електрополирани повърхности и дизайн без пукнатини, които отговарят на изискванията на USP Class VI. Модернизацията елиминира източниците на замърсяване, постигна 99,9% ефективност на почистване и помогна на предприятието да премине проверките на FDA, като същевременно намали процента на бракуваните продукти с 85%. 😊
Как да спазвате правилата на FDA и на медицинските изделия?
Спазването на разпоредбите на FDA и на правилата за медицинските изделия изисква използването на материали с подходящи сертификати, воденето на подробна документация, спазването на Добри производствени практики (ДПП)3, осигуряване на проследяемост и прилагане на системи за качество, които отговарят на изискванията на 21 CFR, част 820, като медицинските кабелни канали изискват одобрени от FDA материали, изпитване за биосъвместимост и производствен контрол, които осигуряват постоянно качество и безопасност при приложенията на медицински изделия.
Съответствието с нормативните изисквания е задължително в медицинските приложения, тъй като неизправностите могат да доведат до увреждане на пациентите, изтегляне на продукти и тежки правни последици.
Изисквания към материалите на FDA
21 CFR, част 177: Материалите, които са в контакт с фармацевтични продукти или медицински изделия, трябва да отговарят на изискванията на FDA за добавки към храни за вещества, които са в непряк контакт с храни.
Основен файл за достъп (MAF): Доставчиците трябва да поддържат главните досиета за достъп на FDA, документиращи безопасността на материалите, производствените процеси и процедурите за контрол на качеството.
Основно досие на лекарството (DMF): За фармацевтичните приложения материалите може да изискват регистрация на главното досие на лекарството с подробна информация за състава и производството.
Сертификат за съответствие: Доставчиците трябва да предоставят сертификати, потвърждаващи, че материалите отговарят на всички приложими разпоредби и спецификации на FDA.
Стандарти за качество на медицинските изделия
Съответствие с ISO 13485: Производството трябва да следва системите за управление на качеството на медицинските изделия по ISO 13485 за проектиране, производство и надзор след пускане на пазара.
21 CFR, част 820 (QSR): Съответствие с нормативната уредба на системата за качество, като се гарантира подходящ контрол на проектирането, контрол на документите и коригиращи/превантивни действия.
Управление на риска: ISO 14971 процеси за управление на риска за медицински изделия, включително анализ на риска, оценка и мерки за контрол.
Контрол на дизайна: Формални процеси за контрол на проектирането, включително планиране на проектирането, изисквания за вход/изход, прегледи, проверка и валидиране.

Документиране и проследимост
Сертификати за материал: Пълна проследимост на материалите със сертификати за анализ, резултати от тестове за биосъвместимост и документация за съответствие с нормативните изисквания.
Производствени записи: Подробни производствени записи, включително параметри на процеса, тестове за контрол на качеството и документация за партидите за пълно проследяване.
Контрол на промените: Официални процедури за контрол на промените за всякакви модификации на материали, процеси или спецификации, които засягат регулаторното съответствие.
Квалификация на доставчика: Изчерпателни програми за квалификация на доставчиците, гарантиращи, че всички материали и компоненти отговарят на изискванията за медицински изделия.
Изисквания за валидиране
Изпитване за биосъвместимост: USP Class VI тестове, включително системно инжектиране, интракутанни тестове и тестове за имплантиране, за да се провери биологичната безопасност.
Валидиране на почистването: Документирани процедури за почистване с данни за валидиране, доказващи ефективното отстраняване на замърсителите и намаляване на биологичното натоварване.
Валидиране на стерилизацията: Валидиране на процесите на стерилизация, включително картографиране на дозите, нива на осигуряване на стерилност и проучвания за съвместимост на материалите.
Тестване на производителността: Електрически, механични и екологични тестове за проверка на съответствието на характеристиките с изискванията за медицински изделия през целия жизнен цикъл на продукта.
Подкрепа за подаване на регулаторни документи
Документация 510(k): Техническа документация, подкрепяща подаването на документи за FDA 510(k) за медицински изделия, включващи кабелни канали.
Технически файлове: Изчерпателни технически досиета за маркировка CE съгласно Регламента за медицинските изделия (MDR) на европейските пазари.
Споразумения за качество: Официални споразумения за качество с доставчиците, определящи отговорностите, спецификациите и изискванията за съответствие.
Одиторска подкрепа: Подкрепа за одити на FDA, нотифицирани органи и клиенти, включително преглед на документацията и инспекции на съоръженията.
Какви материали са необходими за приложения в чисти помещения?
Приложенията за чисти помещения изискват материали с ниски изпускащи свойства, устойчивост на образуване на частици, химическа съвместимост с почистващи препарати, гладки непорьозни повърхности и подходящи нива на проводимост, като неръждаемата стомана 316L, PEEK, PTFE и специализираните полимери, одобрени за чисти помещения, осигуряват оптимална производителност, като същевременно отговарят на изискванията. ISO 146444 стандарти за чисти помещения и поддържане на електрическата цялост в контролирани среди.
Изборът на материали е от решаващо значение, тъй като чистите помещения изискват строг контрол на замърсяването с частици и молекули, което може да застраши качеството на продукта или стерилните условия.
Изисквания за неръждаема стомана
316L Медицински клас: Аустенитна неръждаема стомана с ниско съдържание на въглерод, осигуряваща отлична устойчивост на корозия и биосъвместимост за медицински приложения.
Електрополирано покритие: Електрополирането отстранява несъвършенствата на повърхността, намалява образуването на частици и създава гладки повърхности за ефективно почистване.
Обработка за пасивиране: Химическото пасивиране повишава устойчивостта на корозия и премахва замърсяването с желязо, което може да доведе до промяна на цвета или образуване на частици.
Грапавост на повърхността: Стойностите на Ra под 0,8 микрометра (32 микроинча) свеждат до минимум бактериалната адхезия и улесняват процесите на почистване и стерилизация.
Високоефективни полимери
ПЕЕК (полиетеркетон): Отличната химическа устойчивост, ниското изпускане на газове и биосъвместимостта правят PEEK идеален за приложения във фармацевтиката и медицинските изделия.
PTFE (политетрафлуороетилен): Превъзходната химическа инертност и незалепващите свойства осигуряват отлична устойчивост на почистващи химикали и биологични материали.
Медицински найлони: Специално разработените найлони с одобрение по USP Class VI предлагат добри механични свойства и биосъвместимост за медицински приложения.
POM, одобрен за чисти помещения: Полиоксиметилен с ниско ниво на образуване на частици и добра стабилност на размерите за прецизни приложения в чисти помещения.
Съвместимост с класификацията за чисти помещения
ISO клас 5 (клас 100): Свръхгладки повърхности с минимално генериране на частици за приложения в производството на полупроводници и фармацевтични продукти.
ISO клас 6 (клас 1000): Умерен контрол на частиците при производството на медицински изделия и някои фармацевтични процеси.
ISO клас 7 (клас 10000): Стандартни изисквания за чисти помещения за общи операции по сглобяване на фармацевтични продукти и медицински изделия.
ISO клас 8 (клас 100000): Основни изисквания за чисти помещения за опаковане и някои процеси за производство на медицински изделия.
Контрол на изпускането на газове и замърсяването
Материали с ниско ниво на изпускане на газове: Материали с минимални емисии на летливи органични съединения (ЛОС), които могат да замърсят чувствителни процеси или продукти.
Молекулярно замърсяване: Контрол на молекулярните замърсители, включително силикони, пластификатори и други органични съединения, които могат да повлияят на качеството на продукта.
Йонно замърсяване: Материали с ниско съдържание на йони за предотвратяване на замърсяването на електронни компоненти и фармацевтични продукти.
Екстрахируеми вещества: Минимално количество екстрахируеми вещества, които биха могли да попаднат във фармацевтични продукти или почистващи разтвори по време на употреба.
Матрица за химическа съвместимост
| Почистващ агент | 316L SS | PEEK | PTFE | Медицински найлон |
|---|---|---|---|---|
| Изопропилов алкохол | Отличен | Отличен | Отличен | Добър |
| Водороден пероксид | Отличен | Отличен | Отличен | Fair |
| Четвъртичен амоний | Отличен | Отличен | Отличен | Добър |
| Натриев хипохлорит | Добър | Отличен | Отличен | Беден |
| Пероцетна киселина | Добър | Отличен | Отличен | Беден |
Хасан, който управлява операциите в модерно фармацевтично предприятие в Швейцария, се нуждае от модернизиране на кабелните канали в чистата стая от клас 5 по ISO за производство на стерилни инжекционни продукти. Съществуващите железа генерират частици по време на циклите на почистване и не могат да издържат на агресивните протоколи за стерилизация, необходими за новите им биологични продукти. Предоставихме кабелни втулки от неръждаема стомана 316L с потвърдено ниско ниво на генериране на частици и пълна химическа съвместимост с техните процеси на почистване и стерилизация. Модернизацията постигна брой частици 90% под границите на ISO клас 5, елиминира свързаните с почистването случаи на замърсяване и подпомогна успешното валидиране на новата им стерилна производствена линия.
Как да гарантирате правилната съвместимост при почистване и стерилизация?
Осигуряването на подходящо почистване и съвместимост със стерилизацията изисква избор на материали, които издържат на многократно излагане на почистващи химикали и методи за стерилизация, проектиране на повърхности за пълно почистване, валидиране на процедурите за почистване и поддържане на подробна документация, като медицинските кабелни канали изискват гладки повърхности без пукнатини, химически устойчиви материали и валидирани протоколи за почистване, които постигат необходимите нива на осигуряване на стерилност.
Съвместимостта на почистването и стерилизацията е от съществено значение, тъй като неадекватното обеззаразяване може да доведе до замърсяване на продукта, рискове за безопасността на пациентите и нарушения на нормативните изисквания.
Съвместимост на методите за стерилизация
Автоклавиране с пара: Материалите трябва да издържат на 121°C-134°C автоклавиране с пара5 цикъла без влошаване, промяна на размерите или повреда на уплътнението.
Гама лъчение: Устойчивост на дози гама-лъчение от 25-50 kGy, които обикновено се използват за стерилизация на медицински изделия, без деградация на материала.
Етиленов оксид (EtO): Химическа съвместимост със стерилизацията с EtO, включително устойчивост на стерилизатора и подходящи характеристики на дегазация.
Плазма с водороден пероксид: Съвместимост със системите за нискотемпературна плазмена стерилизация, включително стабилност на материала и пълно проникване на стерилизатора.
Изисквания за валидиране на почистването
Процедури за почистване: Документирани процедури за почистване, определящи химикалите, концентрациите, времето за контакт и механичните действия, необходими за ефективно обеззаразяване.
Протоколи за валидиране: Официални проучвания за валидиране, доказващи ефективността на почистването, като се използват най-лошите сценарии на замърсяване и аналитични тестове.
Критерии за приемливост: Определени критерии за приемане на чистотата, включително визуална проверка, брой частици, нива на биологична натовареност и граници на химически остатъци.
Рутинно наблюдение: Програми за текущ мониторинг, за да се провери постоянната ефективност на почистването и да се идентифицира всяко влошаване на ефективността.
Съображения за дизайна на повърхността
Дренажни функции: Конструктивни характеристики, които подпомагат пълното оттичане на почистващите разтвори и предотвратяват образуването на басейни, в които могат да се задържат замърсители.
Достъпност: Всички повърхности трябва да са достъпни за почистване със стандартни инструменти и процедури, използвани в медицинските заведения.
Изисквания за разглобяване: Помислете дали е необходимо да се разглобяват салниците за почистване или дали непокътнатото почистване е достатъчно за приложението.
Смяна на уплътнението: Процедури за подмяна на уплътнения и валидиране, когато уплътнителните компоненти изискват периодична подмяна поради излагане на почистващи химикали.
Документация и съответствие
Инструкции за почистване: Подробни инструкции за почистване, включващи процедури стъпка по стъпка, спецификации на химикалите и предпазни мерки за безопасност.
Данни за безопасност на материала: Пълна информация за безопасност на материалите, включително химическа съвместимост, температурни граници и съвместимост при стерилизация.
Доклади за валидиране: Доклади за валидиране на почистването, доказващи ефективността, и установяване на изисквания за рутинен мониторинг.
Материали за обучение: Материали за обучение на персонала на лечебното заведение относно правилното почистване, работа и процедури за поддръжка на медицински кабелни канали.
Тестване за контрол на качеството
Изпитване на бионатоварването: Редовно тестване за микробно замърсяване с цел проверка на ефективността на почистването и идентифициране на потенциални проблемни области.
Тестване на ендотоксини: Тестване за бактериални ендотоксини, които могат да предизвикат пирогенни реакции във фармацевтиката и медицинските изделия.
Преброяване на частиците: Тестване на броя на частиците, за да се провери дали изискванията за чисти помещения са спазени след дейностите по почистване и поддръжка.
Анализ на химическите остатъци: Тестване за остатъци от почистващи химикали, които могат да замърсят продуктите или да повлияят на биосъвместимостта.
Какви са основните критерии за избор на различни медицински приложения?
Основните критерии за избор варират в зависимост от приложението, но включват изисквания за съответствие с нормативните изисквания, нива на биосъвместимост, класификации за чисти помещения, методи за стерилизация, излагане на химикали и нужди от електрически характеристики, като хирургическото оборудване изисква най-висока биосъвместимост, фармацевтичното производство се нуждае от химическа устойчивост, а диагностичното оборудване се фокусира върху електрическата цялост, докато всички приложения изискват подходящи регулаторни сертификати и съвместимост при почистване.
Различните медицински приложения имат уникални изисквания, които трябва да бъдат внимателно разгледани при избора на кабелни уплътнения, за да се гарантира оптимална производителност и съответствие с нормативните изисквания.
Хирургично оборудване и оборудване за контакт с пациенти
Изисквания за пряк контакт: Биологична съвместимост клас VI по USP с допълнително тестване за цитотоксичност за материали в пряк контакт с пациента по време на хирургични процедури.
Честота на стерилизация: Възможност за издържане на чести цикли на стерилизация без деградация, като обикновено се изискват материали, устойчиви на стотици цикли на стерилизация.
Електрическа безопасност: Засилени изисквания за електрическа безопасност, включително нисък ток на утечка и надеждна изолация за оборудване, свързано с пациента.
Аварийна надеждност: Критични изисквания за надеждност на животоподдържащо и спешно медицинско оборудване, при което повредата може да окаже пряко въздействие върху безопасността на пациентите.
Фармацевтично производство
Съответствие с GMP: Изисквания за добра производствена практика, включително проследимост на материалите, контрол на промените и документация за валидиране.
Безопасност при контакт с продукта: Материали, които не замърсяват фармацевтичните продукти чрез отмиване, образуване на частици или химическо взаимодействие.
Валидиране на почистването: Обширни изисквания за валидиране на почистването с документирани процедури и критерии за приемане за фармацевтично производство.
Документация за партиди: Пълно документиране на партидите и проследяване на материалите, използвани във фармацевтичното производствено оборудване.
Диагностично и лабораторно оборудване
Изисквания за прецизност: Стабилност на размерите и прецизност за аналитични инструменти, изискващи постоянни механични и електрически характеристики.
Химическа устойчивост: Устойчивост на лабораторни химикали, реактиви и разтворители за почистване, които обикновено се използват в диагностичните приложения.
Производителност на EMC: Изисквания за електромагнитна съвместимост за чувствителни аналитични инструменти и диагностично оборудване.
Стабилност на калибрирането: Механична стабилност, която няма да повлияе на калибрирането на инструмента или точността на измерването с течение на времето.
Производство на медицински изделия
Валидиране на процеса: Материали и компоненти, които поддържат изискванията за валидиране на процесите при производството на медицински изделия.
Системи за качество: Интегриране със системите за качество по ISO 13485, включително процедурите за квалификация на доставчиците и входящата инспекция.
Управление на риска: Материали, които поддържат изискванията за управление на риска на медицинските изделия, включително анализ на режимите на неизправност и стратегии за намаляване на риска.
Регулаторна подкрепа: Подкрепа на доставчика за подаване на регулаторни документи, включително техническа документация и експертен опит в областта на регулирането.
Матрица за вземане на решения за избор
| Тип приложение | Основни критерии | Вторични критерии | Критични стандарти |
|---|---|---|---|
| Хирургично оборудване | Биосъвместимост | Стерилизация | USP Class VI, ISO 10993 |
| Фармацевтични продукти | Химическа устойчивост | Съответствие с GMP | FDA 21 CFR, cGMP |
| Диагностика | Прецизност | Производителност на EMC | IEC 61326, ISO 15189 |
| Производство | Валидиране на процеса | Системи за качество | ISO 13485, 21 CFR 820 |
Анализ на разходите и ползите
Първоначални разходи спрямо жизнен цикъл: Вземете предвид общите разходи за притежание, включително разходите за поддръжка, подмяна и спазване на изискванията по време на целия живот на оборудването.
Регулаторен риск: Балансирайте материалните разходи спрямо рисковете за спазване на нормативните изисквания и потенциалните разходи при неспазване на изискванията.
Изисквания за изпълнение: Уверете се, че избраните материали отговарят на минималните изисквания за изпълнение, без да се допускат прекомерни спецификации, които ненужно увеличават разходите.
Възможности на доставчика: Оценяване на възможностите на доставчиците за текуща поддръжка, документация и помощ за спазване на нормативните изисквания.
Заключение
Изборът на кабелни уплътнения за медицинско оборудване и чисти помещения изисква разбиране на уникалните регулаторни изисквания, изисквания към материалите и характеристиките, които отличават тези приложения от стандартните промишлени приложения. Успехът зависи от балансирането на биосъвместимостта, почистването, спазването на нормативните изисквания и електрическите характеристики.
Ключът към надеждното функциониране на медицинските кабелни жлези се крие в работата с доставчици, които разбират разпоредбите за медицинските изделия и могат да предоставят подходящи материали, документация и постоянна поддръжка през целия жизнен цикъл на продукта. В Bepto сме специализирани в кабелни втулки за медицински цели, които отговарят на изискванията на FDA и международните стандарти за медицински изделия, като осигуряваме гаранция за качество и регулаторна поддръжка, необходими за критични приложения в здравеопазването.
Често задавани въпроси за медицинските кабелни втулки
В: Какви сертификати са необходими за медицинските кабелни салници?
A: Медицинските кабелни канали обикновено изискват сертификат за биосъвместимост USP Class VI, съответствие с FDA 21 CFR за материалите и системи за качество на производството ISO 13485. Специфичните изисквания зависят от вашето приложение и регулаторна юрисдикция.
В: Могат ли обикновените кабелни уплътнения от неръждаема стомана да се използват в медицински приложения?
A: Обикновената неръждаема стомана може да не отговаря на медицинските изисквания. Медицинските приложения се нуждаят от медицинска неръждаема стомана 316L с електрополирано покритие, изпитване за биосъвместимост и подходяща документация за съответствие с нормативните изисквания.
В: Как да почиствам и стерилизирам медицински кабелни жлези?
A: Следвайте утвърдените от производителя процедури за почистване, като използвате одобрени почистващи препарати и методи за стерилизация. Повечето медицински жлези поддържат автоклавиране с пара, гама-лъчение или химическа стерилизация при подходяща съвместимост на материалите.
В: Каква е разликата между кабелните уплътнения за чисти помещения и за медицински цели?
A: Медицинският клас включва изисквания за биосъвместимост и съответствие с изискванията на FDA, докато класът за чисти помещения се фокусира върху контрола на частиците и химическата устойчивост. Някои приложения изискват едновременно медицински спецификации и спецификации за чисти помещения.
В: Колко често трябва да се сменят медицинските кабелни жлези?
A: Честотата на подмяна зависи от циклите на стерилизация, излагането на химикали и препоръките на производителя. Обикновено се проверява след всеки 100-200 цикъла на стерилизация и се подменя въз основа на оценката на състоянието и изискванията за валидиране.
-
Научете повече за специфичните тестове за биологична реактивност, които се изискват за сертифициране по USP Class VI. ↩
-
Направете преглед на серията стандарти ISO 10993 за биологична оценка на медицински изделия. ↩
-
Прегледайте официалните насоки и разпоредби на FDA за текущи добри производствени практики (cGMP). ↩
-
Разгледайте подробно ръководство за стандартите ISO 14644 за класифициране на чистотата на въздуха в чисти помещения. ↩
-
Разберете принципите на стерилизация с пара, включително ролята на времето, температурата и налягането. ↩



